相关试卷
- 备考2026届高考 2021-2025全国各地真题汇编 专题14 化学实验综合
- 备考2026届高考 2021-2025全国各地真题汇编 专题13 生命活动的物质基础 有机合成
- 备考2026届高考 2021-2025全国各地真题汇编 专题11 盐类水解和沉淀溶解平衡
- 备考2026届高考 2021-2025全国各地真题汇编 专题10 弱电解质的电离平衡和溶液的酸碱性
- 备考2026届高考 2021-2025全国各地真题汇编 专题9 化学反应速率与化学平衡
- 备考2026届高考 2021-2025全国各地真题汇编 专题8 化学反应与电能
- 备考2026届高考 2021-2025全国各地真题汇编 专题7 化学反应的热效应
- 备考2026届高考 2021-2025全国各地真题汇编 专题6 化学键 分子和晶体的结构与性质
- 备考2026届高考 2021-2025全国各地真题汇编 专题5 原子结构元素周期律
- 备考2026届高考 2021-2025全国各地真题汇编专题4非金属及其化合物
-
1、二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应(忽略其他副反应):
反应①:
反应②:
在密闭容器中,、时,催化反应相同时间,测得不同温度下转化率、的选择性如图中实线所示(图中虚线表示相同条件下的平衡转化率随温度的变化)。选择性。下列说法正确的是
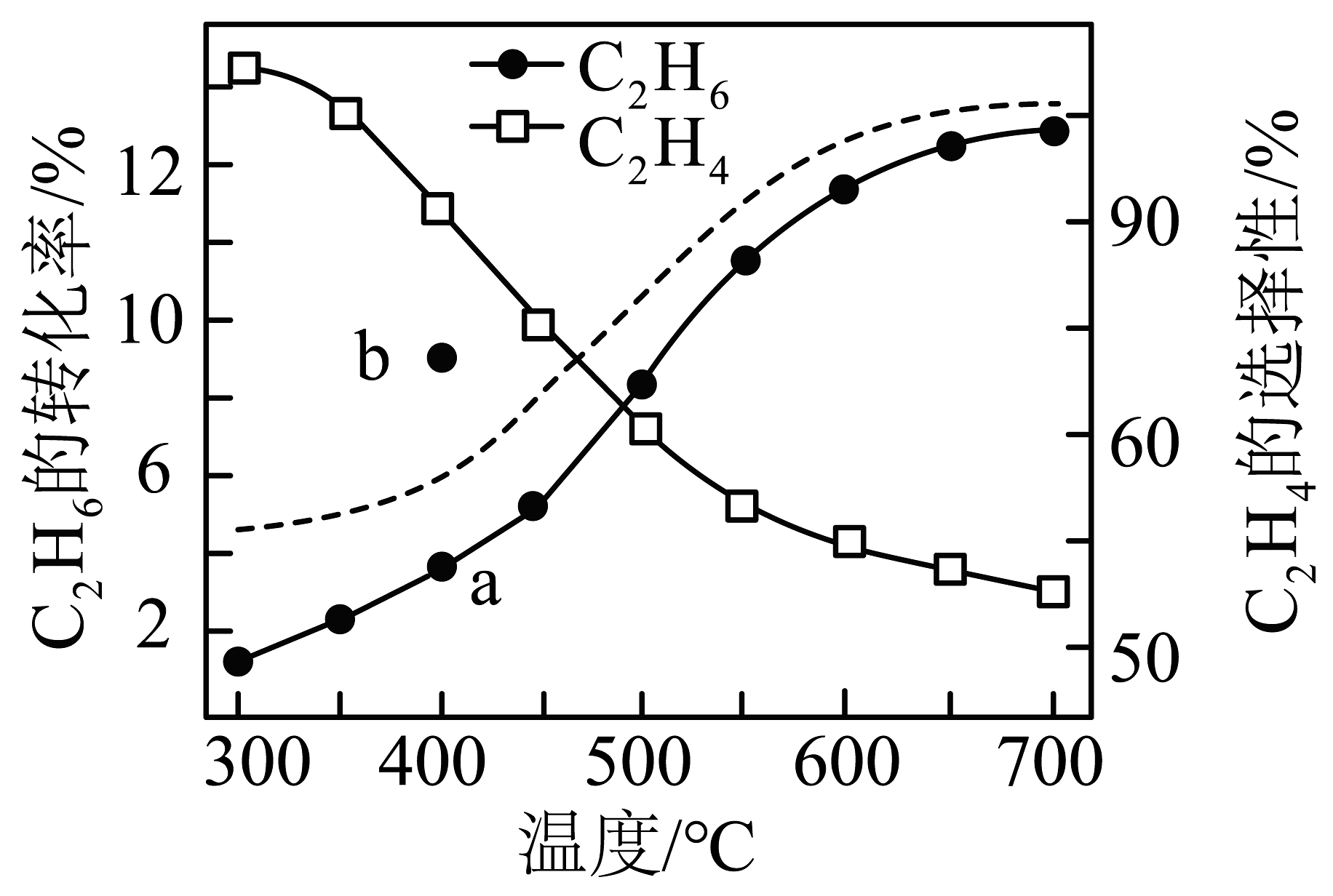 A、反应过程中,的转化率大于的转化率 B、在300~700℃之间,的选择性下降的原因是随温度升高反应①平衡后又向逆反应方向移动 C、保持其他条件不变,400℃时使用高效催化剂能使的转化率从a点的值升高到b点的值 D、随温度升高,转化率接近平衡转化率的主要原因是温度和催化剂共同影响,加快了反应速率
A、反应过程中,的转化率大于的转化率 B、在300~700℃之间,的选择性下降的原因是随温度升高反应①平衡后又向逆反应方向移动 C、保持其他条件不变,400℃时使用高效催化剂能使的转化率从a点的值升高到b点的值 D、随温度升高,转化率接近平衡转化率的主要原因是温度和催化剂共同影响,加快了反应速率 -
2、室温下,通过下列实验探究溶液的性质。
实验1:用pH计测量溶液的pH,测得pH为12.65.
实验2:向的溶液中通入气体至(忽略溶液体积的变化及的挥发)。
实验3:向的溶液中加入溶液。
已知: , , , 。
下列说法正确的是
A、实验1所得溶液中: B、实验2所得溶液中: C、实验3中:反应的平衡常数 D、向溶液中通入少量的离子方程式 -
3、室温下,根据下列卤素单质及其化合物的实验过程及现象,能验证相应实验结论的是
选项
实验过程及现象
实验结论
A
向溶液中通入 , 有白色沉淀产生
酸性:
B
向溶液中先滴加4滴溶液,出现白色沉淀,再滴加4滴溶液,出现黄色沉淀
溶度积常数:
C
用pH计分别测定溶液和溶液pH,溶液pH大
结合能力:
D
向溶液中加入碘单质,有黄绿色气体产生
氧化性:
A、A B、B C、C D、D -
4、利用电解可以将气态苯(
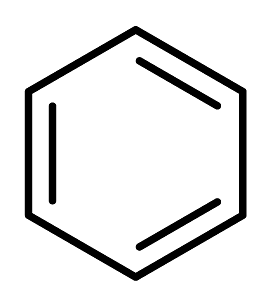 )转化为环己烷(
)转化为环己烷( ),其电解装置如图所示。下列有关说法正确的是
),其电解装置如图所示。下列有关说法正确的是 A、电解时,电极A与电源的正极相连 B、电解时,电极B上产生的气体为 C、反应中每生成
A、电解时,电极A与电源的正极相连 B、电解时,电极B上产生的气体为 C、反应中每生成 , 转移电子数为
D、电解的总反应方程式:
, 转移电子数为
D、电解的总反应方程式:
-
5、化合物Z是一种药物的重要中间体,部分合成路线如下:

下列说法正确的是
A、X分子中含有2个手性碳原子 B、Y分子不存在顺反异构体 C、Z不能与的溶液反应 D、X、Y、Z均能与溶液反应 -
6、在给定条件下,下列制备过程涉及的物质转化不能实现的是A、金属铝制备: B、锅炉除垢: C、酸雨形成: D、检验葡萄糖:
-
7、阅读下列材料,完成下面小题:
铜及其重要化合物在生产中有着重要的应用。在存在下能与氨水反应生成。单质铜作催化剂可以将氧化为。是一种良好的离子型半导体,加入稀硫酸中,溶液变蓝色并有紫红色固体产生。高温下可以被氧化为和 , 将制得的粗铜通过电解精炼得铜。的盐酸溶液能吸收形成配合物 , 结构如图所示。
 (1)、下列有关说法正确的是A、和中碳原子杂化类型均为 B、与形成 , 提供孤对电子 C、中含有键的数目为 D、、、三者晶体的类型相同(2)、下列化学反应表示正确的是A、、和氨水反应生成: B、被氧化为: C、中加入稀硫酸: D、电解精炼铜阴极上电极反应:(3)、下列说法正确的是A、氧化为中,单质铜能降低反应的焓变 B、具有良好的半导体性能,是利用其晶体与硅晶体类型相同 C、高温下被氧化反应中,既是氧化剂又是还原剂 D、的盐酸溶液可用于吸收 , 是利用了的氧化性
(1)、下列有关说法正确的是A、和中碳原子杂化类型均为 B、与形成 , 提供孤对电子 C、中含有键的数目为 D、、、三者晶体的类型相同(2)、下列化学反应表示正确的是A、、和氨水反应生成: B、被氧化为: C、中加入稀硫酸: D、电解精炼铜阴极上电极反应:(3)、下列说法正确的是A、氧化为中,单质铜能降低反应的焓变 B、具有良好的半导体性能,是利用其晶体与硅晶体类型相同 C、高温下被氧化反应中,既是氧化剂又是还原剂 D、的盐酸溶液可用于吸收 , 是利用了的氧化性 -
8、摩尔盐可以用于配制标准溶液。下列说法正确的是A、半径: B、第一电离能: C、电负性: D、热稳定性:
-
9、实验室利用废旧干电池废料(主要成分、、、碳粉等)回收。下列相关原理、装置及操作不正确的是
 A、用装置甲配制稀硫酸 B、用装置乙溶解废料 C、用装置丙过滤分离混合物 D、用装置丁灼烧获得
A、用装置甲配制稀硫酸 B、用装置乙溶解废料 C、用装置丙过滤分离混合物 D、用装置丁灼烧获得 -
10、反应可用于航天器中吸收。下列说法正确的是A、的结构示意图为
 B、中子数为8的氧原子:
C、为极性分子
D、中既含离子键又含极性键
B、中子数为8的氧原子:
C、为极性分子
D、中既含离子键又含极性键
-
11、侯德榜发明的侯氏制碱法造福了全人类。侯氏制碱法中的“碱”指的是A、 B、 C、 D、
-
12、
中国首次实现了利用二氧化碳人工合成淀粉,为全球的“碳达峰”、“碳中和”起到重大的支撑作用,研究二氧化碳的收集和利用成为了科研方面的热点。
I.热化学法将转化为甲醇
反应①
反应②
(已知:(或)的选择性)
将和混合气体以一定流速通过装有催化剂反应器,选择性、的转化率与温度的关系如图所示。

(1)230℃时,测得的转化率为40%,此时剩余的物质的量为。
(2)随着温度的升高,的转化率增大,其主要原因是。
(3)其他条件不变,增大压强,CO选择性变化为(填“不变”、“变大”或“变小”)。
II.和催化重整制取和
1991年,Ashcroft提出了甲烷二氧化碳重整的技术理论:500℃条件下,气体分子吸附至催化剂表面后发生反应,此过程机理模型如图所示(*表示吸附在催化剂表面的活性物种)。

(4)根据图示写出该反应的化学方程式:。
(5)在催化剂中添加少量多孔能提高转化率,其原因是。
(6)根据反应机理,该催化重整的过程可描述为。
-
13、工业上以金焙砂酸浸液(主要成分为和 , 忽略其它杂质)与硫铁矿(主要成分为 , 忽略其它杂质)为原料制备的流程如下:

回答下列问题:
(1)、硫铁矿和金焙砂酸浸液反应的离子方程式为。还原时间与还原率的关系如图所示,则最佳还原时间为小时。 (2)、加调时,与悬浊液中关系如图所示,则调为(填具体值),向调后的溶液中通入空气的目的是。
(2)、加调时,与悬浊液中关系如图所示,则调为(填具体值),向调后的溶液中通入空气的目的是。 (3)、已知:可以制备晶体。请补充完整以溶液为原料制备的实验方案:取溶液, , 静置、过滤、洗涤、干燥。(实验中须选用的试剂:稀硫酸、双氧水、1mol·L-1溶液、溶液)(4)、亚铁盐常用于氧化还原滴定。某实验测定样品中质量分数的方法如下。取样品,加水溶解,加入过量 , 充分反应后,将溶液加热煮沸除去剩余 , 冷却至室温,加入硫酸酸化,再加入标准溶液 , 充分反应后,用酸性溶液滴定过量的溶液至终点,到达滴定终点时消耗溶液的体积为。
(3)、已知:可以制备晶体。请补充完整以溶液为原料制备的实验方案:取溶液, , 静置、过滤、洗涤、干燥。(实验中须选用的试剂:稀硫酸、双氧水、1mol·L-1溶液、溶液)(4)、亚铁盐常用于氧化还原滴定。某实验测定样品中质量分数的方法如下。取样品,加水溶解,加入过量 , 充分反应后,将溶液加热煮沸除去剩余 , 冷却至室温,加入硫酸酸化,再加入标准溶液 , 充分反应后,用酸性溶液滴定过量的溶液至终点,到达滴定终点时消耗溶液的体积为。已知:酸性条件下与和反应的离子方程式如下:
①加入的目的是除去 , 已知反应后生成 , 写出该反应的化学方程式:。
②计算样品中的质量分数(写出计算过程)。
-
14、物质在水中存在电离平衡、水解平衡。请根据所学知识回答:(1)、25℃时,体积均为10 mL,pH均为2的醋酸溶液与一元酸溶液分别加水稀释至1000 mL,稀释过程中pH的变化如图所示。

①25℃时,醋酸的电离常数HX的电离常数。(填“>”、“<”或“=”,下同)
②稀释100倍后,醋酸溶液中由水电离出的c(H+)HX溶液中由水电离出的c(H+)。
(2)、泡沫灭火器的原理是硫酸铝、碳酸氢钠溶液之间发生反应。①NaHCO3溶液呈碱性的原因是(用离子方程式表示)
②使用时将灭火器倒过来摇动即可,试写出该反应的离子方程式:。
(3)、常温下,将pH=2的HA溶液和pH=12的溶液等体积混合,混合溶液的pH=5。该混合溶液中c(A-)-c(Na+)=mol/L(填准确数值,无需计算)。(4)、已知:二元酸H2R电离方程式是 , , 假设0.1 mol/LNaHR溶液c(H+)=a mol/L,则0.1 mol/LH2R溶液中c(H+)是___________A、小于 B、大于 C、等于 D、等于(5)、T℃时Kw=10-13 , 该温度下将Va LpH=a的NaOH溶液与VbL 10-b mol/L硫酸混合。若所得混合溶液呈中性,且a=12,b=1,则Va:Vb;若Va:Vb=1:3,且a=11,b=3,则所得溶液的pH=。 -
15、食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于 , 实验室用标准溶液测定食醋中醋酸的浓度,以检测食醋是否符合国家标准,某品牌白醋的醋酸浓度测定过程如图所示:

 (1)、选用(填“甲”或“乙”)滴定管量取白醋后,滴定管读数如丙图所示,此时液面显示读数为 , 将其稀释至备用。(2)、为尽可能的减少实验误差,应该选(填“酚酞”、“甲基橙”或“石蕊”)作指示剂。(3)、用标准氢氧化钠溶液滴定待测的白醋时,眼睛应该注视。(4)、该滴定实验达到终点时的现象是。(5)、用标准溶液滴定上述稀释后的醋酸溶液,滴定结果如表所示:
(1)、选用(填“甲”或“乙”)滴定管量取白醋后,滴定管读数如丙图所示,此时液面显示读数为 , 将其稀释至备用。(2)、为尽可能的减少实验误差,应该选(填“酚酞”、“甲基橙”或“石蕊”)作指示剂。(3)、用标准氢氧化钠溶液滴定待测的白醋时,眼睛应该注视。(4)、该滴定实验达到终点时的现象是。(5)、用标准溶液滴定上述稀释后的醋酸溶液,滴定结果如表所示:滴定次数
待测溶液的体积
标准溶液的体积
滴定前刻度
滴定后刻度
1
0.02
25.01
2
0.70
25.71
3
0.50
24.20
则该品牌白醋中醋酸含量为。
(6)、下列操作中,可能使所测白醋中醋酸的浓度数值偏高的是______(填字母,下同)。A、读取溶液体积时,开始时仰视读数,滴定结束时俯视读数 B、取待测液的滴管,取液前滴定管尖嘴处无气泡,取液后尖嘴处出现气泡 C、碱式滴定管未用标准溶液润洗就直接注入标准溶液 D、滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥 -
16、乙醇-水催化重整可获得 , 其主要反应为:
反应①
反应②
在、 , 若仅考虑上述反应,平衡时和的选择性及的产率随温度的变化如图所示。
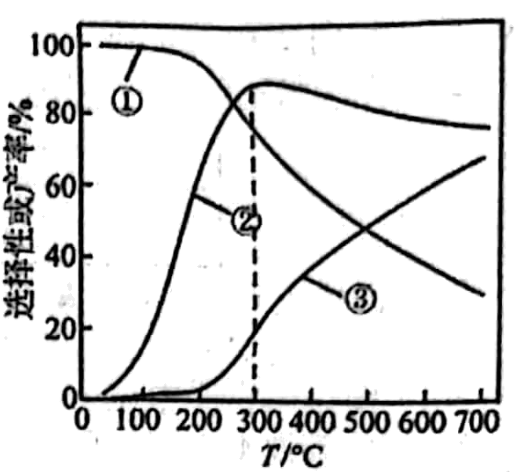
的选择性
下列说法不正确的是
A、反应的 B、图中曲线①表示平衡时选择性随温度的变化 C、一定温度下,增大可提高的平衡转化率 D、由图可知,后升高温度曲线②呈下降趋势,说明温度对反应②速率的影响比对反应①的大 -
17、燃煤烟气脱硫的方法有多种,方法之一是常温下用氨水将转化为 , 再氧化成。已知的电离常数 , , 的电离常数。下列说法正确的是A、常温下溶液的 B、溶液中: C、若溶液中时,溶液的 D、向溶液中通入空气发生反应的离子方程式:
-
18、常温下,根据下列实验操作和现象所得到的结论正确的是
选项
实验操作和现象
结论
A
用试纸测得等浓度的溶液的约为9,溶液的约为8
酸性强弱:
B
相同条件下,分别测量和醋酸溶液的导电性,前者的导电性强
醋酸浓度越大,电离程度越大
C
将充满的密闭玻璃球浸泡在热水中,气体红棕色加深
D
向溶有的溶液中通入气体 , 出现白色沉淀
气体一定具有强氧化性
A、A B、B C、C D、D -
19、常温下,向溶液中缓慢加入固体(溶液体积不变),溶液中、、的物质的量分数随的变化如图所示。下列说法不正确的是
 A、 B、点到点发生的主要离子反应: C、点溶液中离子的物质的量浓度大小关系为 D、b点溶液中
A、 B、点到点发生的主要离子反应: C、点溶液中离子的物质的量浓度大小关系为 D、b点溶液中 -
20、探究反应的速率影响因素,设计了以下实验,下列说法正确的是
锥形瓶号
1
2
3
4
反应温度/℃
20
20
40
40
溶液/mL
10
10
10
10
溶液/mL
10
5
10
4
0
x
0
6
浑浊出现时间/s
10
16
5
8
A、该反应也可以通过单位时间内浓度的变化来表示化学反应速率的快慢 B、2号瓶中x为5 C、3号瓶第反应结束,用来表示前内平均反应速率为 D、由1号瓶和4号瓶实验结果可得温度越高反应速率越快