备考2026届高考 2021-2025全国各地真题汇编 专题10 弱电解质的电离平衡和溶液的酸碱性
试卷更新日期:2026-04-25 类型:二轮复习
一、选择题
-
1. 在浓度为0.1mol/L的NaH2PO4溶液中,如下说法正确的是( )A、溶液中浓度最大的离子是H2 B、c(H3PO4)+c(H2)+c()+c()=0.1mol/L C、c(Na+)+c(H+)=c(H2)+2c()+3c() D、磷酸第二步电离平衡的平衡常数表达式为K=2. 甲胺水溶液中存在以下平衡:。已知:时,的 , 的。下列说法错误的是A、的 B、溶液中存在 C、时,溶液与溶液相比,溶液中的小 D、溶液与相同浓度的溶液以任意比例混合,混合液中存在3. 常温下、将等体积、浓度均为0.40mol•L﹣1BaCl2溶液与新制H2SO3溶液混合,出现白色浑浊;再滴加过量的H2O2溶液,振荡,出现白色沉淀。
已知:H2SO3 Ka1=1.4×10﹣2 , Ka2=6.0×10﹣8。Ksp(BaSO3)=5.0×10﹣10 , Ksp(BaSO4)=1.1×10﹣10。
下列说法不正确的是( )
A、H2SO3溶液中存在c(H+)>c()>c()>c(OH﹣) B、将0.40mol•L﹣1H2SO3溶液稀释到0.20mol•L﹣1 , c()几乎不变 C、BaCl2溶液与H2SO3溶液混合后出现的白色浑浊不含有BaSO3 D、存在反应Ba2++H2SO3+H2O2═BaSO4↓+2H++H2O是出现白色沉淀的主要原因4. 25℃下,水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是( )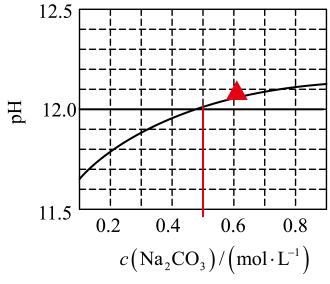 A、时,溶液中 B、水解程度随其浓度增大而减小 C、在水中的 D、的溶液和的溶液等体积混合,得到的溶液5. 下表列出25℃时不同羧酸的pKa(即﹣lgKa)。根据表中的数据推测,结论正确的是( )
A、时,溶液中 B、水解程度随其浓度增大而减小 C、在水中的 D、的溶液和的溶液等体积混合,得到的溶液5. 下表列出25℃时不同羧酸的pKa(即﹣lgKa)。根据表中的数据推测,结论正确的是( )羧酸
CH3COOH
CH2FCOOH
CH2ClCOOH
CH2BrCOOH
pKa
4.76
2.59
2.87
2.90
A、酸性强弱:CH2ICOOH>CH2BrCOOH B、对键合电子的吸引能力强弱:F<Cl<Br C、25℃时的pKa大小:CHF2COOH<CH2FCOOH D、25℃时0.1mol/L溶液的碱性强弱:CH3COONa>CH2ClCOONa6. 常温下,一元酸的。在某体系中,与离子不能穿过隔膜,未电离的可自由穿过该膜(如图所示)。
设溶液中 , 当达到平衡时,下列叙述正确的是( )
A、溶液Ⅰ中 B、溶液Ⅱ中的的电离度为 C、溶液Ⅰ和Ⅱ中的不相等 D、溶液Ⅰ和Ⅱ中的之比为7. 苹果酸是二元弱酸,以H2A表示,常用于制造药物、糖果等。25℃时,溶液中H2A、HA-和A2-的分布系数随溶液pH变化如图。例如:A2-的分布系数
该温度下,下列说法错误的是( )
 A、曲线①是H2A的分布系数曲线 B、H2A的 C、反应的平衡常数 D、pH=6时,溶液中粒子浓度的大小关系为8. 常温下,下列有关电解质溶液的叙述正确的是( )A、在 溶液中 B、在 溶液中 C、在 溶液中 D、氨水和NH4Cl溶液混合,形成pH=9的溶液中9. 25℃时,下列说法正确的是( )A、NaHA溶液呈酸性,可以推测H2A为强酸 B、可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐 C、0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α1、α2 , 则α1<α2 D、100 mL pH=10.00的Na2CO3溶液中水电离出H+的物质的量为1.0×10-5mol10. 0.1mol•L﹣1NaOH分别滴入20mL0.1mol•L﹣1HX与20mL0.1mol•L﹣1HCl溶液中,其pH随滴入NaOH溶液体积变化的图像如图所示,下列说法正确的是( )
A、曲线①是H2A的分布系数曲线 B、H2A的 C、反应的平衡常数 D、pH=6时,溶液中粒子浓度的大小关系为8. 常温下,下列有关电解质溶液的叙述正确的是( )A、在 溶液中 B、在 溶液中 C、在 溶液中 D、氨水和NH4Cl溶液混合,形成pH=9的溶液中9. 25℃时,下列说法正确的是( )A、NaHA溶液呈酸性,可以推测H2A为强酸 B、可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐 C、0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α1、α2 , 则α1<α2 D、100 mL pH=10.00的Na2CO3溶液中水电离出H+的物质的量为1.0×10-5mol10. 0.1mol•L﹣1NaOH分别滴入20mL0.1mol•L﹣1HX与20mL0.1mol•L﹣1HCl溶液中,其pH随滴入NaOH溶液体积变化的图像如图所示,下列说法正确的是( ) A、b点:c(X﹣)•c(OH﹣)=10﹣12mol2•L2 B、c点:c(X﹣)﹣c(HX)=c(OH﹣)﹣c(H+) C、a、d点溶液混合后为酸性 D、水的电离程度:d>c>b>a11. 实验室用基准配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定标准溶液。下列说法错误的是( )A、可用量筒量取标准溶液置于锥形瓶中 B、应选用配带塑料塞的容量瓶配制标准溶液 C、应选用烧杯而非称量纸称量固体 D、达到滴定终点时溶液显橙色12. 某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列说法正确的是( )A、25℃时,若测得 溶液 ,则HR是弱酸 B、25℃时,若测得 溶液 且 ,则HR是弱酸 C、25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,则HR是弱酸 D、25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱酸13. 用硫酸和NaN3可制备一元弱酸HN3。下列说法错误的是( )A、NaN3的水溶液显碱性 B、N3-的空间构型为V形 C、NaN3为含有共价键的离子化合物 D、N3-的中心N原子所有价电子均参与成键14. 草酸广泛应用于食品、药品等领域。常温下,通过下列实验探究了草酸的性质:
A、b点:c(X﹣)•c(OH﹣)=10﹣12mol2•L2 B、c点:c(X﹣)﹣c(HX)=c(OH﹣)﹣c(H+) C、a、d点溶液混合后为酸性 D、水的电离程度:d>c>b>a11. 实验室用基准配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定标准溶液。下列说法错误的是( )A、可用量筒量取标准溶液置于锥形瓶中 B、应选用配带塑料塞的容量瓶配制标准溶液 C、应选用烧杯而非称量纸称量固体 D、达到滴定终点时溶液显橙色12. 某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列说法正确的是( )A、25℃时,若测得 溶液 ,则HR是弱酸 B、25℃时,若测得 溶液 且 ,则HR是弱酸 C、25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,则HR是弱酸 D、25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱酸13. 用硫酸和NaN3可制备一元弱酸HN3。下列说法错误的是( )A、NaN3的水溶液显碱性 B、N3-的空间构型为V形 C、NaN3为含有共价键的离子化合物 D、N3-的中心N原子所有价电子均参与成键14. 草酸广泛应用于食品、药品等领域。常温下,通过下列实验探究了草酸的性质:实验1:向溶液中滴入一定量溶液。混合溶液的与的关系如图所示。
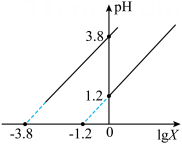
实验2:向溶液中加入溶液。
已知:时,。混合后溶液体积变化忽略不计。
下列说法错误的是( )
A、实验1,当溶液中时, B、实验1,当溶液呈中性时: C、实验2,溶液中有沉淀生成 D、实验2,溶液中存在:15. 时,的电离常数。下列描述不正确的是A、 B、 C、 D、溶液中, , 则16. 常温下,用溶液分别滴定下列两种混合溶液:Ⅰ.20.00mL浓度均为和溶液
Ⅱ.20.00mL浓度均为和溶液
两种混合溶液的滴定曲线如图。已知 , 下列说法正确的是
 A、Ⅰ对应的滴定曲线为N线 B、点水电离出的数量级为 C、时,Ⅱ中 D、时,Ⅰ中之和小于Ⅱ中之和
A、Ⅰ对应的滴定曲线为N线 B、点水电离出的数量级为 C、时,Ⅱ中 D、时,Ⅰ中之和小于Ⅱ中之和二、实验探究题
-
17. 铬及其化合物在催化、金属防腐等方面具有重要应用。(1)、催化剂 可由 加热分解制备,反应同时生成无污染气体。
①完成化学方程式: 。
② 催化丙烷脱氢过程中,部分反应历程如图1, 过程的焓变为(列式表示)。

③ 可用于 的催化氧化。设计从 出发经过3步反应制备 的路线(用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为。
(2)、 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:(ⅰ)
(ⅱ)
①下列有关 溶液的说法正确的有。
A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量 溶液,反应(ⅰ)的平衡逆向移动
D.加入少量 固体,平衡时 与 的比值保持不变
② 时, 溶液中 随pH的变化关系如图2。当 时,设 、 与 的平衡浓度分别为x、y、z ,则x、y、z之间的关系式为 ;计算溶液中 的平衡浓度(写出计算过程,结果保留两位有效数字)。

③在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长( )有关;在一定波长范围内,最大A对应的波长( )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收程度之和。为研究pH对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、 不同的 稀溶液,测得其A随 的变化曲线如图3。波长 、 和 中,与 的 最接近的是;溶液 从a变到b的过程中, 的值(填“增大”“减小”或“不变”)。
18. 食醋是烹饪美食的调味品,有效成分主要为醋酸(用 表示)。 的应用与其电离平衡密切相关。25℃时, 的 。(1)、配制 的 溶液,需 溶液的体积为mL。(2)、下列关于250mL容量瓶的操作,正确的是。 (3)、某小组研究25℃下 电离平衡的影响因素。
(3)、某小组研究25℃下 电离平衡的影响因素。提出假设 稀释 溶液或改变 浓度, 电离平衡会发生移动。
设计方案并完成实验 用浓度均为 的 和 溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
序号
Ⅰ
40.00
/
/
0
2.86
Ⅱ
4.00
/
36.00
0
3.36
…
Ⅶ
4.00
a
b
3∶4
4.53
Ⅷ
4.00
4.00
32.00
1∶1
4.65
①根据表中信息,补充数据: , 。
②由实验Ⅰ和Ⅱ可知,稀释 溶液,电离平衡(填”正”或”逆”)向移动;结合表中数据,给出判断理由:。
③由实验Ⅱ~VIII可知,增大 浓度, 电离平衡逆向移动。
实验结论 假设成立。
(4)、小组分析上表数据发现:随着 的增加, 的值逐渐接近 的 。查阅资料获悉:一定条件下,按 配制的溶液中, 的值等于 的 。
对比数据发现,实验VIII中 与资料数据 存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定 溶液的浓度再验证。
(ⅰ)移取 溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为 ,则该 溶液的浓度为 。在答题卡虚线框中,画出上述过程的滴定曲线示意图并标注滴定终点。
(ⅱ)用上述 溶液和 溶液,配制等物质的量的 与
 混合溶液,测定pH,结果与资料数据相符。(5)、小组进一步提出:如果只有浓度均约为 的 和 溶液,如何准确测定 的 ?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
混合溶液,测定pH,结果与资料数据相符。(5)、小组进一步提出:如果只有浓度均约为 的 和 溶液,如何准确测定 的 ?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。Ⅰ
移取 溶液,用 溶液滴定至终点,消耗 溶液
Ⅱ
, 测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
(6)、根据 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途。19. 酸及盐在生活生产中应用广泛。(1)、甲苯氧化可生成苯甲酸。向盛有2mL甲苯的试管中,加入几滴酸性溶液,振荡,观察到体系颜色。(2)、某苯甲酸粗品含少量泥沙和氯化钠。用重结晶法提纯该粗品过程中,需要的操作及其顺序为:加热溶解、(填下列操作编号)。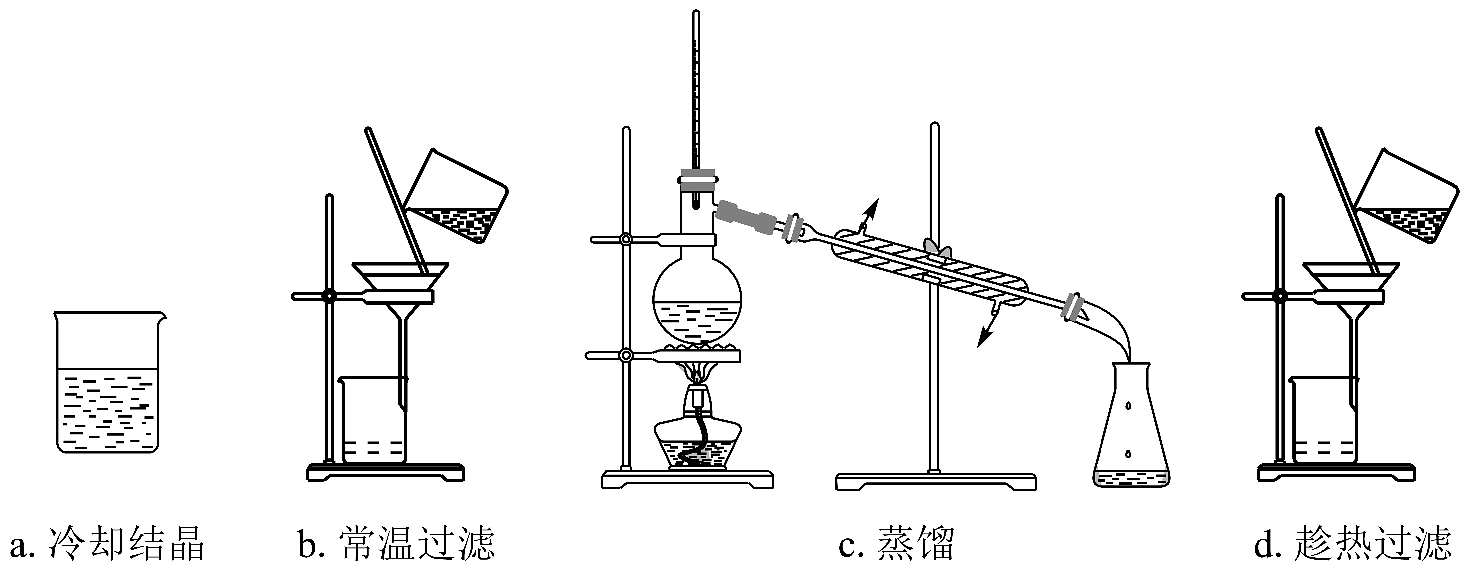 (3)、兴趣小组测定常温下苯甲酸饱和溶液的浓度和苯甲酸的 , 实验如下:取50.00mL苯甲酸饱和溶液,用溶液滴定,用pH计测得体系的pH随滴入溶液体积V变化的曲线如图。据图可得:
(3)、兴趣小组测定常温下苯甲酸饱和溶液的浓度和苯甲酸的 , 实验如下:取50.00mL苯甲酸饱和溶液,用溶液滴定,用pH计测得体系的pH随滴入溶液体积V变化的曲线如图。据图可得:
①。
②苯甲酸的(列出算式,水的电离可忽略)。
(4)、该小组继续探究取代基对芳香酸酸性的影响。①知识回顾 羧酸酸性可用衡量。下列羧酸的变化顺序为:。随着卤原子电负性 , 羧基中的羟基增大,酸性增强。
②提出假设 甲同学根据①中规律推测下列芳香酸的酸性强弱顺序为:

③验证假设 甲同学测得常温下三种酸的饱和溶液的pH大小顺序为Ⅲ>Ⅱ>Ⅰ,据此推断假设成立。但乙同学认为该推断依据不足,不能用所测得的pH直接判断大小顺序,因为。
乙同学用(3)中方法测定了上述三种酸的 , 其顺序为Ⅱ>Ⅰ>Ⅲ。
④实验小结 假设不成立,芳香环上取代基效应较复杂,①中规律不可随意推广。
(5)、该小组尝试测弱酸HClO的。①丙同学认为不宜按照(3)中方法进行实验,其原因之一是次氯酸易分解。该分解反应的离子方程式为。
②小组讨论后,选用0.100mol/LNaClO溶液(含少量NaCl)进行实验,以获得HClO的。简述该方案(包括所用仪器及数据处理思路)。
③教师指导:设计实验方案时,需要根据物质性质,具体问题具体分析。
三、综合题
-
20. 二甲胺[(CH3)2NH]、N,N-二甲基甲酰胺[HCON(CH3)2]均是用途广泛的化工原料。请回答:(1)、用氨和甲醇在闭容器中合成二甲胺,反应方程式如下:
Ⅰ.
Ⅱ.
Ⅲ.
可改变甲醇平衡转化率的因素是_______。
A、温度 B、投料比[n(NH3):n(CH3OH)] C、压强 D、催化剂(2)、25℃下,(CH3)2NH·H2O的电离常数为Kb,-lgKb=3.2,则1mol/L[(CH3)2NH2] +Cl-水溶液的pH=。(3)、在[(CH3)2NH2] +Cl-的有机溶液中电化学还原CO2制备HCON(CH3)2阴极上生成HCON(CH3)2的电极反应方程式是。(4)、上述电化学方法产率不高,工业中常用如下反应生产HCON(CH3)2:。某条件下反应自发且熵减,则反应在该条件下0(填“>”、“<”或“=”)。(5)、有研究采用CO2、H2和(CH3)2NH催化反应制备HCON(CH3)2。在恒温密闭容器中,投料比 , 催化剂M足量。反应方程式如下:Ⅳ.
V.
三种物质的物质的量百分比随反应时间变化如图所示。
(例:HCOOH的物质的量百分比

①请解释HCOOH的物质的量百分比随反应时间变化的原因(不考虑催化剂M活性降低或失活)。
②若用SiH4代替H2作为氢源与CO2反应生成HCOOH,可以降低反应所需温度。请从化学键角度解释原因。
21. 天津地处环渤海湾,海水资源丰富。科研人员把铁的配合物(L为配体)溶于弱碱性的海水中,制成吸收液,将气体转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:①的吸收氧化;②的再生。反应原理如下:①
②
回答下列问题:
(1)、该工艺的总反应方程式为。1mol 发生该反应的热量变化为 , 在总反应中的作用是。(2)、研究不同配体与所形成的配合物(A、B、C)对吸收转化率的影响。将配合物A、B、C分别溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向三份吸收液持续通入 , 测得单位体积吸收液中吸收转化率随时间变化的曲线如图1所示。以由100%降至80%所持续的时间来评价铁配合物的脱硫效率,结果最好的是(填“A”、“B”或“C”)。 (3)、的电离方程式为。25℃时,溶液中、、在含硫粒子总浓度中所占分数随溶液pH的变化关系如图2,由图2计算,的 , 。再生反应在常温下进行,解离出的易与溶液中的形成沉淀。若溶液中的 , , 为避免有FeS沉淀生成,应控制溶液pH不大于(已知25℃时,FeS的为)。
(3)、的电离方程式为。25℃时,溶液中、、在含硫粒子总浓度中所占分数随溶液pH的变化关系如图2,由图2计算,的 , 。再生反应在常温下进行,解离出的易与溶液中的形成沉淀。若溶液中的 , , 为避免有FeS沉淀生成,应控制溶液pH不大于(已知25℃时,FeS的为)。 22. 磷是生命活动中不可或缺的元素。请回答:(1)、关于ⅤA族元素原子结构的描述,下列说法正确的是_______。A、基态P原子轨道上的电子自旋方向相同 B、的最外层电子数为18 C、的半径小于的半径 D、电子排布为的P原子处于激发态(2)、某化合物的晶胞如图。
22. 磷是生命活动中不可或缺的元素。请回答:(1)、关于ⅤA族元素原子结构的描述,下列说法正确的是_______。A、基态P原子轨道上的电子自旋方向相同 B、的最外层电子数为18 C、的半径小于的半径 D、电子排布为的P原子处于激发态(2)、某化合物的晶胞如图。
①化学式是;
②将该化合物加入到含少量石蕊的中,实验现象是(从酸碱性和溶解性角度推测)。
(3)、两分子脱水聚合得到一分子 , 从的结构角度分析差异的原因。(4)、兴趣小组对某磷灰石[主要成分为和少量]进行探究,设计了两种制备的方法:Ⅰ.用稍过量的浓与磷灰石反应,得到溶液、少量气体、渣(主要成分为)。
Ⅱ.将磷灰石脱水、还原,得到的白磷燃烧后与水反应制得溶液。
①方法I,所得溶液中含有的杂质酸是。
②以方法Ⅰ中所得渣为硫源,设计实验制备无水 , 流程如下:

溶液A是 , 系列操作B是 , 操作C是。
③方法Ⅱ中,脱水得到的(足量)与炭(C)、高温下反应,生成白磷和另一种可燃性气体,该反应的化学方程式是。
四、流程题
-
23. 实验室模拟“镁法工业烟气脱硫”并制备 , 其实验过程可表示为
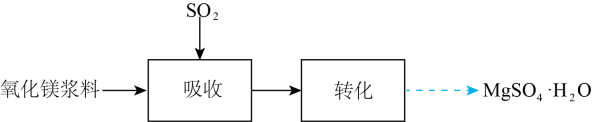 (1)、在搅拌下向氧化镁浆料中匀速缓慢通入气体,生成 , 反应为 , 其平衡常数K与、、、的代数关系式为;下列实验操作一定能提高氧化镁浆料吸收效率的有(填序号)。
(1)、在搅拌下向氧化镁浆料中匀速缓慢通入气体,生成 , 反应为 , 其平衡常数K与、、、的代数关系式为;下列实验操作一定能提高氧化镁浆料吸收效率的有(填序号)。A.水浴加热氧化镁浆料
B.加快搅拌速率
C.降低通入气体的速率
D.通过多孔球泡向氧化镁浆料中通
(2)、在催化剂作用下被氧化为。已知的溶解度为0.57g(20℃),氧化溶液中的离子方程式为;在其他条件相同时,以负载钴的分子筛为催化剂,浆料中被氧化的速率随pH的变化如题图甲所示。在pH=6~8范围内,pH增大,浆料中的氧化速率增大,其主要原因是。 (3)、制取晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的浆料与溶液充分反应。浆料与溶液的加料方式是;补充完整制取晶体的实验方案:向含有少量、的溶液中,。(已知:、在时完全转化为氢氧化物沉淀;室温下从饱和溶液中结晶出 , 在150~170℃下干燥得到 , 实验中需要使用MgO粉末)
(3)、制取晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的浆料与溶液充分反应。浆料与溶液的加料方式是;补充完整制取晶体的实验方案:向含有少量、的溶液中,。(已知:、在时完全转化为氢氧化物沉淀;室温下从饱和溶液中结晶出 , 在150~170℃下干燥得到 , 实验中需要使用MgO粉末)