备考2026届高考 2021-2025全国各地真题汇编 专题5 原子结构元素周期律
试卷更新日期:2026-04-25 类型:二轮复习
一、选择题
-
1. 根据元素周期律推测,下列说法不正确的是( )A、原子半径:Mg>Na B、电负性:C> Si C、非金属性:Br>I D、热稳定性:NH3>PH32. 下列化学用语表示不正确的是( )A、CH4的结构式:
 B、基态氧原子的轨道表示式
B、基态氧原子的轨道表示式 C、p 电子云轮廓图:
C、p 电子云轮廓图: D、CH3CH(CH2CH3)CH2CH3的系统命名:2-乙基丁烷
3. 科学家通过核反应。发现氚。下列说法正确的是( )A、表示一个质子 B、的基态原子核外电子排布式为 C、与互为同位素 D、的原子结构示意图为
D、CH3CH(CH2CH3)CH2CH3的系统命名:2-乙基丁烷
3. 科学家通过核反应。发现氚。下列说法正确的是( )A、表示一个质子 B、的基态原子核外电子排布式为 C、与互为同位素 D、的原子结构示意图为 4. 我国探月工程取得重大进展.月壤中含有Ca、Fe等元素的磷酸盐,下列元素位于元素周期表第二周期的是( )A、O B、P C、Ca D、Fe5. 依据下列实验操作及现象,不能得出相应结论的是( )
4. 我国探月工程取得重大进展.月壤中含有Ca、Fe等元素的磷酸盐,下列元素位于元素周期表第二周期的是( )A、O B、P C、Ca D、Fe5. 依据下列实验操作及现象,不能得出相应结论的是( )实验操作及现象
结论
A
将稀盐酸滴入NaHCO3溶液中,产生的气体通入澄清的石灰水,石灰水变浑浊
非金属性:Cl>C
B
硫化锌(ZnS,白色)、硫化镉(CdS,黄色)为难溶电解质。向浓度均为0.1 mol/L的Zn2+、Cd2+混合液中,滴加Na2S稀溶液,先出现的沉淀是黄色的
C
向可能含有Fe2+的未知溶液中,滴加1滴溶液,有特征蓝色沉淀生成
原未知溶液中含有Fe2+
D
向含有新制的氢氧化铜的碱性溶液中,加入乙醛溶液并加热,出现砖红色沉淀
乙醛具有还原性
A、A B、B C、C D、D6. 长周期原子序数依次增大的主族元素X、Y、Z三种元素,X的价层电子数为4,Y有1个未成对电子,Z+的最高能级4p轨道填满,则下列说法正确的是( )A、X、Y、Z属于同一周期元素 B、氧化物对应水化物碱性最强的是X C、单质熔点最高的是Y D、原子半径是最大的是Z7. 根据元素周期律,同时满足条件(ⅰ)和条件(ⅱ)的元素是( )(ⅰ)电负性是同主族元素中最大:
(ⅱ)第一电离能比同周期相邻主族元素大的。
A、Al B、Si C、B D、Be8. 元素a~i为短周期元素,其第一电离能与原子序数的关系如图。下列说法正确的是 A、a和g同主族 B、金属性: C、原子半径: D、最简单氢化物沸点:9. 钙霞石是一种生产玻璃陶瓷的原料,所含M、Q、R、T、X、Y、Z为原子序数依次增大的前20号主族元素,M是原子半径最小的元素,Q是形成物质种类最多的元素,R是地壳中含量最高的元素,T、X、Y同周期,Q、X均与Y相邻,Z的原子序数等于M、R和T的原子序数之和。下列说法正确的是( )A、M与Z可形成离子化合物 B、原子半径: C、是极性分子 D、电负性:10. 一种高聚物被称为“无机橡胶”,可由如图所示的环状三聚体制备。X、Y和Z都是短周期元素,X、Y价电子致相等,X、Z电子层数相同,基态Y的轨道半充满,Z的最外层只有1个未成对电子,下列说法正确的是( )
A、a和g同主族 B、金属性: C、原子半径: D、最简单氢化物沸点:9. 钙霞石是一种生产玻璃陶瓷的原料,所含M、Q、R、T、X、Y、Z为原子序数依次增大的前20号主族元素,M是原子半径最小的元素,Q是形成物质种类最多的元素,R是地壳中含量最高的元素,T、X、Y同周期,Q、X均与Y相邻,Z的原子序数等于M、R和T的原子序数之和。下列说法正确的是( )A、M与Z可形成离子化合物 B、原子半径: C、是极性分子 D、电负性:10. 一种高聚物被称为“无机橡胶”,可由如图所示的环状三聚体制备。X、Y和Z都是短周期元素,X、Y价电子致相等,X、Z电子层数相同,基态Y的轨道半充满,Z的最外层只有1个未成对电子,下列说法正确的是( ) A、X、Z的第一电离能: B、X、Y的简单氢化物的键角: C、最高价含氧酸的酸性: D、X、Y、Z均能形成多种氧化物11. 可用于水的杀菌消毒,遇水发生反应:。下列说法正确的是( )A、反应中各分子的键均为键 B、反应中各分子的VSEPR模型均为四面体形 C、键长小于H—O键长 D、HClO分子中Cl的价电子层有2个孤电子对12. 由O、F、I组成化学式为的化合物,能体现其成键结构的片段如图所示。下列说法正确的是
A、X、Z的第一电离能: B、X、Y的简单氢化物的键角: C、最高价含氧酸的酸性: D、X、Y、Z均能形成多种氧化物11. 可用于水的杀菌消毒,遇水发生反应:。下列说法正确的是( )A、反应中各分子的键均为键 B、反应中各分子的VSEPR模型均为四面体形 C、键长小于H—O键长 D、HClO分子中Cl的价电子层有2个孤电子对12. 由O、F、I组成化学式为的化合物,能体现其成键结构的片段如图所示。下列说法正确的是 A、图中O代表F原子 B、该化合物中存在过氧键 C、该化合物中I原子存在孤对电子 D、该化合物中所有碘氧键键长相等
A、图中O代表F原子 B、该化合物中存在过氧键 C、该化合物中I原子存在孤对电子 D、该化合物中所有碘氧键键长相等二、填空题
-
13. 氧是构建化合物的重要元素。请回答:(1)、某化合物的晶胞如图1,Cl−的配位数(紧邻的阳离子数)为;写出该化合物的化学式 , 写出该化合物与足量NH4Cl溶液反应的化学方程式。





HA
HB
HC
HD
图1
图2
(2)、下列有关单核微粒的描述正确的是____。A、Ar的基态原子电子排布方式只有一种 B、Na的第二电离能>Ne的第一电离能 C、Ge的基态原子简化电子排布式为[Ar]4s24p2 D、Fe原子变成Fe+ , 优先失去3d轨道上的电子(3)、化合物HA、HB、HC和HD的结构如图2。①HA、HB和HC中羟基与水均可形成氢键(-O-H┄OH2),按照氢键由强到弱对三种酸排序 , 请说明理由。
②已知HC、HD钠盐的碱性NaC>NaD,请从结构角度说明理由。
14. 下表列出了七种元素(用字母表示)在元素周期表中的位置。回答下列问题:周期
族
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
2
X
R
3
M
Y
Z
Q
W
(1)、写出X的原子结构示意图: , 原子半径:XR(填“大于”或“小于”)(2)、Q和W的最高价氧化物对应的水化物的酸性:>(填化学式)。(3)、化合物MW的电子式为 , 其中含有的化学键类型是。(4)、实验室提供了下列试剂:溶液、溶液、氨水、溶液。请设计实验方案证明碱性:。15. 锡()是现代“五金”之一,广泛应用于合金、半导体工业等。(1)、位于元素周期表的第5周期第IVA族。将的基态原子最外层轨道表示式补充完整: (2)、和是锡的常见氯化物,可被氧化得到。
(2)、和是锡的常见氯化物,可被氧化得到。
①分子的模型名称是。
②的键是由锡的轨道与氯的轨道重叠形成。键。
(3)、白锡和灰锡是单质的常见同素异形体。二者晶胞如图:白锡具有体心四方结构;灰锡具有立方金刚石结构。
①灰锡中每个原子周围与它最近且距离相等的原子有个。
②若白锡和灰锡的晶胞体积分别为和 , 则白锡和灰锡晶体的密度之比是。
(4)、单质的制备:将与焦炭充分混合后,于惰性气氛中加热至 , 由于固体之间反应慢,未明显发生反应。若通入空气在下,能迅速被还原为单质 , 通入空气的作用是。三、流程题
-
16. 铜阳极泥(含有Au、、、等)是一种含贵金属的可再生资源,回收贵金属的化工流程如下:

已知:①当某离子的浓度低于时,可忽略该离子的存在;
② ;
③易从溶液中结晶析出;
④不同温度下的溶解度如下:
温度℃
0
20
40
60
80
溶解度/g
14.4
26.1
37.4
33.2
29.0
回答下列问题:
(1)、Cu属于区元素,其基态原子的价电子排布式为;(2)、“滤液1”中含有和 , “氧化酸浸”时反应的离子方程式为;(3)、“氧化酸浸”和“除金”工序抣需加入一定量的:①在“氧化酸浸”工序中,加入适量的原因是。
②在“除金”工序溶液中,浓度不能超过。
(4)、在“银转化”体系中,和浓度之和为 , 两种离子分布分数随浓度的变化关系如图所示,若浓度为 , 则的浓度为。 (5)、滤液4中溶质主要成分为(填化学式);在连续生产的模式下,“银转化”和“银还原”工序需在℃左右进行,若反应温度过高,将难以实现连续生产,原因是。17. 工业上利用如下流程将粗硒进行精制,结合流程,回答下列问题
(5)、滤液4中溶质主要成分为(填化学式);在连续生产的模式下,“银转化”和“银还原”工序需在℃左右进行,若反应温度过高,将难以实现连续生产,原因是。17. 工业上利用如下流程将粗硒进行精制,结合流程,回答下列问题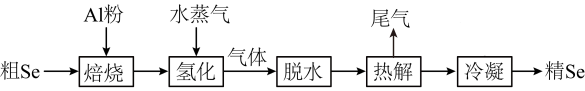 (1)、Ⅰ.焙烧产物为 , 其中Se的化合价为 , 铝的基态电子排布式为。(2)、“氢化”过程涉及到的化学方程式为。(3)、已知热解方程式为: , 回答下列问题:热解后,温度迅速从1000K降至500K,对于Se蒸汽而言,从气态变为固态的过程为。热解后迅速降温的目的。尾气的成分为(填化学式)。(4)、Ⅱ.取0.1g样品,加入 , 生成 , 向其中加入0.1mol/L的和少量的淀粉KI溶液,用去40.00mL的溶液,反应完成后,再加: (),至蓝色消失,通过反应②Se(IV)与反应的物质的量之比为。
(1)、Ⅰ.焙烧产物为 , 其中Se的化合价为 , 铝的基态电子排布式为。(2)、“氢化”过程涉及到的化学方程式为。(3)、已知热解方程式为: , 回答下列问题:热解后,温度迅速从1000K降至500K,对于Se蒸汽而言,从气态变为固态的过程为。热解后迅速降温的目的。尾气的成分为(填化学式)。(4)、Ⅱ.取0.1g样品,加入 , 生成 , 向其中加入0.1mol/L的和少量的淀粉KI溶液,用去40.00mL的溶液,反应完成后,再加: (),至蓝色消失,通过反应②Se(IV)与反应的物质的量之比为。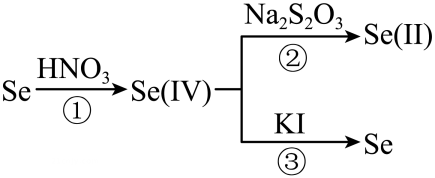
反应③的离子方程式为。
(5)、样品中Se的含量。四、综合题
-
18. 硫是一种重要的非金属元素。(1)、基态S原子的价层电子的轨道表示式为。H2S的VSEPR模型名称为 , 其空间结构为。(2)、H2O、H2S、H2Se的沸点由高到低的顺序为。(3)、NH4HS的电子式为。在25℃和101 kPa下,NH3与H2S两种气体反应生成1 mol NH4HS固体时,放出90.4 kJ的热量,该反应的热化学方程式为。(4)、25℃时,H2S的Ka1和Ka2分别为1.1×10-7、1.3×10-13 , NH3·H2O的Kb为1.8×10-5 , 则NH4HS水溶液显(填“酸性”“中性”“碱性”)。(5)、硫化锂晶体的晶胞如右图,晶胞中含有硫离子的数目为;与硫离子最近且距离相等的锂离子的数目为。
 (6)、将1.0 g硫粉和2.0 g铁粉均匀混合,放在陶土网上堆成条状。用灼热的玻璃棒触及混合粉末的一端引发反应,反应剧烈。实验中可能发生的反应为(用化学方程式表示)。19.
(6)、将1.0 g硫粉和2.0 g铁粉均匀混合,放在陶土网上堆成条状。用灼热的玻璃棒触及混合粉末的一端引发反应,反应剧烈。实验中可能发生的反应为(用化学方程式表示)。19.(以下题目中的图片根据回忆所得信息结合文献资料重新整合所得,仅供参考)
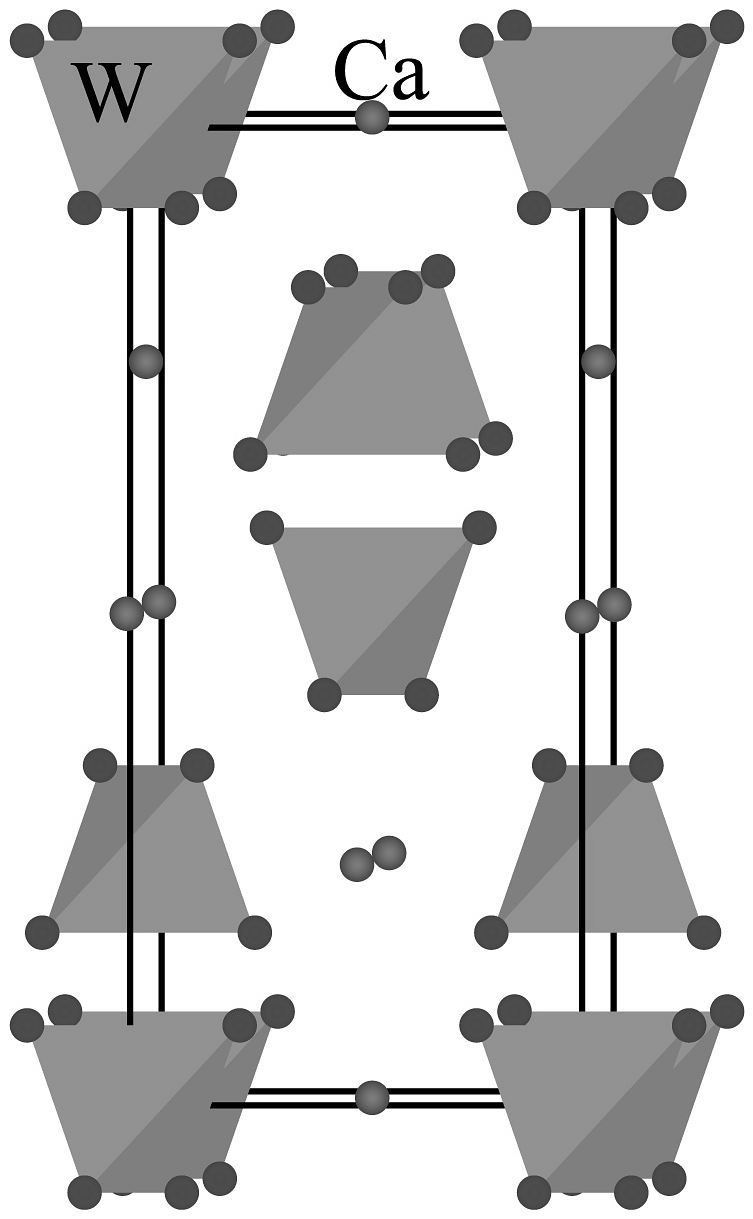
(1)钨作灯丝与_______性质有关(不定项)。
A.延展性 B导电性 C.高熔点 D.高密度
(2)钨有金属光泽的原因________ (从微观角度解释)。(3)原子在晶胞中的_______位置。
A. 顶点 B. 棱上 C. 面上 D. 体心 (4)钨在周期表中的位置是_______。

A. 第五周期第ⅡB族 B. 第五周期第ⅣB族 C. 第六周期第ⅡB族 D. 第六周期第ⅥB族 (5)根据价层电子对斥理论,的价层电子对数是________。
(6)图晶胞号O原子,若晶胞仅含1个完整四面体,组成该四面体的O编号是________。
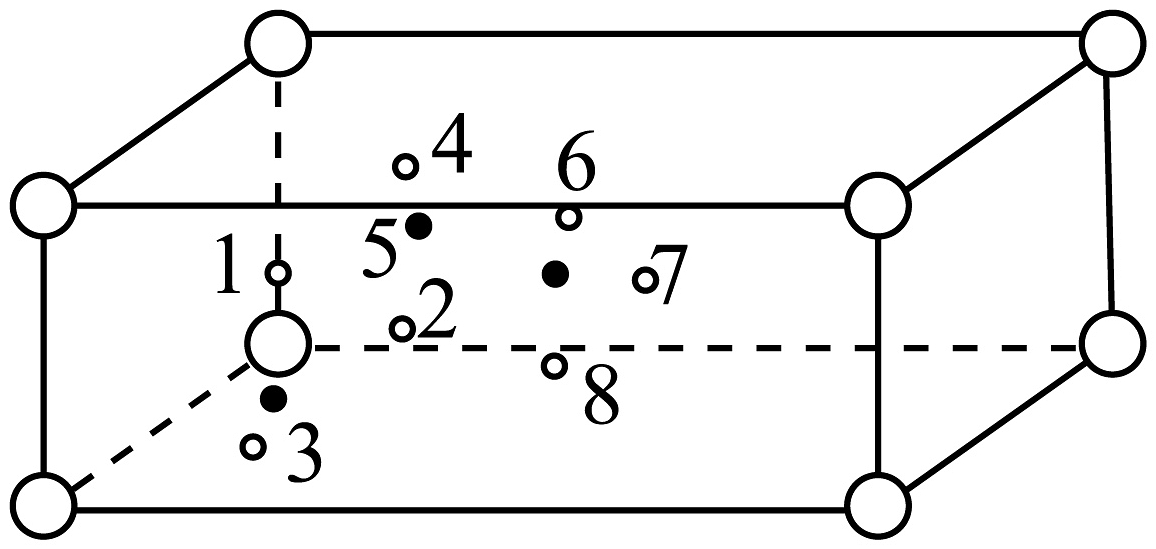
表格(各种矿石密度)。

(7)给出晶胞参数,求并说明“重石头”俗名依据________。(有V和M?)
电解制备是光电陶瓷材料
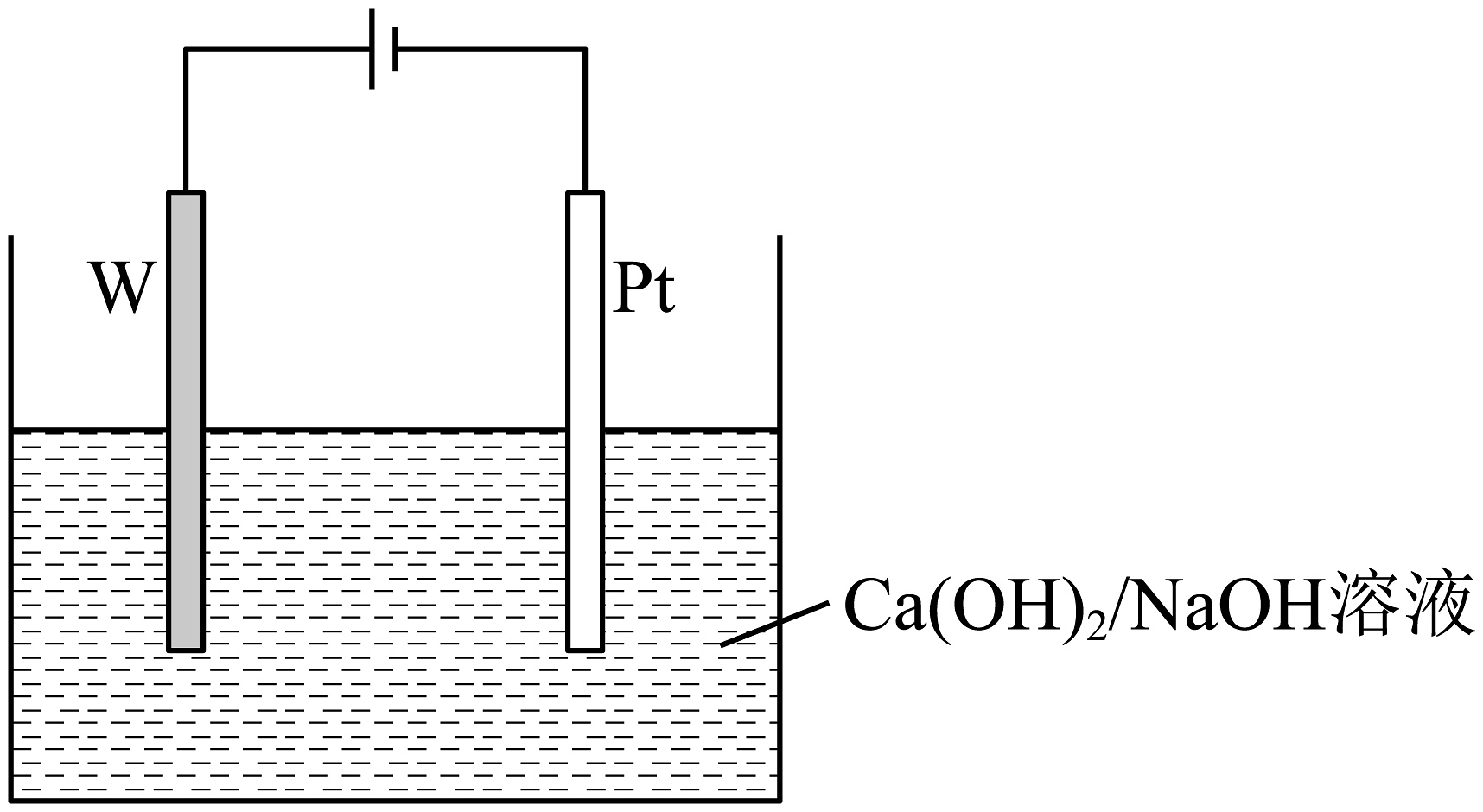
已知
(8)写出电解的阳极方程式________。
(9)为获取高纯产物,制备时需要不断通入的原因________。
20. 钛单质及其化合物在航空、航天、催化等领域应用广泛。(1)、基态Ti原子的价层电子排布式为。(2)、298K下,反应的、 , 则298K下该反应(填“能”或“不能”)自发进行。(3)、以为原料可制备。将与10.0molTi放入容积为的恒容密闭容器中,反应体系存在下列过程。编号
过程
(a)
(b)
(c)
(d)
①kJ/mol。
②不同温度下,平衡时反应体系的组成如图。曲线Ⅰ对应的物质为。

③温度下, , 反应(c)的平衡常数(列出算式,无须化简)。
(4)、钛基催化剂可以催化储氢物质肼的分解反应:(e)
(f)
为研究某钛基催化剂对上述反应的影响,以肼的水溶液为原料(含的物质的量为),进行实验,得到、随时间t变化的曲线如图。其中,为与的物质的量之和;为剩余的物质的量。设为0~t时间段内反应(e)消耗的物质的量,该时间段内,本体系中催化剂的选择性用表示。

①内,的转化率为(用含的代数式表示)。
②内,催化剂的选择性为(用含与的代数式表示,写出推导过程)。
21. Fe单质及其化合物应用广泛。回答下列问题:(1)、在元素周期表中,Fe位于第周期族。基态Fe原子与基态Fe3+离子未成对电子数之比为(2)、尿素分子(H2NCONH2)与Fe3+形成配离子的硝酸盐[Fe(H2NCONH2)6](NO3)3俗称尿素铁,既可作铁肥,又可作缓释氮肥。①元素C,N,O中,第一电离能最大的是 , 电负性最大的是
②尿素分子中,C原子采取的轨道杂化方式为
③八面体配离子[Fe(H2NCONH2)6]3+中Fe3+的配位数为6,碳氮键的键长均相等,则与Fe2+配位的原子是(填元素符号)。
(3)、α-Fe可用作合成氨催化剂、其体心立方晶胞如图所示(晶胞边长为apm)。①α-Fe晶胞中Fe原子的半径为pm。
②研究发现,α一Fe晶胞中阴影所示m,n两个截面的催化活性不同,截面单位面积含有Fe原子个数越多,催化活性越低。m,n截面中,催化活性较低的是 , 该截面单位面积含有的Fe原子为个·pm-2。
 22. 氮和氧是构建化合物的常见元素。
22. 氮和氧是构建化合物的常见元素。已知:
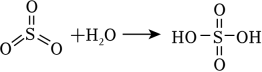
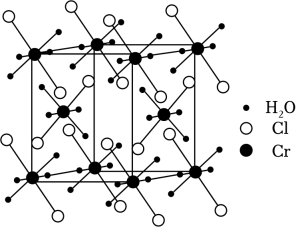
请回答:
(1)、某化合物的晶胞如图,其化学式是 , 晶体类型是 。(2)、下列说法正确的是 。A、电负性:B>N>O B、离子半径:P3﹣<S2﹣<Cl﹣ C、第一电离能:Ge<Se<As D、基态Cr的简化电子排布式:[Ar]3d4(3)、①H2N﹣NH2+H+→H2N﹣ , 其中﹣NH2的N原子杂化方式为 ;比较键角∠HNH:H2N﹣NH2中的﹣NH2H2N﹣中的﹣(填“>”、“<”或“=”),请说明理由 。②将HNO3与SO3按物质的量之比1:2发生化合反应生成A,测得A由2种微粒构成,其中之一是。比较氧化性强弱: HNO3(填“>”、“<”或“=”);写出A中阴离子的结构式 。
五、实验探究题
-
23. 氢碘酸常用于合成碘化物。某化学兴趣小组用如图装置(夹持装置等略)制备氢碘酸。

步骤如下:
ⅰ.在A中加入和 , 快速搅拌,打开通入 , 反应完成后,关闭 , 静置、过滤得滤液;
ⅱ.将滤液转移至B中,打开通入 , 接通冷凝水,加热保持微沸,直至除尽;
ⅲ.继续加热蒸馏,C中收集沸点为间的馏分,得到117mL氢碘酸(密度为 , HI质量分数为57%)。
回答下列问题:
(1)、仪器A的名称: , 通入发生反应的化学方程式:。(2)、步骤ⅰ中快速搅拌的目的:(填序号)a.便于产物分离 b.防止暴沸 c.防止固体产物包覆碘
(3)、步骤ⅰ中随着反应的进行,促进碘溶解的原因(用离子方程式表示)。(4)、步骤ⅱ中的尾气常用(填化学式)溶液吸收。(5)、步骤ⅱ实验开始时的操作顺序:先通入 , 再加热;步骤ⅲ实验结束时相对应的操作顺序:。(6)、列出本实验产率的计算表达式:。(7)、氢碘酸见光易分解,易被空气氧化,应保存在。24. 某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。(1)、浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中存在盐酸和MnO2。①反应的离子方程式是。
②电极反应式:
i还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii氧化反应:。
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱.
ii随c(Cl-)降低,。
④补充实验证实了③中的分析。
实验操作
试剂
产物
I
较浓H2SO4
有Cl2
II
a
有Cl2
III
a+b
无Cl2
a是 , b是。
(2)、利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是 , 从原子结构角度说明理由。(3)、根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是。(4)、Ag分别与1mol·L1的盐酸、氢溴酸、氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:。(5)、总结:物质氧化性和还原性变化的一般规律是。