备考2026届高考 2021-2025全国各地真题汇编 专题11 盐类水解和沉淀溶解平衡
试卷更新日期:2026-04-25 类型:二轮复习
一、选择题
-
1. 化学与生产生活密切相关,下列说法不正确的是A、具有强氧化性,可用于杀菌消毒 B、聚丙烯是高分子材料,可用作吸水剂 C、溶液呈碱性,可用于除油污 D、硬铝密度小、强度高,抗腐蚀能力强,可用作飞机材料2. 下列过程与水解反应无关的是( )A、热的纯碱溶液去除油脂 B、重油在高温、高压和催化剂作用下转化为小分子烃 C、蛋白质在酶的作用下转化为氨基酸 D、向沸水中滴入饱和溶液制备胶体3. 下列对物质性质的解释错误的是( )
选项
物质性质
解释
A
氯化钠熔点高于氯化铯
氯化钠离子键强于氯化铯
B
碘易溶于四氯化碳
碘和四氯化碳都是非极性分子
C
草酸氢钠溶液显酸性
草酸氢根离子水解程度大于电离程度
D
离子液体导电性良好
离子液体中有可移动的阴、阳离子
A、A B、B C、C D、D4. 将配制成悬浊液,向其中滴加的溶液。(M代表、或)随加入溶液体积(V)的变化关系如图所示。
下列叙述正确的是( )
A、交点a处: B、 C、时,不变 D、5. 向饱和氯水中加入少量Na2SO3固体,下列说法正确的是( )A、溶液pH减小 B、溶液颜色变深 C、溶液漂白性增强 D、溶液导电性减弱6. 室温下,用含少量的溶液制备的过程如题图所示。已知 , 。下列说法正确的是( ) A、溶液中: B、“除镁”得到的上层清液中: C、溶液中: D、“沉锰”后的滤液中:7. 一种分解氯化铵实现产物分离的物质转化关系如下,其中代表或中的一种。下列说法正确的是( )
A、溶液中: B、“除镁”得到的上层清液中: C、溶液中: D、“沉锰”后的滤液中:7. 一种分解氯化铵实现产物分离的物质转化关系如下,其中代表或中的一种。下列说法正确的是( )
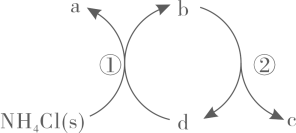 A、、分别是 B、既可以是 , 也可以是 C、已知为副产物,则通入水蒸气可减少的产生 D、等压条件下,反应、的反应热之和,小于氯化铵直接分解的反应热8. 甲酸是重要的化工原料。工业废水中的甲酸及其盐,通过离子交换树脂(含固体活性成分 , R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上甲酸根的物质的量分数)与废水初始关系如图(已知甲酸),下列说法错误的是
A、、分别是 B、既可以是 , 也可以是 C、已知为副产物,则通入水蒸气可减少的产生 D、等压条件下,反应、的反应热之和,小于氯化铵直接分解的反应热8. 甲酸是重要的化工原料。工业废水中的甲酸及其盐,通过离子交换树脂(含固体活性成分 , R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上甲酸根的物质的量分数)与废水初始关系如图(已知甲酸),下列说法错误的是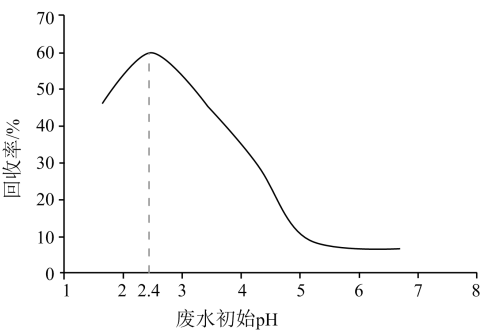 A、活性成分在水中存在平衡: B、的废水中 C、废水初始 , 随下降,甲酸的电离被抑制,与作用的数目减少 D、废水初始 , 离子交换树脂活性成分主要以形态存在9. 已知: Kap= 1.8×10-10
A、活性成分在水中存在平衡: B、的废水中 C、废水初始 , 随下降,甲酸的电离被抑制,与作用的数目减少 D、废水初始 , 离子交换树脂活性成分主要以形态存在9. 已知: Kap= 1.8×10-10K=1.1×105
下列有关说法不正确的是( )
A、过量AgCI在1.0mol/LNaCl溶液中,c(Ag+)=1.8X10-10mol/L B、过量AgCI在水中所得的饱和溶液中滴加0.0010mol/LAgNO3溶液,有AgCl生成 C、过量AgCl在水中溶解的质量大于在相同体积3.0mol/LNaCI溶液中溶解的质量 D、0.010molAgCI在1L10mol/L的盐酸中不能完全溶解10. 已知为两性氢氧化物,在不同pH条件下,与的总和为c,现有如下图:下列说法正确的是( ) A、由M点可以计算 B、恰好完全沉淀的 C、P点溶液质量小于Q点溶液质量 D、随着pH的增大溶液中比值先增大后减小11. 环境保护工程师研究利用Na2S、FeS和H2S处理水样中的Cd2+。
A、由M点可以计算 B、恰好完全沉淀的 C、P点溶液质量小于Q点溶液质量 D、随着pH的增大溶液中比值先增大后减小11. 环境保护工程师研究利用Na2S、FeS和H2S处理水样中的Cd2+。已知25℃时,H2S饱和溶液浓度约为0.1mol•L﹣1 , Ka1(H2S)=10﹣6.97 , Ka2(H2S)=10﹣12.90 , Ksp(FeS)=10﹣17.20 , Ksp(CdS)=10﹣26.10。
下列说法错误的是( )
A、Na2S溶液中:c(H+)+c(Na+)=c(OH﹣)+c(HS﹣)+2c(S2﹣) B、0.01mol•L﹣1Na2S溶液中:c(Na+)>c(S2﹣)>c(OH﹣)>c(HS﹣) C、向c(Cd2+)=0.01mol•L﹣1的溶液中加入FeS,可使c(Cd2+)<10﹣8mol•L﹣1 D、向c(Cd2+)=0.01mol•L﹣1的溶液中通入H2S气体至饱和,所得溶液中:c(H+)>c(Cd2+)12. 锂辉石是锂的重要来源,其焙烧后的酸性浸出液中含有和杂质离子,可在0~14范围内调节对其净化(即相关离子浓度)。时,与关系见下图(碱性过强时和会部分溶解)。下列说法正确的是( )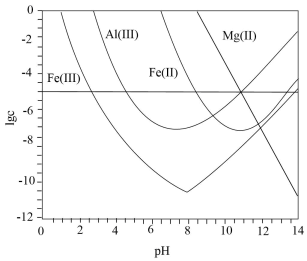 A、可被净化的区间最大 B、加入适量 , 可进一步提升净化程度 C、净化的先后顺序: D、13. 室温时,用 的标准 溶液滴定 浓度相等的 、 和 混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用)。
A、可被净化的区间最大 B、加入适量 , 可进一步提升净化程度 C、净化的先后顺序: D、13. 室温时,用 的标准 溶液滴定 浓度相等的 、 和 混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用)。

若溶液中离子浓度小于 时,认为该离子沉淀完全。 , , )。下列说法正确的是( )
A、a点:有白色沉淀生成 B、原溶液中 的浓度为 C、当 沉淀完全时,已经有部分 沉淀 D、b点:14. 铜(I)、乙腈(简写为L)的某水溶液体系中含铜物种的分布曲线如图。纵坐标(δ)为含铜物种占总铜的物质的量分数,总铜浓度为。下列描述正确的是( ) A、的 B、当时, C、n从0增加到2,结合L的能力随之减小 D、若 , 则15. 常温下,溶液中以氢氧化物形式沉淀时,与的关系如图[其中X代表或]。
A、的 B、当时, C、n从0增加到2,结合L的能力随之减小 D、若 , 则15. 常温下,溶液中以氢氧化物形式沉淀时,与的关系如图[其中X代表或]。已知: , 比更易与碱反应,形成;溶液中时,X可忽略不计。

下列说法错误的是( )
A、L为与的关系曲线 B、的平衡常数为 C、调节溶液浓度,通过碱浸可完全分离和 D、调节溶液为 , 可将浓度均为的和完全分离16. 乙二胺( , 简写为Y)可结合转化为(简写为)(简写为)。与Y可形成和两种配离子。室温下向溶液中加入Y,通过调节混合溶液的改变Y的浓度,从而调控不同配离子的浓度(忽略体积变化)。混合溶液中和Y的初始浓度分别为和。与的变化关系如图1所示(其中M代表、或),分布系数与的变化关系如图2所示(其中N代表Y、或)。比如。
下列说法错误的是( )
A、曲线I对应的离子是 B、最大时对应的 C、反应的平衡常数 D、时,二、填空题
-
17. 我国科研人员以高炉渣(主要成分为 , , 和等)为原料,对炼钢烟气(和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:

已知:
(1)、高炉渣与经焙烧产生的“气体”是。(2)、“滤渣”的主要成分是和。(3)、“水浸2”时主要反应的化学方程式为 , 该反应能进行的原因是。(4)、铝产品可用于。(5)、某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞底面显示为图丙,晶胞参数。图丙中与N的距离为;化合物的化学式是 , 其摩尔质量为 , 阿伏加德罗常数的值是 , 则晶体的密度为(列出计算表达式)。
三、实验探究题
-
18. 二氧化硫脲(TD)是还原性漂白剂,可溶于水,难溶于乙醇,在受热或碱性条件下易水解:。其制备与应用探究如下:
Ⅰ.由硫脲制备TD
按如图装置,在三颈烧瓶中加入硫脲和水,溶解,冷却至5℃后,滴入溶液,控制温度低于10℃和进行反应。反应完成后,结晶、过滤、洗涤、干燥后得到产品TD。
Ⅱ.用TD进行高岭土原矿脱色(去除)探究
将高岭土原矿(质量分数为)制成悬浊液,加入TD,在一定条件下充分反应,静置,分离出上层清液 , 用分光光度法测得该清液中浓度为 , 计算的去除率。

回答下列问题:
(1)、仪器的名称是。(2)、Ⅰ中控制“温度低于10℃和”的目的是。(3)、写出制备TD的化学方程式。(4)、中S的化合价为。Ⅰ的反应中,因条件控制不当生成了 , 最终导致TD中出现黄色杂质,该杂质是(填化学式)。(5)、Ⅰ中“洗涤”选用乙醇的理由是。(6)、高岭土中去除率为(用含的代数式表示)。Ⅱ中“静置”时间过长,导致脱色效果降低的原因是。19. 胆矾( )易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的 (杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:(1)、制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有(填标号)。A.烧杯 B.容量瓶 C.蒸发皿 D.移液管
(2)、将 加入到适量的稀硫酸中,加热,其主要反应的化学方程式为 , 与直接用废铜和浓硫酸反应相比,该方法的优点是。(3)、待 完全反应后停止加热,边搅拌边加入适量 ,冷却后用 调 为3.5~4,再煮沸 ,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、、乙醇洗涤、 , 得到胆矾。其中,控制溶液 为3.5~4的目的是 , 煮沸 的作用是。(4)、结晶水测定:称量干燥坩埚的质量为 ,加入胆矾后总质量为 ,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为 。根据实验数据,胆矾分子中结晶水的个数为(写表达式)。(5)、下列操作中,会导致结晶水数目测定值偏高的是(填标号)。①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少胆矾迸溅出来
四、综合题
-
20. 以银锰精矿主要含、、和氧化锰矿主要含为原料联合提取银和锰的一种流程示意图如下。
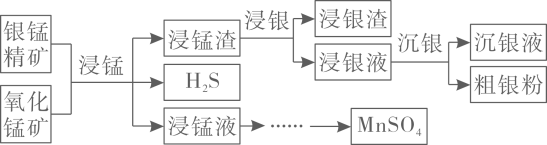
已知:酸性条件下,的氧化性强于。
(1)、“浸锰”过程是在溶液中使矿石中的锰元素浸出,同时去除 , 有利于后续银的浸出;矿石中的银以的形式残留于浸锰渣中。“浸锰”过程中,发生反应 , 则可推断:填“”或“”。
在溶液中,银锰精矿中的和氧化锰矿中的发生反应,则浸锰液中主要的金属阳离子有。
(2)、“浸银”时,使用过量和的混合液作为浸出剂,将中的银以形式浸出。将“浸银”反应的离子方程式补充完整:
结合平衡移动原理,解释浸出剂中的作用:。
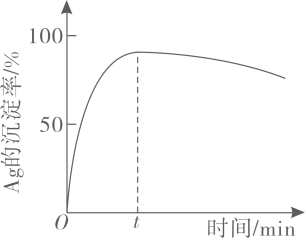
(3)、“沉银”过程中需要过量的铁粉作为还原剂。该步反应的离子方程式有。
一定温度下,的沉淀率随反应时间的变化如图所示。解释分钟后的沉淀率逐渐减小的原因:。
 (4)、结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:。21. 催化剂能催化脱除烟气中的NO,反应为 。(1)、催化剂的制备。将预先制备的一定量的粉末置于80℃的水中,在搅拌下加入一定量的溶液,经蒸发、焙烧等工序得到颗粒状催化剂。在水溶液中水解为沉淀的离子方程式为;反应选用溶液而不选用溶液的原因是。(2)、催化剂的应用。将一定物质的量浓度的NO、、(其余为)气体匀速通过装有催化剂的反应器,测得NO的转化率随温度的变化如题图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是;反应温度高于380℃,NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有(用化学方程式表示)。
(4)、结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:。21. 催化剂能催化脱除烟气中的NO,反应为 。(1)、催化剂的制备。将预先制备的一定量的粉末置于80℃的水中,在搅拌下加入一定量的溶液,经蒸发、焙烧等工序得到颗粒状催化剂。在水溶液中水解为沉淀的离子方程式为;反应选用溶液而不选用溶液的原因是。(2)、催化剂的应用。将一定物质的量浓度的NO、、(其余为)气体匀速通过装有催化剂的反应器,测得NO的转化率随温度的变化如题图所示。反应温度在320~360℃范围内,NO转化率随温度变化不明显的原因是;反应温度高于380℃,NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有(用化学方程式表示)。 (3)、废催化剂的回收。回收废催化剂并制备的过程可表示为
(3)、废催化剂的回收。回收废催化剂并制备的过程可表示为
①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有。
②通过萃取可分离钒和钨,在得到的钒酸中含有。已知具有八元环结构,其结构式可表示为。
③向pH=8的溶液中加入过量的溶液,生成沉淀。已知: , 加过量溶液的目的是。
五、流程题
-
22. 钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。

注:加沉淀剂使一种金属离子浓度小于等于 , 其他金属离子不沉淀,即认为完全分离。
已知:①。
②以氢氧化物形式沉淀时,和溶液的关系如图所示。
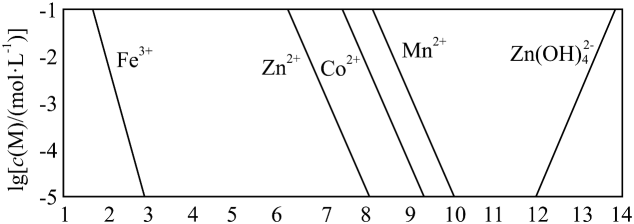
回答下列问题:
(1)、“酸浸”前,需将废渣磨碎,其目的是。(2)、“酸浸”步骤中,发生反应的化学方程式是。(3)、假设“沉铜”后得到的滤液中和均为 , 向其中加入至沉淀完全,此时溶液中 , 据此判断能否实现和的完全分离(填“能”或“不能”)。(4)、“沉锰”步骤中,生成 , 产生的物质的量为。(5)、“沉淀”步骤中,用调 , 分离出的滤渣是。(6)、“沉钴”步骤中,控制溶液 , 加入适量的氧化 , 其反应的离子方程式为。(7)、根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是。23. 稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下: 
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,稀土离子保持 价不变; 的 ; 开始溶解时的pH为8.8;有关金属离子沉淀的相关pH见下表。
离子
开始沉淀时的pH
8.8
1.5
3.6
6.2~7.4
沉淀完全时的pH
/
3.2
4.7
/
(1)、“氧化调pH”中,化合价有变化的金属离子是。(2)、“过滤1”前,用 溶液调pH至的范围内,该过程中 发生反应的离子方程式为。(3)、“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于 (保留两位有效数字)。(4)、①“加热搅拌”有利于加快 溶出、提高产率,其原因是。②“操作X”的过程为:先 , 再固液分离。
(5)、该工艺中,可再生循环利用的物质有(写化学式)。(6)、稀土元素钇(Y)可用于制备高活性的合金类催化剂 。①还原 和 熔融盐制备 时,生成
 转移 电子。
转移 电子。② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为。
-