备考2026届高考 2021-2025全国各地真题汇编 专题9 化学反应速率与化学平衡
试卷更新日期:2026-04-25 类型:二轮复习
一、选择题
-
1. 下列措施能降低化学反应速率的是( )A、催化氧化氨制备硝酸时加入铂 B、中和滴定时,边滴边摇锥形瓶 C、锌粉和盐酸反应时加水稀释 D、石墨合成金刚石时增大压强2. 加氢转化成甲烷,是综合利用实现“碳中和”和“碳达峰”的重要方式。525℃,101kPa下,。反应达到平衡时,能使平衡向正反应方向移动的是( )A、减小体系压强 B、升高温度 C、增大浓度 D、恒容下充入惰性气体3. 为研究三价铁配合物性质进行如下实验(忽略溶液体积变化)。

已知:为黄色、为红色、为无色。
下列说法不正确的是( )
A、①中浓盐酸促进平衡正向移动 B、由①到②,生成并消耗 C、②、③对比,说明:②>③ D、由①→④推断,若向①深黄色溶液中加入、淀粉溶液,溶液也无明显变化4. 下列实验操作能达到实验目的的是( )选项
实验操作
实验目的
A
将铁制镀件与铜片分别接直流电源的正、负极,平行浸入CuSO4溶液中
在铁制镀件表面镀铜
B
向粗盐水中先后加入过量NaCO3溶液、NaOH液和 BaCl2溶液
粗盐提纯中,去除Ca2+、Mg2+和SO42-杂质离子
C
向2mL0.1mol·L-1K2Cr2O7溶液中滴加5滴6mol·L-1NaOH溶液,再滴加5滴6mol·L-1H2SO4溶液
探究c(H+)对如下平衡的影响:Cr2O72-+H2O ==2CrO42-+ 2H+
(橙色) (黄色)
D
将有机物M溶于乙醇,加入金属钠
操究M中是否含有羟基
A、A B、B C、C D、D5. 一定条件下,“”4种原料按固定流速不断注入连续流动反应器中,体系pH-t振荡图像及涉及反应如下。其中AB段发生反应①~④,①②为快速反应。下列说法错误的是( )
①
②
③
④
⑤
A、原料中不影响振幅和周期 B、反应④: C、反应①~④中,对的氧化起催化作用 D、利用pH响应变色材料,可将pH振荡可视化6. 已知298K,101kPa时,。该反应在密闭的刚性容器中分别于T1、T2温度下进行,CO2的初始浓度为 , 关系如图所示。下列说法错误的是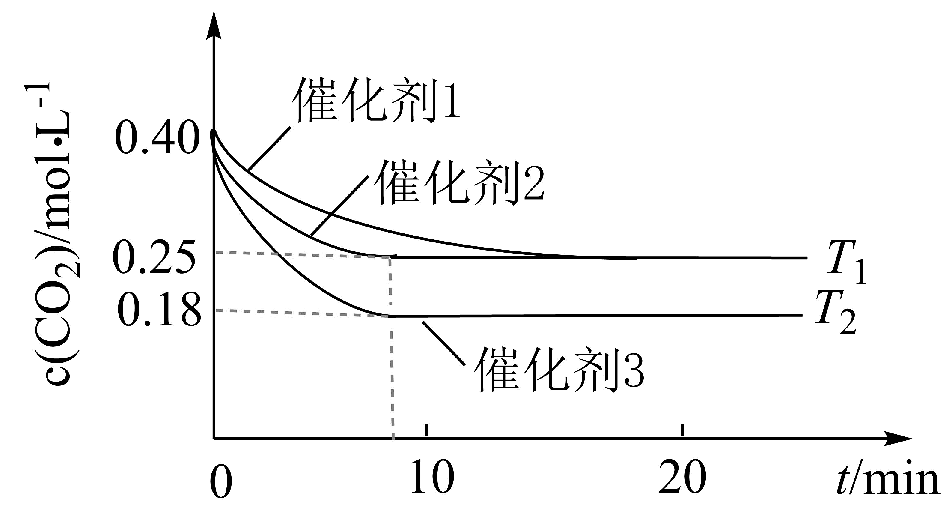 A、T1>T2 B、T1下反应达到平衡时 C、使用催化剂1的反应活化能比催化剂2的大 D、使用催化剂2和催化剂3的反应历程相同7. 温度T下,向1L真空刚性容器中加入 , 反应达到平衡时, ,
A、T1>T2 B、T1下反应达到平衡时 C、使用催化剂1的反应活化能比催化剂2的大 D、使用催化剂2和催化剂3的反应历程相同7. 温度T下,向1L真空刚性容器中加入 , 反应达到平衡时, ,下列说法正确的是
A、再充入1mol X和1mol Y,此时 B、再充入1mol X,平衡时 C、再充入 , 平衡向右移动 D、若温度升高,X的转化率增加,则上述反应8. 室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下
的影响因素,测得不同条件下 浓度随时间变化关系如图。
浓度随时间变化关系如图。实验序号
水样体积/mL
纳米铁质量/mg
水样初始pH
①
50
8
6
②
50
2
6
③
50
2
8

下列说法正确的是( )
A、实验①中,0~2小时内平均反应速率v()=2.0mol•L﹣1•h﹣1 B、实验③中,反应的离子方程式为:2Fe++8H+═2Fe3++Se+4H2O C、其他条件相同时,适当增加纳米铁质量可加快反应速率 D、其他条件相同时,水样初始pH越小,的去除效果越好9. 在恒温恒容密闭容器中充入一定量W(g),发生如下反应:
反应②和③的速率方程分别为v2=k2c2(X)和v3=k3c(Z),其中k2、k3分别为反应②和③的速率常数,反应③的活化能大于反应②。测得W(g)的浓度随时间的变化如下表。
t/min
0
1
2
3
4
5
c(W)/(mol•L﹣1)
0.160
0.113
0.080
0.056
0.040
0.028
下列说法正确的是( )
A、0~2min内,X的平均反应速率为0.080mol•L﹣1•min﹣1 B、若增大容器容积,平衡时Y的产率增大 C、若k2=k3 , 平衡时c(Z)=c(X) D、若升高温度,平衡时c(Z)减小10. 金属硫化物()催化反应 , 既可以除去天然气中的 , 又可以获得。下列说法正确的是( ) A、该反应的 B、该反应的平衡常数 C、题图所示的反应机理中,步骤Ⅰ可理解为中带部分负电荷的S与催化剂中的M之间发生作用 D、该反应中每消耗 , 转移电子的数目约为11. 下列事实能用平衡移动原理解释的是( )A、溶液中加入少量固体,促进分解 B、密闭烧瓶内的和的混合气体,受热后颜色加深 C、铁钉放入浓中,待不再变化后,加热能产生大量红棕色气体 D、锌片与稀反应过程中,加入少量固体,促进的产生12. 向恒温恒容密闭容器中通入2mol 和1mol , 反应达到平衡后,再通入一定量 , 达到新平衡时,下列有关判断错误的是( )A、的平衡浓度增大 B、反应平衡常数增大 C、正向反应速率增大 D、的转化总量增大13. 下列实验操作及现象能得出相应结论的是( )
A、该反应的 B、该反应的平衡常数 C、题图所示的反应机理中,步骤Ⅰ可理解为中带部分负电荷的S与催化剂中的M之间发生作用 D、该反应中每消耗 , 转移电子的数目约为11. 下列事实能用平衡移动原理解释的是( )A、溶液中加入少量固体,促进分解 B、密闭烧瓶内的和的混合气体,受热后颜色加深 C、铁钉放入浓中,待不再变化后,加热能产生大量红棕色气体 D、锌片与稀反应过程中,加入少量固体,促进的产生12. 向恒温恒容密闭容器中通入2mol 和1mol , 反应达到平衡后,再通入一定量 , 达到新平衡时,下列有关判断错误的是( )A、的平衡浓度增大 B、反应平衡常数增大 C、正向反应速率增大 D、的转化总量增大13. 下列实验操作及现象能得出相应结论的是( )选项
实验操作及现象
结论
A
向盛有与的恒压密闭容器中通入一定体积的 , 最终气体颜色变浅
化学平衡向减少的方向移动
B
以为指示剂,用标准溶液滴定溶液中的 , 先出现白色沉淀,后出现砖红色沉淀
C
向盛有溶液的试管中加入过量铁粉,充分反应后静置,滴加KSCN溶液无明显变化;静置,取上层清液滴加几滴氯水,溶液变红
具有还原性
D
向盛有2mL饱和溶液的试管中滴加鸡蛋清溶液,振荡,有沉淀析出;加蒸馏水稀释,再振荡,沉淀溶解
蛋白质沉淀后活性改变
A、A B、B C、C D、D二、填空题
-
14. 在某温度下,在体积为5L的密闭容器内发生如下反应:CH4(g)+H2O(g)⇌CO(g)+3H2(g)﹣Q(1)、在上述反应的反应物与生成物中,非极性分子为:。(2)、若反应20min后气体总物质的量增加了10mol,则甲烷的平均反应速率为 。(3)、下列选项中的物理量不变时,一定可以判断反应达到平衡的是 ____。A、容器中氢元素的质量分数 B、容器内的压强 C、反应的平衡常数 D、容器内气体的平均相对分子质量(4)、在某一时刻,v正=v逆=v0 , 反应若改变一条件,可使得v正<v逆<v0 , 指出可以改变的条件,并说明理由:。
已知CO与H2合成CH3OH是可逆反应:CO+2H2⇌CH3OH。
(5)、若上述反应达到平衡时CO与H2的转化率相同,则投料比n(CO):n(H2)=。三、实验探究题
-
15. 化学反应平衡常数对认识化学反应的方向和限度具有指导意义。实验小组研究测定“”平衡常数的方法,对照理论数据判断方法的可行性。(1)、理论分析
①易挥发,需控制生成较小。
②根据时分析,控制合适 , 可使生成较小;用浓度较大的溶液与过量反应,反应前后几乎不变; , 仅需测定平衡时溶液和。
③与水反应的程度很小,可忽略对测定干扰;低浓度挥发性很小,可忽略。
实验探究
序号
实验内容及现象
I
, 将溶液()与过量混合,密闭并搅拌,充分反应后,溶液变为黄色,容器液面上方有淡黄色气体。
Ⅱ
, 将溶液()与过量混合,密闭并搅拌,反应时间与I相同,溶液变为淡黄色,容器液面上方未观察到黄色气体。
Ⅲ
测定I、Ⅱ反应后溶液的;取一定量反应后溶液,加入过量固体,用标准溶液滴定,测定。
已知:;和溶液颜色均为无色。
①Ⅲ中,滴定时选用淀粉作指示剂,滴定终点时的现象是。用离子方程式表示的作用:。
②I中,与反应前的溶液相比,反应后溶液的(填“增大”、“减小”或“不变”)。平衡后,按计算所得值小于的K值,是因为挥发导致计算时所用的浓度小于其在溶液中实际浓度。
③Ⅱ中,按计算所得值也小于的K值,可能原因是。
(2)、实验改进分析实验I、Ⅱ中测定结果均偏小的原因,改变实验条件,再次实验。
控制反应温度为 , 其他条件与Ⅱ相同,经实验准确测得该条件下的平衡常数。
①判断该实验测得的平衡常数是否准确,应与值比较。
②综合调控和温度的目的是。
16. 我国科学家研发出一种乙醇(沸点78.5℃)绿色制氢新途径,并实现高附加值乙酸(沸点118℃)的生产,主要反应为:Ⅰ.
Ⅱ.
回答下列问题:
(1)、乙醇可由秸秆生产,主要过程为秸秆纤维素乙醇
(2)、对于反应Ⅰ:①已知 则。
②一定温度下,下列叙述能说明恒容密闭容器中反应达到平衡状态的是(填标号)。
A.容器内的压强不再变化
B.混合气体的密度不再变化
C.的体积分数不再变化
D.单位时间内生成 , 同时消耗
③反应后从混合气体分离得到 , 最适宜的方法为。
(3)、恒压100kPa下,向密闭容器中按投料,产氢速率和产物的选择性随温度变化关系如图1,关键步骤中间体的能量变化如图2。[比如:乙酸选择性]
①由图1可知,反应Ⅰ最适宜的温度为270℃,原因为。
②由图中信息可知,乙酸可能是(填“产物1”“产物2”或“产物3”)。
③270℃时,若该密闭容器中只发生反应Ⅰ、Ⅱ,平衡时乙醇的转化率为90%,乙酸的选择性为80%,则 , 平衡常数(列出计算式即可;用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
17. 乙二醇是一种重要化工原料,以合成气为原料合成乙二醇具有重要意义。Ⅰ.直接合成法: , 不同温度下平衡常数如下表所示。
温度
298K
355K
400K
平衡常数
10
(1)、该反应的0(填“>”或“<”)。(2)、已知的燃烧热分别为 , 则上述合成反应的(用a、b和c表示)。(3)、实验表明,在500K时,即使压强(34MPa)很高乙二醇产率(7%)也很低,可能的原因是(答出1条即可)。Ⅱ.间接合成法:用合成气和制备的DMO合成乙二醇,发生如下3个均放热的连续反应,其中MG生成乙二醇的反应为可逆反应。
 (4)、在2MPa、催化、固定流速条件下,发生上述反应,初始氢酯比 , 出口处检测到DMO的实际转化率及MG、乙二醇、乙醇的选择性随温度的变化曲线如图所示[某物质的选择性]。
(4)、在2MPa、催化、固定流速条件下,发生上述反应,初始氢酯比 , 出口处检测到DMO的实际转化率及MG、乙二醇、乙醇的选择性随温度的变化曲线如图所示[某物质的选择性]。
①已知曲线Ⅱ表示乙二醇的选择性,则曲线(填图中标号,下同)表示DMO的转化率,曲线表示MG的选择性。
②有利于提高A点DMO转化率的措施有(填标号)。
A.降低温度 B.增大压强
C.减小初始氢酯比 D.延长原料与催化剂的接触时间
③483K时,出口处的值为(精确至0.01)。
④A点反应的浓度商(用物质的量分数代替浓度计算,精确至0.001)。
四、综合题
-
18. 甲烷转化为多碳化合物具有重要意义。一种将甲烷溴化再偶联为丙烯()的研究所获得的部分数据如下。回答下列问题:(1)、已知如下热化学方程式:
计算反应的。
(2)、与反应生成 , 部分会进一步溴化。将和。通入密闭容器,平衡时,、与温度的关系见下图(假设反应后的含碳物质只有、和)。
(i)图中的曲线是(填“a”或“b”)。
(ii)时,的转化 , 。
(iii)时,反应的平衡常数。
(3)、少量可提高生成的选择性。时,分别在有和无的条件下,将和 , 通入密闭容器,溴代甲烷的物质的量(n)随时间(t)的变化关系见下图。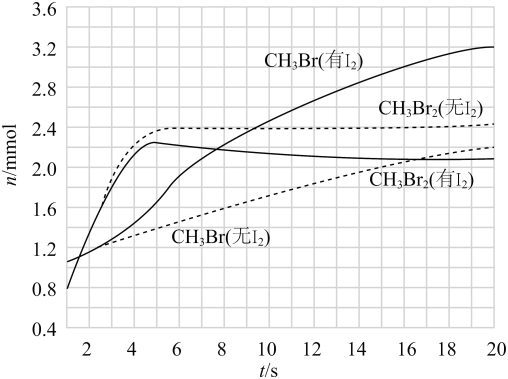
(i)在之间,有和无时的生成速率之比。
(ii)从图中找出提高了选择性的证据:。
(ⅲ)研究表明,参与反应的可能机理如下:
①
②
③
④
⑤
⑥
根据上述机理,分析提高选择性的原因:。
19. 氧气、二氧化氯常用于漂白、杀菌,有重要的应用价值。请回答:
(1)、下列措施中能提高新制饱和氣水中HClO浓度的是____。A、加 NaCI固体 B、加水 C、加 CaCO3粉末 D、加足量Ca(OH)2溶液(2)、氯气常用于自来水消毒。稀氯水中存在如下反应(不考虑其他反应):Ⅰ.Cl2(aq)+ H2O(I)=H+ (aq)+CI- (aq)+ HClO(aq)
Ⅱ.2HClO(aq)=Cl2O(aq)+H2O(D) K=10-2.0
Ⅲ.HClO(aq)=H+(aq)+ ClO-(aq)
T1℃时,在不同pH下,约2mg/L氯水中部分含氯微粒的平衡浓度对数值(lgc)如图1所示(溶液体积保持不变)。
①Cl2O分子的空间构型是。
②在pH=4~9之间,ClO-浓度增加,其最大来源是(填含氣微粒符号)。
③该氣水中氯元素质量守恒表达式:c(CI-)=c(HClO)+。
④在图中画出pH=4~9之间,1gc(Cl2O)随pH的变化曲线。
 (3)、某研究小组提出,商用ClO2(常含杂质Cl2)在水中易发生如下反应,影响自来水消毒效果。
(3)、某研究小组提出,商用ClO2(常含杂质Cl2)在水中易发生如下反应,影响自来水消毒效果。Ⅳ.2ClO2(aq)+ H2O(I) = ClO3-(aq)+ClO2-(aq)+2H+ (aq)
Ⅴ.2ClO2(aq)+ ClO-(aq)+ H2O(I) - 2ClO3-(aq) + 2H+(aq) + CI- (aq)
ClO,中Cl,含量对ClO,反应初始速率[u(ClO2)]的影响如图2所示。实验条件:
T2℃,ClO2初始浓度相同。
①Cl2的存在主要加快了反应(填“IV”或“V”)。
②指出改变υ初始(ClO2)的影响因素,并解释原因。
20. 乙二醇(EG)是一种重要的基础化工原料,可通过石油化工和煤化工等工业路线合成。(1)、石油化工路线中,环氧乙烷(EO)水合工艺是一种成熟的乙二醇生产方法,环氧乙烷和水反应生成乙二醇,伴随生成二乙二醇(DEG)的副反应。主反应:
副反应:
体系中环氧乙烷初始浓度为 , 恒温下反应30min,环氧乙烷完全转化,产物中。
①0~30min内,
②下列说法正确的是(填序号)。
a.主反应中,生成物总能量高于反应物总能量
b.0~30min内,
c.0~30min内,
d.选择适当催化剂可提高乙二醇的最终产率
(2)、煤化工路线中,利用合成气直接合成乙二醇,原子利用率可达100%,具有广阔的发展前景。反应如下:。按化学计量比进料,固定平衡转化率 , 探究温度与压强的关系。分别为0.4、0.5和0.6时,温度与压强的关系如图:
①代表的曲线为(填“”“”或“”);原因是。
②0(填“>”“<”或“=”)。
③已知:反应 , , x为组分的物质的量分数。M、N两点对应的体系,(填“>”“<”或“=”),D点对应体系的的值为。
④已知:反应 , , p为组分的分压。调整进料比为 , 系统压强维持 , 使 , 此时(用含有m和的代数式表示)。
五、流程题
-
21. 某含锶(Sr)废渣主要含有SrSO4、SiO2、CaCO3、SrCO3和MgCO3等,一种提取该废渣中锶的流程如下图所示.

已知25℃时,
回答下列问题:
(1)、锶位于元素周期表第五周期第ⅡA族.基态原子价电子排布式为 .(2)、“浸出液”中主要的金属离子有Sr2+ 、 (填离子符号).(3)、“盐浸”中转化反应的离子方程式为;25℃时,向0.01mol SrSO4粉末中加入100mL 0.11mol▪L-1BaCl2溶液,充分反应后,理论上溶液中= (忽略溶液体积的变化).
(4)、其他条件相同时,盐浸2h,浸出温度对锶浸出率的影响如图1所示.随温度升高锶浸出率增大的原因是. (5)、“漫出渣2”中主要含有 、 (填化学式).(6)、将窝穴体a(结构如图2所示)与形成的超分子加入“浸出液”中,能提取其中的 , 原因是.(7)、由制备无水的最优方法是 (填标号).
(5)、“漫出渣2”中主要含有 、 (填化学式).(6)、将窝穴体a(结构如图2所示)与形成的超分子加入“浸出液”中,能提取其中的 , 原因是.(7)、由制备无水的最优方法是 (填标号).a.加热脱水
b.在 HCl气流中加热
c.常温加压
d.加热加压
22. 白云石的主要化学成分为 , 还含有质量分数约为2.1%的Fe2O3和1.0%的SiO2。利用白云石制备高纯度的碳酸钙和氧化镁,流程示意图如下。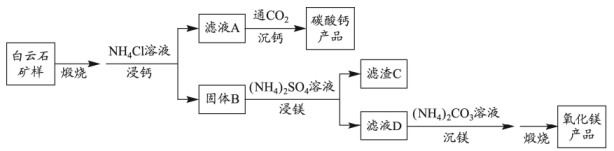
已知:
物质
(1)、白云石矿样煅烧完全分解的化学方程式为。(2)、用量对碳酸钙产品的影响如下表所示。氧化物()浸出率/%
产品中纯度/%
产品中Mg杂质含量/%
(以计)
计算值
实测值
2.1∶1
98.4
1.1
99.1
99.7
——
2.2∶1
98.8
1.5
98.7
99.5
0.06
2.4∶1
99.1
6.0
95.2
97.6
2.20
备注:ⅰ、浸出率=(浸出的质量/煅烧得到的质量)(M代表Ca或Mg)
ⅱ、纯度计算值为滤液A中钙、镁全部以碳酸盐形式沉淀时计算出的产品中纯度。
①解释“浸钙”过程中主要浸出的原因是。
②沉钙反应的离子方程式为。
③“浸钙”过程不适宜选用的比例为。
④产品中纯度的实测值高于计算值的原因是。
(3)、“浸镁”过程中,取固体B与一定浓度的溶液混合,充分反应后的浸出率低于60%。加热蒸馏,的浸出率随馏出液体积增大而增大,最终可达98.9%。从化学平衡的角度解释浸出率增大的原因是。(4)、滤渣C中含有的物质是。(5)、该流程中可循环利用的物质是。
-