备考2026届高考 2021-2025全国各地真题汇编 专题6 化学键 分子和晶体的结构与性质
试卷更新日期:2026-04-25 类型:二轮复习
一、选择题
-
1. 下列化学用语表示不正确的是( )A、CH4的结构式:
 B、基态氧原子的轨道表示式
B、基态氧原子的轨道表示式 C、p 电子云轮廓图:
C、p 电子云轮廓图: D、CH3CH(CH2CH3)CH2CH3的系统命名:2-乙基丁烷
2. 下列属于极性分子的是A、 B、 C、 D、3. 下列物质均为共价晶体且成键结构相似,其中熔点最低的是A、金刚石(C) B、单晶硅() C、金刚砂() D、氮化硼( , 立方相)4. 仪器分析在化学研究中有重要应用。下列方法选择错误的是( )A、用pH计区分KCl溶液和NaNO3溶液 B、用X射线衍射法区分玻璃和蓝宝石 C、用原子光谱鉴定样品中含有元素Li D、用质谱区分正己醇和正庚醇5. 基本概念和理论是化学思维的基石。下列叙述错误的是A、理论认为模型与分子的空间结构相同 B、元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律 C、泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子 D、杂化轨道由1个s轨道和3个p轨道混杂而成6. 是一种合成聚酯的催化剂,可用“硝酸钠法”制备,反应方程式为。下列说法错误的是( )A、中元素的化合价为 B、的空间结构为平面三角形 C、反应中氧化剂和还原剂的物质的量之比为 D、反应中消耗 , 转移7. 能代表化合物(N2H4)2Zn(SO4)2的结构片段如图(氢原子未画出),下列有关该化合物的描述不正确的是( )
D、CH3CH(CH2CH3)CH2CH3的系统命名:2-乙基丁烷
2. 下列属于极性分子的是A、 B、 C、 D、3. 下列物质均为共价晶体且成键结构相似,其中熔点最低的是A、金刚石(C) B、单晶硅() C、金刚砂() D、氮化硼( , 立方相)4. 仪器分析在化学研究中有重要应用。下列方法选择错误的是( )A、用pH计区分KCl溶液和NaNO3溶液 B、用X射线衍射法区分玻璃和蓝宝石 C、用原子光谱鉴定样品中含有元素Li D、用质谱区分正己醇和正庚醇5. 基本概念和理论是化学思维的基石。下列叙述错误的是A、理论认为模型与分子的空间结构相同 B、元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律 C、泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子 D、杂化轨道由1个s轨道和3个p轨道混杂而成6. 是一种合成聚酯的催化剂,可用“硝酸钠法”制备,反应方程式为。下列说法错误的是( )A、中元素的化合价为 B、的空间结构为平面三角形 C、反应中氧化剂和还原剂的物质的量之比为 D、反应中消耗 , 转移7. 能代表化合物(N2H4)2Zn(SO4)2的结构片段如图(氢原子未画出),下列有关该化合物的描述不正确的是( ) A、图中球①代表原子团NH2 B、该化合物易溶于水 C、作还原剂时,该化合物释放H+ D、氮原子上没有孤电子对,晶体中不存在氢键8. 如图是X的晶胞结构,有关说法正确是( )
A、图中球①代表原子团NH2 B、该化合物易溶于水 C、作还原剂时,该化合物释放H+ D、氮原子上没有孤电子对,晶体中不存在氢键8. 如图是X的晶胞结构,有关说法正确是( ) A、X种含有键 B、X是混合晶体 C、X的分子式为 D、X种C原子有一对孤电子9. 以下氮氧化合物, , , 的结构式,有关说法正确的是( )
A、X种含有键 B、X是混合晶体 C、X的分子式为 D、X种C原子有一对孤电子9. 以下氮氧化合物, , , 的结构式,有关说法正确的是( )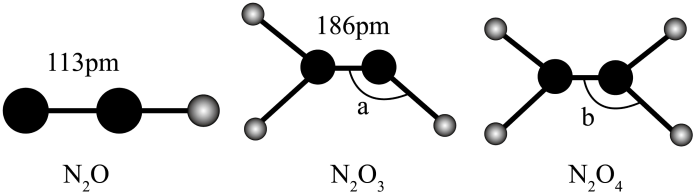 A、氮氮键的键能: B、熔点: C、分子的极性: D、的键角:10. 由结构不能推测出对应性质的是
A、氮氮键的键能: B、熔点: C、分子的极性: D、的键角:10. 由结构不能推测出对应性质的是选项
结构
性质
A
的VSEPR模型为平面三角形
具有氧化性
B
钾和钠的原子结构不同,电子跃迁时能量变化不同
钾和钠的焰色不同
C
乙烯和乙炔分子均含有键
两者均可发生加聚反应
D
石墨层中未参与杂化的p轨道中的电子,可在整个碳原子平面中运动
石墨具有类似金属的导电性
A、A B、B C、C D、D11. 是优良的固态电解质材料,取代部分后产生空位,可提升传导性能。取代后材料的晶胞结构示意图(未画出)及其作为电解质的电池装置如下。下列说法错误的是( ) A、每个晶胞中个数为12 B、该晶胞在yz平面的投影为
A、每个晶胞中个数为12 B、该晶胞在yz平面的投影为 C、取代后,该电解质的化学式为
D、若只有发生迁移,外电路转移的电子数与通过截面MNPQ的数目相等
12. 铜催化下,由电合成正丙醇的关键步骤如图。下列说法正确的是( )
C、取代后,该电解质的化学式为
D、若只有发生迁移,外电路转移的电子数与通过截面MNPQ的数目相等
12. 铜催化下,由电合成正丙醇的关键步骤如图。下列说法正确的是( ) A、Ⅰ到Ⅱ的过程中发生氧化反应 B、Ⅱ到Ⅲ的过程中有非极性键生成 C、Ⅳ的示意图为
A、Ⅰ到Ⅱ的过程中发生氧化反应 B、Ⅱ到Ⅲ的过程中有非极性键生成 C、Ⅳ的示意图为 D、催化剂Cu可降低反应热
13. 一定条件下,存在缺陷位的LiH晶体能吸附使其分解为N,随后N占据缺陷位(如图)。下列说法错误的是
D、催化剂Cu可降低反应热
13. 一定条件下,存在缺陷位的LiH晶体能吸附使其分解为N,随后N占据缺陷位(如图)。下列说法错误的是 A、 B、半径: C、 D、LiH晶体为离子晶体14. 从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符的是
A、 B、半径: C、 D、LiH晶体为离子晶体14. 从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符的是选项
实例
解释
A
原子光谱是不连续的线状谱线
原子的能级是量子化的
B
键角依次减小
孤电子对与成键电子对的斥力大于成键电子对之间的斥力
C
晶体中与8个配位,而晶体中与6个配位
比的半径大
D
逐个断开中的键,每步所需能量不同
各步中的键所处化学环境不同
A、A B、B C、C D、D15. 科学家合成了一种如图所示的纳米“分子客车”,能装载多种稠环芳香烃。三种芳烃与“分子客车”的结合常数(值越大越稳定)见表。下列说法错误的是
芳烃
芘
并四苯
蒄
结构



结合常数
385
3764
176000
A、芳烃与“分子客车”可通过分子间相互作用形成超分子 B、并四苯直立装载与平躺装载的稳定性基本相同 C、从分子大小适配看“分子客车”可装载2个芘 D、芳烃π电子数越多越有利于和“分子客车”的结合16. 阅读下列材料,完成问题。地球上的生物氮循环涉及多种含氮物质,转化关系之一如图所示(X、Y均为氮氧化物),羟胺(NH2OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与盐酸反应的产物盐酸羟胺([NH3OH]Cl)广泛用于药品、香料等的合成。
已知25℃时,Ka(HNO2)=7.2×10﹣4 , Kb(NH3•H2O)=1.8×10﹣5 , Kb(NH2OH)=8.7×10﹣9。
 (1)、NA是阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,2.24LX和Y混合气体中氧原子数为0.1NA B、1L0.1mol•L﹣1NaNO2溶液中Na+和
(1)、NA是阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,2.24LX和Y混合气体中氧原子数为0.1NA B、1L0.1mol•L﹣1NaNO2溶液中Na+和 数均为0.1NA
C、3.3gNH2OH完全转化为
数均为0.1NA
C、3.3gNH2OH完全转化为 时,转移的电子数为0.6NA
D、2.8gN2中含有的价电子总数为0.6NA
(2)、下列有关物质结构或性质的比较中,正确的是( )A、键角:NH3>
时,转移的电子数为0.6NA
D、2.8gN2中含有的价电子总数为0.6NA
(2)、下列有关物质结构或性质的比较中,正确的是( )A、键角:NH3> B、熔点:NH2OH>[NH3OH]Cl
C、25℃同浓度水溶液的pH:[NH3OH]Cl>NH4Cl
D、羟胺分子间氢键的强弱:O—H…O>N—H…N
17. 碘晶体为层状结构,层间作用为范德华力,层间距为.下图给出了碘的单层结构,层内碘分子间存在“卤键”(强度与氢键相近)NA.为阿伏加德罗常数的值.下列说法错误的是( )
B、熔点:NH2OH>[NH3OH]Cl
C、25℃同浓度水溶液的pH:[NH3OH]Cl>NH4Cl
D、羟胺分子间氢键的强弱:O—H…O>N—H…N
17. 碘晶体为层状结构,层间作用为范德华力,层间距为.下图给出了碘的单层结构,层内碘分子间存在“卤键”(强度与氢键相近)NA.为阿伏加德罗常数的值.下列说法错误的是( ) A、碘晶体是混合型晶体 B、液态碘单质中也存在“卤键” C、127g碘晶体中有个“卤键” D、碘晶体的密度为
A、碘晶体是混合型晶体 B、液态碘单质中也存在“卤键” C、127g碘晶体中有个“卤键” D、碘晶体的密度为二、填空题
-
18. 我国科研人员以高炉渣(主要成分为 , , 和等)为原料,对炼钢烟气(和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:

已知:
(1)、高炉渣与经焙烧产生的“气体”是。(2)、“滤渣”的主要成分是和。(3)、“水浸2”时主要反应的化学方程式为 , 该反应能进行的原因是。(4)、铝产品可用于。(5)、某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞底面显示为图丙,晶胞参数。图丙中与N的距离为;化合物的化学式是 , 其摩尔质量为 , 阿伏加德罗常数的值是 , 则晶体的密度为(列出计算表达式)。 19. 铁红是颜料,什么什么自古以来使用很多的……(题干缺失)。(1)、赭红的主要成分是_______。A、 B、 C、 D、(2)、饱和氯化铁溶液说法正确的是_______。A、常温显中性 B、加铁粉变红褐色 C、遇沸水后得到胶体 D、加氨水有白色沉淀(3)、有关铁原子说法正确的是_______。(不定项)A、有4个不同能级的电子 B、有5个未成对电子 C、占据15个原子轨道 D、有26种能量不同的电子(4)、加热试管中固体至红热,则_______。(不定项)
19. 铁红是颜料,什么什么自古以来使用很多的……(题干缺失)。(1)、赭红的主要成分是_______。A、 B、 C、 D、(2)、饱和氯化铁溶液说法正确的是_______。A、常温显中性 B、加铁粉变红褐色 C、遇沸水后得到胶体 D、加氨水有白色沉淀(3)、有关铁原子说法正确的是_______。(不定项)A、有4个不同能级的电子 B、有5个未成对电子 C、占据15个原子轨道 D、有26种能量不同的电子(4)、加热试管中固体至红热,则_______。(不定项)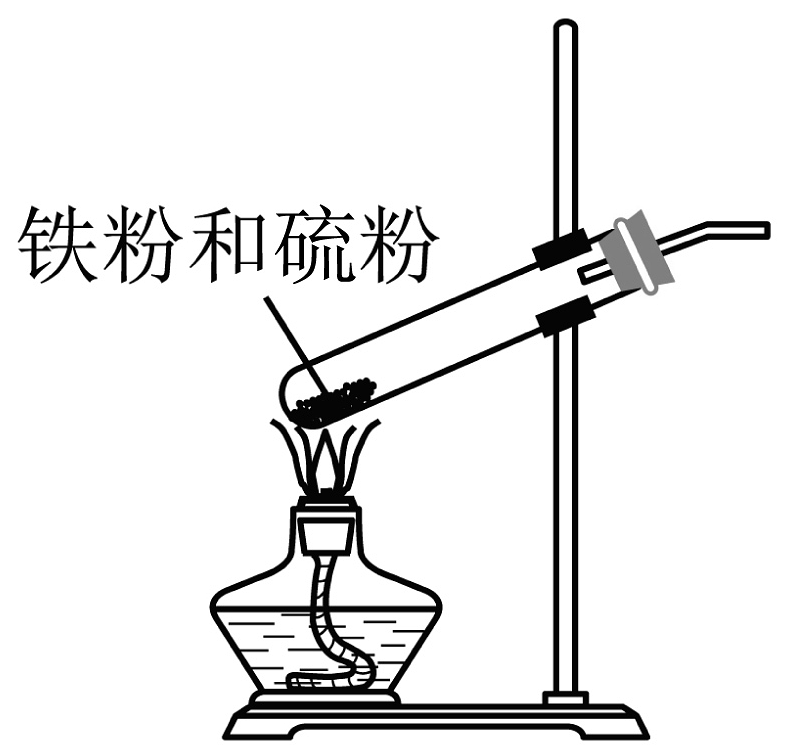 A、移开酒精灯后固体保持红热 B、S只做还原剂 C、主要产生的气体附产物为 D、最终得到黑色的(5)、内界为 , 配体有种(6)、 , 加水稀释至体积为原来的2倍,则。
A、移开酒精灯后固体保持红热 B、S只做还原剂 C、主要产生的气体附产物为 D、最终得到黑色的(5)、内界为 , 配体有种(6)、 , 加水稀释至体积为原来的2倍,则。A.增大 B.不变 C.减小
并用浓度商Q与平衡常数K的大小关系解释原因。
(7)、已知 , 求的分布系数。x
1
2
3
4
K
30.2
134.9
97.72
1.02
三、实验探究题
-
20. 银及其化合物在催化与电化学等领域中具有重要应用。
 (1)、在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图1所示,回答下列问题:
(1)、在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图1所示,回答下列问题:①中间体OMC生成吸附态EO(ads)的活化能为 kJ/mol。
②由EO(g)生成AA(g)的热化学方程式为 。
(2)、一定条件下,银催化剂表面上存在反应:Ag2O(s)⇌2Ag(s)+O2(g),该反应平衡压强pc与温度T的关系如表:T/K
401
443
463
pc/kPa
10
51
100
①463K时的平衡常数Kp=。
②起始状态Ⅰ中有Ag2O、Ag和O2 , 经图2过程达到各平衡状态:
已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是 (填字母)。
A.从Ⅰ到Ⅱ的过程ΔS>0
B.pc(Ⅱ)>pc(Ⅲ)
C.平衡常数:K(Ⅱ)>K(Ⅳ)
D.若体积V(Ⅲ)=2V(Ⅰ),则Q(Ⅰ)=K(Ⅲ)
E.逆反应的速率:v(Ⅰ)>v(Ⅱ)=v(Ⅲ)>v(Ⅳ)
③某温度下,向恒容容器中加入Ag2O,分解过程中反应速率v(O2) 与压强p的关系为v(O2)=k(1﹣),k为速率常数(定温下为常数)。当固体质量减少4%时,逆反应速率最大。若转化率为14.5%,则v(O2)=(用k表示)。
(3)、α﹣AgI可用作固体离子导体,能通过加热γ﹣AgI制得。上述两种晶体的晶胞示意图如图3所示(为了简化,只画出了碘离子在晶胞中的位置)。①测定晶体结构最常用的仪器是 (填字母)。
A.质谱仪
B.红外光谱仪
C.核磁共振仪
D.X射线衍射仪
②γ﹣AgI与α﹣AgI晶胞的体积之比为 。
③测定α﹣AgI中导电离子类型的实验装置如图4所示。实验测得支管a中AgI质量不变,可判定导电离子是Ag+而不是I﹣ , 依据是 。
四、综合题
-
21. 锰氧化物具有较大应用价值,回答下列问题:(1)、在元素周期表中位于第周期族;同周期中,基态原子未成对电子数比多的元素是(填元素符号)。(2)、如某种氧化物的四方晶胞及其在xy平面的投影如图所示,该氧化物化学式为。

当晶体有O原子脱出时,出现O空位,的化合价(填“升高”“降低”或“不变”),O空位的产生使晶体具有半导体性质。下列氧化物晶体难以通过该方式获有半导体性质的是(填标号)。
A. B. C. D.
(3)、(见图)是晶型转变的诱导剂。的空间构型为;中咪唑环存在大键,则N原子采取的轨道杂化方式为。 (4)、可作转化为的催化剂(见下图)。的熔点远大于 , 除相对分子质量存在差异外,另一重要原因是。
(4)、可作转化为的催化剂(见下图)。的熔点远大于 , 除相对分子质量存在差异外,另一重要原因是。 22. 以苯为代表的挥发性有机污染物可以在Co3O4的催化作用下,与O2反应生成CO2和H2O,进一步将CO2转化成高附加值的化学品,可减少污染和碳排放。
22. 以苯为代表的挥发性有机污染物可以在Co3O4的催化作用下,与O2反应生成CO2和H2O,进一步将CO2转化成高附加值的化学品,可减少污染和碳排放。Ⅰ.CO2与苯的分子结构
(1)、CO2分子中碳原子的杂化轨道类型为 , 苯是(填“极性”或“非极性”)分子。(2)、Ⅱ.苯的催化氧化Co3O4做催化剂时,在有、无光照条件下,苯的催化氧化产物相同,但反应历程不同。无光照条件下反应活化能为38 kJ/mol,有光照条件下反应活化能为26 kJ/mol。右图是290℃时,有、无光照条件下,苯的转化率随时间的变化曲线。

光照条件下,对应的转化率曲线为(填“a”或“b”)。
(3)、有、无光照条件下,两种反应历程的(填“相等”或“不等”)。(4)、Ⅲ.CO2的转化CO2与H2反应可以合成甲醇:
一定温度下,等物质的量的CO2和H2在恒容密闭容器中发生上述反应达到平衡后,下列各操作有利于平衡正向移动的是(填序号)。
a.分离出甲醇 b.充入稀有气体 c.增加H2量 d.降低温度
(5)、一定条件下,以CO2和CH3OH为原料制备HCOOH和甲酸盐,其装置原理如图。
①电极a是极,电极反应式为;
②电解过程中,电极b一侧的溶液pH将(填“升高”“不变”或“降低”);
③电解过程中通过阳离子交换膜的离子为。
23. 铜在自然界大多以硫化物形式成矿。请回答:
(1)、有关铜和硫的说法正确的是____A、基态硫原子有7对成对电子 B、铜焰色试验呈绿色,与铜原子核外电子跃迁释放能量有关 C、基态铜原子失去2个电子,3d轨道形成全充满结构 D、配位键强度:[Cu(NH3)]2+>[Cu(NH3)]+(2)、一种铜化合物的晶胞如图1,写出由配离子表示的该化合物的化学式 (3)、化合物A[化学式:(H2N)3PS]和B[化学式:(H2N)3PO]具有相似的结构,如图2。
(3)、化合物A[化学式:(H2N)3PS]和B[化学式:(H2N)3PO]具有相似的结构,如图2。
①化合物B给出H+趋势相对更大,请从结构角度分析原因
②将化合物A与足量稀硫酸混合,在加热条件下充分反应,得到气体C和含H3PO4的溶液,写出发生反应的化学方程式。
③设计实验检验气体C(要求利用气体C的氧化性或还原性)。
(4)、有同学以Cu3FeS4为原料,设计如下转化方案: ①步骤I的化学方程式
①步骤I的化学方程式②步骤I中,溶液E中铜元素全部转化为难溶性CuBr。气体X为(要求不引入其他新的元素);溶液F中除K+、H+、Br外,浓度最高的两种离子(按浓度由高到低顺序)。
五、流程题
-
24. 从褐铁矿型金-银矿(含Au、Ag、、、CuO、等)中提取Au、Ag,并回收其它有价金属的一种工艺如下:

已知:①金-银矿中Cu、Mn元素的含量分别为0.19%、2.35%。
②25℃时,的为。
回答下列问题:
(1)、基态Cu原子的价层电子排布式为。(2)、“还原酸浸”时,反应的离子方程式为。(3)、“浸金银”时,Au溶解涉及的主要反应如下:①
②
上述过程中的催化剂为。
(4)、“沉铜”前,“滤液1”多次循环的目的为。(5)、根据“还原酸浸”“氧化”,推断的氧化性由强到弱的顺序为。(6)、25℃“沉铁”后,调节“滤液4”的pH至8.0,无析出,则。(7)、一种锑锰合金的立方晶胞结构如图。
①该晶胞中,每个Sb周围与它最近且相等距离的Mn有个。
②为阿伏加德罗常数的值,晶胞边长为anm,则晶体的密度为(列出计算式即可)。
25. 可用于制备光学材料和回收砷。(1)、制备。由闪锌矿[含及少量硫化镉等]制备的过程如下:
已知:。当离子浓度小于时,认为离子沉淀完全。
①酸浸时通入可提高浸出率的原因是。
②通入除镉。通过计算判断当溶液时,是否沉淀完全(写出计算过程)。
③沉锌前调节溶液的至 , 加入的氧化物为(填化学式)。
(2)、制备光学材料。如图甲所示,晶体中掺入少量后,会出现能量不同的“正电”区域、“负电”区域,光照下发出特定波长的光。
区域A“
 ”中的离子为(填离子符号),区域B带(填“正电”或“负电”)。(3)、回收砷。用去除酸性废液中的三价砷 , 并回收生成的沉淀。
”中的离子为(填离子符号),区域B带(填“正电”或“负电”)。(3)、回收砷。用去除酸性废液中的三价砷 , 并回收生成的沉淀。已知:溶液中主要以弱酸形式存在,。
时,按向酸性废液中加入 , 砷回收率随反应时间的变化如图乙所示。

①写出与反应生成的离子方程式:。
②反应后,砷回收率下降的原因有。
-