备考2026届高考 2021-2025全国各地真题汇编 专题8 化学反应与电能
试卷更新日期:2026-04-25 类型:二轮复习
一、选择题
-
1. 2024年5月8日,我国第三艘航空母舰福建舰顺利完成首次海试。舰体表面需要采取有效的防锈措施,下列防锈措施中不形成表面钝化膜的是A、发蓝处理 B、阳极氧化 C、表面渗镀 D、喷涂油漆2. 近年来,我国新能源产业得到了蓬勃发展,下列说法错误的是( )A、理想的新能源应具有资源丰富、可再生、对环境无污染等特点 B、氢氧燃料电池具有能量转化率高、清洁等优点 C、锂离子电池放电时锂离子从负极脱嵌,充电时锂离子从正极脱嵌 D、太阳能电池是一种将化学能转化为电能的装置3. 通过电化学方法制备Br,进而由Br,与
 反应合成
反应合成 为提高电流利用效率,某小组设计电化学合成示意图如下,已知氧化性:H2O2>Br。下列说法不正确的是( )
为提高电流利用效率,某小组设计电化学合成示意图如下,已知氧化性:H2O2>Br。下列说法不正确的是( ) A、电极A与电源正极相连 B、电极B的电极反应式为:O2+ 2H++ 2e2-=H2O2 C、电解液中 H2SO4可以用氢溴酸代替 D、原料足量的情况下,理论上电路中转移0.2mole可得到0.1mol
A、电极A与电源正极相连 B、电极B的电极反应式为:O2+ 2H++ 2e2-=H2O2 C、电解液中 H2SO4可以用氢溴酸代替 D、原料足量的情况下,理论上电路中转移0.2mole可得到0.1mol 4. 某电池的正极材料为 , 负极材料为嵌锂石墨。利用人工智能筛选出的补锂试剂 , 能使失活的电池再生并延长寿命,且保持电池原结构。将注入电池后充电补锂,过程中转化为气体离去。下列有关充电补锂的说法错误的是( )A、在阳极失去电子 B、生成气体中含有氟代烃 C、过程中铁元素的价态降低 D、反应并离去是该电池保持原结构的原因5. 关于如图所示的装置,下列说法错误的是( )
4. 某电池的正极材料为 , 负极材料为嵌锂石墨。利用人工智能筛选出的补锂试剂 , 能使失活的电池再生并延长寿命,且保持电池原结构。将注入电池后充电补锂,过程中转化为气体离去。下列有关充电补锂的说法错误的是( )A、在阳极失去电子 B、生成气体中含有氟代烃 C、过程中铁元素的价态降低 D、反应并离去是该电池保持原结构的原因5. 关于如图所示的装置,下列说法错误的是( ) A、该装置将化学能转化为电能 B、是负极,发生反应 C、向电极附近迁移 D、若将装置中的换为 , 则为负极6. 一种可充放电电池的结构示意图如图所示。该电池放电时,产物为和 , 随温度升高Q(消耗转移的电子数)增大。下列说法不正确的是
A、该装置将化学能转化为电能 B、是负极,发生反应 C、向电极附近迁移 D、若将装置中的换为 , 则为负极6. 一种可充放电电池的结构示意图如图所示。该电池放电时,产物为和 , 随温度升高Q(消耗转移的电子数)增大。下列说法不正确的是 A、熔融盐中的物质的量分数影响充放电速率 B、充放电时,优先于通过固态电解质膜 C、放电时,随温度升高Q增大,是因为正极区转化为 D、充电时,锂电极接电源负极7. 我国科技工作者设计了如图所示的可充电电池,以为电解质,电解液中加入1,3-丙二胺()以捕获 , 使放电时还原产物为。该设计克服了导电性差和释放能力差的障碍,同时改善了的溶剂化环境,提高了电池充放电循环性能。
A、熔融盐中的物质的量分数影响充放电速率 B、充放电时,优先于通过固态电解质膜 C、放电时,随温度升高Q增大,是因为正极区转化为 D、充电时,锂电极接电源负极7. 我国科技工作者设计了如图所示的可充电电池,以为电解质,电解液中加入1,3-丙二胺()以捕获 , 使放电时还原产物为。该设计克服了导电性差和释放能力差的障碍,同时改善了的溶剂化环境,提高了电池充放电循环性能。
回答下列问题。
(1)、下列说法错误的是A、放电时,电池总反应为 B、充电时,多孔碳纳米管电极与电源正极连接 C、充电时,电子由电极流向阳极,向阴极迁移 D、放电时,每转移电子,理论上可转化(2)、对上述电池放电时的捕获和转化过程开展了进一步研究,电极上转化的三种可能反应路径及相对能量变化如图(*表示吸附态)。
下列说法错误的是
A、捕获的反应为 B、路径2是优先路径,速控步骤反应式为
B、路径2是优先路径,速控步骤反应式为 C、路径1、3经历不同的反应步骤但产物相同;路径2、3起始物相同但产物不同
D、三个路径速控步骤均涉及转化,路径2、3的速控步骤均伴有再生
8. 破损的镀锌铁皮在氨水中发生电化学腐蚀,生成[Zn(NH3)4]2+和H2 , 下列说法不正确的是( )A、氨水浓度越大,腐蚀趋势越大 B、随着腐蚀的进行,溶液pH变大 C、铁电极上的电极反应式为:2NH3+2e﹣═2+H2↑ D、每生成标准状况下224mLH2 , 消耗0.010molZn9. 下列有关电极方程式或离子方程式错误的是A、碱性锌锰电池的正极反应:MnO2+H2O+e-=MnO(OH)+OH- B、铅酸蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO2+4H+ C、K3[Fe(CN)6]溶液滴入FeCl2溶液中:K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓ D、TiCl4加入水中:TiCl4+(x+2)H2O=TiO2·xH2O↓+4H++4Cl-10. 金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有关。下图为两种对海水中钢闸门的防腐措施示意图:
C、路径1、3经历不同的反应步骤但产物相同;路径2、3起始物相同但产物不同
D、三个路径速控步骤均涉及转化,路径2、3的速控步骤均伴有再生
8. 破损的镀锌铁皮在氨水中发生电化学腐蚀,生成[Zn(NH3)4]2+和H2 , 下列说法不正确的是( )A、氨水浓度越大,腐蚀趋势越大 B、随着腐蚀的进行,溶液pH变大 C、铁电极上的电极反应式为:2NH3+2e﹣═2+H2↑ D、每生成标准状况下224mLH2 , 消耗0.010molZn9. 下列有关电极方程式或离子方程式错误的是A、碱性锌锰电池的正极反应:MnO2+H2O+e-=MnO(OH)+OH- B、铅酸蓄电池充电时的阳极反应:Pb2++2H2O-2e-=PbO2+4H+ C、K3[Fe(CN)6]溶液滴入FeCl2溶液中:K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓ D、TiCl4加入水中:TiCl4+(x+2)H2O=TiO2·xH2O↓+4H++4Cl-10. 金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有关。下图为两种对海水中钢闸门的防腐措施示意图:
图1 图2
下列说法正确的是
A、图1、图2中,阳极材料本身均失去电子 B、图2中,外加电压偏高时,钢闸门表面可发生反应:O2+4e−+2H2O=4OH− C、图2中,外加电压保持恒定不变,有利于提高对钢闸门的防护效果 D、图1、图2中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应11. 葡萄糖酸钙是一种重要的补钙剂,工业上以葡萄糖、碳酸钙为原料,在溴化钠溶液中采用间接电氧化反应制备葡萄糖酸钙,其阳极区反应过程如下:
下列说法错误的是
A、溴化钠起催化和导电作用 B、每生成葡萄糖酸钙,理论上电路中转移了电子 C、葡萄糖酸能通过分子内反应生成含有六元环状结构的产物 D、葡萄糖能发生氧化、还原、取代、加成和消去反应12. 如图,c管为上端封口的量气管,为测定乙酸溶液浓度,量取待测样品加入b容器中,接通电源,进行实验。下列说法正确的是( )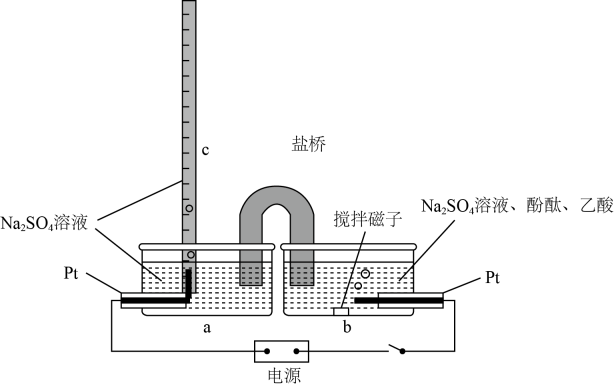 A、左侧电极反应: B、实验结束时,b中溶液红色恰好褪去 C、若c中收集气体 , 则样品中乙酸浓度为 D、把盐桥换为U形铜导线,不影响测定结果13. 利用活性石墨电极电解饱和食盐水,进行如图所示实验。闭合 , 一段时间后( )
A、左侧电极反应: B、实验结束时,b中溶液红色恰好褪去 C、若c中收集气体 , 则样品中乙酸浓度为 D、把盐桥换为U形铜导线,不影响测定结果13. 利用活性石墨电极电解饱和食盐水,进行如图所示实验。闭合 , 一段时间后( )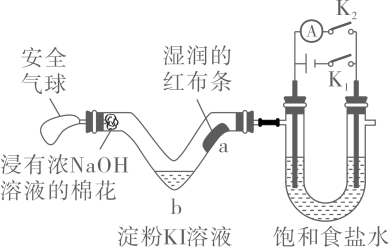 A、U型管两侧均有气泡冒出,分别是和 B、a处布条褪色,说明具有漂白性 C、b处出现蓝色,说明还原性: D、断开 , 立刻闭合 , 电流表发生偏转14. 某理论研究认为:燃料电池(图b)的电极Ⅰ和Ⅱ上所发生反应的催化机理示意图分别如图a和图c,其中获得第一个电子的过程最慢。由此可知,理论上
A、U型管两侧均有气泡冒出,分别是和 B、a处布条褪色,说明具有漂白性 C、b处出现蓝色,说明还原性: D、断开 , 立刻闭合 , 电流表发生偏转14. 某理论研究认为:燃料电池(图b)的电极Ⅰ和Ⅱ上所发生反应的催化机理示意图分别如图a和图c,其中获得第一个电子的过程最慢。由此可知,理论上 A、负极反应的催化剂是ⅰ B、图a中,ⅰ到ⅱ过程的活化能一定最低 C、电池工作过程中,负极室的溶液质量保持不变 D、相同时间内,电极Ⅰ和电极Ⅱ上的催化循环完成次数相同15. 我国科研人员采用图示的电解池,由百里酚(TY)合成了百里醌(TQ)。电极b表面的主要反应历程见图(灰球表示电极表面催化剂),下列说法错误的是( )
A、负极反应的催化剂是ⅰ B、图a中,ⅰ到ⅱ过程的活化能一定最低 C、电池工作过程中,负极室的溶液质量保持不变 D、相同时间内,电极Ⅰ和电极Ⅱ上的催化循环完成次数相同15. 我国科研人员采用图示的电解池,由百里酚(TY)合成了百里醌(TQ)。电极b表面的主要反应历程见图(灰球表示电极表面催化剂),下列说法错误的是( ) A、电解时,从右室向左室移动 B、电解总反应: C、以
A、电解时,从右室向左室移动 B、电解总反应: C、以 为原料,也可得到TQ
D、用标记电解液中的水,可得到
为原料,也可得到TQ
D、用标记电解液中的水,可得到
二、实验探究题
-
16. 资料显示,可以将氧化为。某小组同学设计实验探究被氧化的产物及铜元素的价态。
已知:易溶于溶液,发生反应红棕色;和氧化性几乎相同。
(1)、将等体积的溶液加入到铜粉和的固体混合物中,振荡。实验记录如下:
实验现象
实验Ⅰ
极少量溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色
实验Ⅱ
部分溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色
实验Ⅲ
完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色
初始阶段,被氧化的反应速率:实验Ⅰ填“”“”或“”实验Ⅱ。
实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有蓝色或无色 , 进行以下实验探究:
步骤取实验Ⅲ的深红棕色溶液,加入 , 多次萃取、分液。
步骤取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
步骤的目的是。
查阅资料, , 无色容易被空气氧化。用离子方程式解释步骤的溶液中发生的变化:。
结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是 , 实验Ⅰ中铜被氧化的化学方程式是。分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入浓溶液,填实验现象 , 观察到少量红色的铜。分析铜未完全反应的原因是。
(2)、上述实验结果,仅将氧化为价。在隔绝空气的条件下进行电化学实验,证实了能将氧化为。装置如图所示,分别是。 (3)、运用氧化还原反应规律,分析在上述实验中被氧化的产物中价态不同的原因:。17. 铅酸电池是用途广泛并不断发展的化学电源。(1)、十九世纪,铅酸电池工作原理初步形成并延续至今。
(3)、运用氧化还原反应规律,分析在上述实验中被氧化的产物中价态不同的原因:。17. 铅酸电池是用途广泛并不断发展的化学电源。(1)、十九世纪,铅酸电池工作原理初步形成并延续至今。铅酸电池工作原理:
①充电时,阴极发生的电极反应为。
②放电时,产生a库仑电量,消耗的物质的量为。已知:转移电子所产生的电量为96500库仑。
③作为电解质溶液性质稳定、有较强的导电能力,参与电极反应并有利于保持电压稳定。该体系中不氧化 , 氧化性弱与其结构有关,的空间结构是。
④铅酸电池储存过程中,存在化学能的缓慢消耗:电极在作用下产生的可将电极氧化。氧化发生反应的化学方程式为。
(2)、随着铅酸电池广泛应用,需要回收废旧电池材料,实现资源的再利用。回收过程中主要物质的转化关系示意图如下。
①将等物质转化为的过程中,步骤I加入溶液的目的是。
②步骤Ⅱ、Ⅲ中和作用分别是。
(3)、铅酸电池使用过程中,负极因生成导电性差的大颗粒 , 导致电极逐渐失活。通过向负极添加石墨、多孔碳等碳材料,可提高铅酸电池性能。碳材料的作用有(填序号)。a.增强负极导电性
b.增大负极材料比表面积,利于生成小颗粒
c.碳材料作还原剂,使被还原
18. 环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。  (1)、①阳极室产生Cl2后发生的反应有:、CH2=CH2+HClO→HOCH2CH2Cl。
(1)、①阳极室产生Cl2后发生的反应有:、CH2=CH2+HClO→HOCH2CH2Cl。②结合电极反应式说明生成溶液a的原理。
(2)、一定条件下,反应物按一定流速通过该装置。电解效率η和选择性S的定义:
η(B)= ×100%
S(B)= ×100%
①若η(EO)=100%,则溶液b的溶质为。
②当乙烯完全消耗时,测得η(EO)≈70%,S(EO)≈97%,推测η(EO)≈70%的原因:
I.阳极有H2O放电
II.阳极有乙烯放电
III.阳极室流出液中含有Cl2和HClO
……
i.检验电解产物,推测I不成立。需要检验的物质是。
ii.假设没有生成EO的乙烯全部在阳极放电生成CO2 , η(CO2)≈%。经检验阳极放电产物没有CO2。
iii.实验证实推测III成立,所用试剂及现象是。
可选试剂:AgNO3溶液、KI溶液、淀粉溶液、品红溶液。
三、综合题
-
19. 空气中含量的控制和资源利用具有重要意义。(1)、燃煤烟气中的捕集可通过如下所示的物质转化实现。

“吸收”后所得的溶液与石灰乳反应的化学方程式为;载人航天器内,常用LiOH固体而很少用KOH固体吸收空气中的 , 其原因是。
(2)、合成尿素[]是利用的途径之一、尿素合成主要通过下列反应实现反应Ⅰ:
反应Ⅱ:
①密闭体系中反应Ⅰ的平衡常数(K)与温度的关系如图甲所示,反应Ⅰ的(填“=0”或“>0”或“<0”)。

②反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[]和尿素转化为氰酸铵()等副反应。尿素生产中实际投入和的物质的量之比为 , 其实际投料比值远大于理论值的原因是。
(3)、催化电解吸收的KOH溶液可将转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率()随电解电压的变化如图乙所示。
其中, , n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为时,电解过程中含碳还原产物的为0,阴极主要还原产物为(填化学式)。
②当电解电压为时,阴极由生成的电极反应式为。
③当电解电压为时,电解生成的和的物质的量之比为(写出计算过程)。
20. 水是重要的生活资源,根据题意回答下列问题。(1)、天然水中提纯得到重水,重水中存在电离平衡 , 其图像如图,回答下列问题: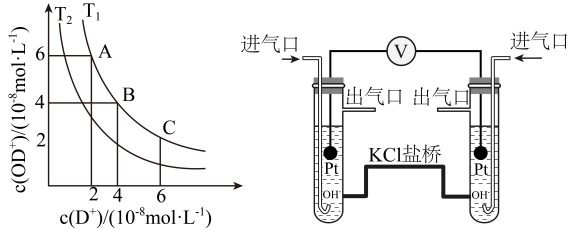
①“A、B、C”三点中呈中性的是。
②(填写“>”“<”或者“=”)
(2)、有如右图所示原电池,回答下列问题:①用进行实验,左侧通入 , 产物为 , 盐桥中移向(填“左侧”或者“右侧”),总反应方程式为。
②用进行实验,一侧通入 , 电池总反应方程式不变,该侧的电极反应方程式为。
(3)、利用驰豫法可研究快捷反应的速率常数(k在一定温度下为常数),其原理是通过微扰(如瞬时升温)使化学平衡发生偏离,观测体系微扰后从不平衡态趋向新平衡态所需的驰豫时间 , 从而获得k的信息对于若将纯水瞬时升温到25℃,测得。已知:25℃时, , , , (为的平衡浓度)。
①25℃时, , 的平衡常数(保留2位有效数字)。
②下列能正确表示瞬时升温后反应建立新平衡的过程示意图为。
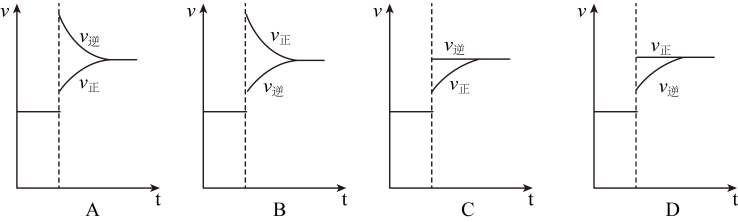
③25℃时,计算得为
21. 通过电化学、热化学等方法,将CO2转化为HCOOH等化学品,是实现“双碳”目标的途径之一。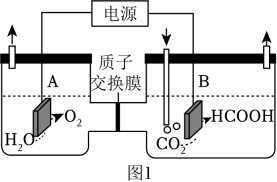
请回答:
(1)、某研究小组采用电化学方法将CO2转化为HCOOH,装置如图1。电极B上的电极反应式是 。(2)、该研究小组改用热化学方法,相关热化学方程式如下:Ⅰ:C(s)+O2(g)═CO2(g)
ΔH1=﹣393.5kJ•mol﹣1
Ⅱ:C(s)+H2(g)+O2(g)═HCOOH(g)
ΔH2=﹣378.7kJ•mol﹣1
Ⅲ:CO2(g)+H2(g)⇌HCOOH(g)
ΔH3
①ΔH3=kJ•mol﹣1。
②反应Ⅲ在恒温、恒容的密闭容器中进行,CO2和H2的投料浓度均为1.0mol•L﹣1 , 平衡常数K=2.4×10﹣8 , 则CO2的平衡转化率为 。
③用氨水吸收HCOOH,得到1.00mol•L﹣1氨水和0.18mol•L﹣1甲酸铵的混合溶液,298K时该混合溶液的pH=。[已知:298K时,电离常数Kb(NH3•H2O)=1.8×10﹣5、Ka(HCOOH)=1.8×10﹣4]
(3)、为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂M的DMSO(有机溶剂)溶液,CO2和H2在溶液中反应制备HCOOH,反应过程中保持CO2(g)和H2(g)的压强不变,总反应CO2+H2⇌HCOOH的反应速率为v,反应机理如下列三个基元反应,各反应的活化能E2<E1<<E3(不考虑催化剂活性降低或丧失)。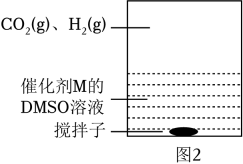
Ⅳ:M+CO2⇌Q
E1
Ⅴ:Q+H2⇌L
E2
Ⅴ:L⇌M+HCOOH
E3
①催化剂M足量条件下,下列说法正确的是 ____。
A、v与CO2(g)的压强无关 B、v与溶液中溶解H2的浓度无关 C、温度升高,v不一定增大 D、在溶液中加入N(CH2CH3)3 , 可提高CO2转化率(4)、②实验测得:298K,p(CO2)=p(H2)=2MPa下,v随催化剂M浓度c变化如图3。c⩽c0时,v随c增大而增大:c>c0时,v不再显著增大。请解释原因。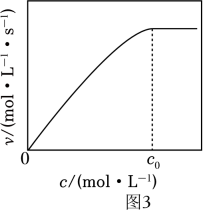 22. 反应在工业上有重要应用。(1)、该反应在不同温度下的平衡常数如表所示。
22. 反应在工业上有重要应用。(1)、该反应在不同温度下的平衡常数如表所示。温度/℃
700
800
830
1000
平衡常数
1.67
1.11
1.00
0.59
①反应的△H0(填“>”“<”或“=”)。
②反应常在较高温度下进行,该措施的优缺点是。
(2)、该反应常在Pd膜反应器中进行,其工作原理如图所示。
①利用平衡移动原理解释反应器存在Pd膜时具有更高转化率的原因是。
②某温度下,H2在Pd膜表面上的解离过程存在如下平衡: , 其正反应的活化能远小于逆反应的活化能。下列说法错误的是。
A.Pd膜对气体分子的透过具有选择性
B.过程2的△H>0
C.加快Pd膜内H原子迁移有利于H2的解离
D.H原子在Pd膜表面上结合为H2的过程为放热反应
③同温同压下,等物质的量的CO和H2O通入无Pd膜反应器,CO的平衡转化率为75%;若换成Pd膜反应器,CO的平衡转化率为90%,则相同时间内出口a和出口b中H2的质量比为。
(3)、该反应也可采用电化学方法实现,反应装置如图所示。
①固体电解质采用(填“氧离子导体”或“质子导体”)。
②阴极的电极反应式为。
③同温同压下,相同时间内,若进口Ⅰ处n(CO):n(H2O)=a:b,出口Ⅰ处气体体积为进口Ⅰ处的y倍,则CO的转化率为(用a,b,y表示)。
四、流程题
-
23. 根据下列有机流程,回答有关问题
 (1)、化合物G中含有的官能团为 。(2)、A→B的反应类型是 。(3)、化合物A满足下列条件的同分异构体有 种,其中核磁共振氢谱图像为4组峰的结构简式为 。
(1)、化合物G中含有的官能团为 。(2)、A→B的反应类型是 。(3)、化合物A满足下列条件的同分异构体有 种,其中核磁共振氢谱图像为4组峰的结构简式为 。①可以发生银镜反应。
②含有苯环。
(4)、B→C的反应方程式为 。(5)、C→D的所需试剂与反应条件为 。(6)、下列关于化合物E的说法,错误的是 。a.可以发生聚合反应
b.所有9个碳原子共平面
c.可以形成分子内、分子间氢键
d.含有一个手性碳原子
(7)、电催化过程中,二氧化碳与物质D的反应应当在 (填“阳极”或“阴极”)进行。(8)、根据上述信息,补齐下列反应流程: 24. 超纯是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯方面取得了显著成果,工业上以粗镓为原料,制备超纯的工艺流程如下:
24. 超纯是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯方面取得了显著成果,工业上以粗镓为原料,制备超纯的工艺流程如下:
已知:①金属的化学性质和相似,的熔点为;
②(乙醚)和(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
物质
沸点/
55.7
34.6
42.4
365.8
回答下列问题:
(1)、晶体的晶体类型是;(2)、“电解精炼”装置如图所示,电解池温度控制在的原因是 , 阴极的电极反应式为; (3)、“合成”工序中的产物还包括和 , 写出该反应的化学方程式:;(4)、“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是;(5)、下列说法错误的是____;A、流程中得到了循环利用 B、流程中,“合成”至“工序X”需在无水无氧的条件下进行 C、“工序X”的作用是解配 , 并蒸出 D、用核磁共振氢谱不能区分和(6)、直接分解不能制备超纯 , 而本流程采用“配体交换”工艺制备超纯的理由是;(7)、比较分子中的键角大小:(填“>”“<”或“=”),其原因是。
(3)、“合成”工序中的产物还包括和 , 写出该反应的化学方程式:;(4)、“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是;(5)、下列说法错误的是____;A、流程中得到了循环利用 B、流程中,“合成”至“工序X”需在无水无氧的条件下进行 C、“工序X”的作用是解配 , 并蒸出 D、用核磁共振氢谱不能区分和(6)、直接分解不能制备超纯 , 而本流程采用“配体交换”工艺制备超纯的理由是;(7)、比较分子中的键角大小:(填“>”“<”或“=”),其原因是。