备考2026届高考 2021-2025全国各地真题汇编 专题7 化学反应的热效应
试卷更新日期:2026-04-25 类型:二轮复习
一、选择题
-
1. 右图是简易量热计装置示意图,下列反应的反应热不适宜用该装置测定的是( )
 A、BaO和足量的水 B、Al和足量的NaOH溶液 C、ZnO和足量的稀硫酸 D、KOH溶液和足量的稀盐酸2. 下列说法不正确的是( )A、葡萄糖氧化生成和的反应是放热反应 B、核酸可看作磷酸、戊糖和碱基通过一定方式结合而成的生物大分子 C、由氨基乙酸形成的二肽中存在两个氨基和两个羧基 D、向饱和的溶液中加入少量鸡蛋清溶液会发生盐析3. 下列反应均能自发进行,相关判断不正确的是( )
A、BaO和足量的水 B、Al和足量的NaOH溶液 C、ZnO和足量的稀硫酸 D、KOH溶液和足量的稀盐酸2. 下列说法不正确的是( )A、葡萄糖氧化生成和的反应是放热反应 B、核酸可看作磷酸、戊糖和碱基通过一定方式结合而成的生物大分子 C、由氨基乙酸形成的二肽中存在两个氨基和两个羧基 D、向饱和的溶液中加入少量鸡蛋清溶液会发生盐析3. 下列反应均能自发进行,相关判断不正确的是( )H2SO4(l) + Fe(OH)2(s) = FeSO4(s) + 2H,O(I) △H1
H2SO4(l)+ 2NaOH(s)= Na2SO4(s)+ 2H2O(I) △H2
H2SO4(l)+ Na2O(s) = Na2SO4(s) + H2O(I) △H3
SO3(g) + Na2O(s) = Na2SO4(s) △H4
SO3(g) + H2O(I)= H2SO4(I) △H5
A、△H1-△H2>0 B、△H2-△H3>0 C、△H3-△H4<O D、△H4 , -△H5<04. 为理解离子化合物溶解过程的能量变化,可设想固体溶于水的过程分两步实现,示意图如下。
下列说法不正确的是( )
A、固体溶解是吸热过程 B、根据盖斯定律可知: C、根据各微粒的状态,可判断 , D、溶解过程的能量变化,与固体和溶液中微粒间作用力的强弱有关5. 一定条件下,石墨转化为金刚石反应过程的能量变化如图所示,下列说法正确的是( ) A、该反应为放热反应 B、石墨和金刚石互为同位素 C、反应中涉及化学键的断裂和形成 D、反应物的总能量大于生成物的总能量6. 下列说法正确的是A、常温常压下和混合无明显现象,则反应在该条件下不自发 B、 , 升高温度,平衡逆移,则反应的平衡常数减小 C、 , 则正反应的活化能大于逆反应的活化能 D、 , 则7. 按下图装置进行实验。搅拌一段时间后,滴加浓盐酸。不同反应阶段的预期现象及其相应推理均合理的是( )
A、该反应为放热反应 B、石墨和金刚石互为同位素 C、反应中涉及化学键的断裂和形成 D、反应物的总能量大于生成物的总能量6. 下列说法正确的是A、常温常压下和混合无明显现象,则反应在该条件下不自发 B、 , 升高温度,平衡逆移,则反应的平衡常数减小 C、 , 则正反应的活化能大于逆反应的活化能 D、 , 则7. 按下图装置进行实验。搅拌一段时间后,滴加浓盐酸。不同反应阶段的预期现象及其相应推理均合理的是( ) A、烧瓶壁会变冷,说明存在的反应 B、试纸会变蓝,说明有生成,产氨过程熵增 C、滴加浓盐酸后,有白烟产生,说明有升华 D、实验过程中,气球会一直变大,说明体系压强增大8. 某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g)⇌Y(g)(ΔH1<0),Y(g)⇌Z(g)(ΔH2<0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的是( )
A、烧瓶壁会变冷,说明存在的反应 B、试纸会变蓝,说明有生成,产氨过程熵增 C、滴加浓盐酸后,有白烟产生,说明有升华 D、实验过程中,气球会一直变大,说明体系压强增大8. 某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g)⇌Y(g)(ΔH1<0),Y(g)⇌Z(g)(ΔH2<0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的是( ) A、
A、 B、
B、 C、
C、 D、
D、 9. 下列实验能达到目的的是( )
9. 下列实验能达到目的的是( )实验目的
实验方法或操作
A
测定中和反应的反应热
酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温度
B
探究浓度对化学反应速率的影响
量取同体积不同浓度的溶液,分别加入等体积等浓度的溶液,对比现象
C
判断反应后是否沉淀完全
将溶液与溶液混合,反应后静置,向上层清液中再加1滴溶液
D
检验淀粉是否发生了水解
向淀粉水解液中加入碘水
A、A B、B C、C D、D10. 已知共价键的键能与热化学方程式信息如下表:共价键
H- H
H-O
键能/(kJ·mol-1)
436
463
热化学方程式
2H2(g) + O2 (g)=2H2O(g) ΔH= -482kJ·mol-1
则2O(g)=O2(g)的ΔH为( )
A、428 kJ·mol-1 B、-428 kJ·mol-1 C、498 kJ·mol-1 D、-498 kJ·mol-111. AgCN与可发生取代反应,反应过程中的C原子和N原子均可进攻 , 分别生成腈和异腈两种产物。通过量子化学计算得到的反应历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是
A、从生成和的反应都是放热反应 B、过渡态TS1是由的C原子进攻的而形成的 C、Ⅰ中“”之间的作用力比Ⅱ中“”之间的作用力弱 D、生成放热更多,低温时是主要产物12. 恒容密闭容器中, 在不同温度下达平衡时,各组分的物质的量(n)如图所示。下列说法正确的是( )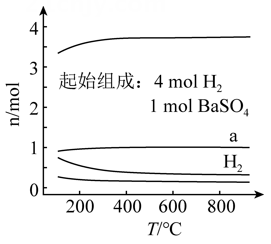 A、该反应的 B、a为 随温度的变化曲线 C、向平衡体系中充入惰性气体,平衡不移动 D、向平衡体系中加入 的平衡转化率增大13. 相关有机物分别与氢气发生加成反应生成1mol环己烷(
A、该反应的 B、a为 随温度的变化曲线 C、向平衡体系中充入惰性气体,平衡不移动 D、向平衡体系中加入 的平衡转化率增大13. 相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图所示:
)的能量变化如图所示:
下列推理不正确的是( )
A、2ΔH1≈ΔH2 , 说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比 B、ΔH2<ΔH3 , 说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定 C、3ΔH1<ΔH4 , 说明苯分子中不存在三个完全独立的碳碳双键 D、ΔH3-ΔH1<0,ΔH4-ΔH3>0,说明苯分子具有特殊稳定性14. Li电池使用过程中会产生LiH,对电池的性能和安全性带来影响。可用D2O与LiH进行反应测定LiH含量,由产物中的n(D2)/n(HD)比例可推算n(Li)/n(LiH)。已知:①2LiH⇌2Li+H2 △H>0
②LiH+H2O=LiOH+H2↑
下列说法错误的是( )
A、H2O、D2O的化学性质基本相同 B、Li与D2O反应的方程式是2Li+2D2O=2LiOD+D2↑ C、n(D2)/n(HD)比例小说明n(Li)/n(LiH)比例大 D、80℃下的n(D2)/n(HD)大于25℃下的n(D2)/n(HD)15. 在密闭容器中发生反应:2A(g)+B(g)⇌2C(g),往密闭容器中以n(A):n(B)=2:1通入两种反应物,15min后A在四温度下的转化率如下表所示,且T1<T2<T3<T4 , 下列说法正确的是( )温度
T1
T2
T3
T4
转化率
10%
70%
70%
60%
A、该反应是吸热反应 B、T温度时(T2<T<T3),A的转化率是70% C、T3温度下,若反应在15min后继续进行,则A的转化率变大 D、T4温度反应15min后,若c(B)=0.5mol•L﹣1 , 则T4温度时的平衡常数是4.5二、实验探究题
-
16. 粉末可在较低温度下还原。回答下列问题:(1)、已知一定温度下:
则的(用m和n表示)。
(2)、图1分别是和下还原过程中反应体系电阻随反应时间变化的曲线,可用(填标号)表示反应的快慢。
a. b. c. d.
(3)、图1中曲线(填“Ⅰ”“Ⅱ”或“Ⅲ”)对应的反应温度最高。(4)、研究发现对的还原性主要来自于其产生的。一般认为在表面被氧化成有两种可能途径,图2是理论计算得到的相对能量变化图,据此推测途径(填“a”或“b”)是主要途径。 (5)、产生的可能反应:①或②。将放在含微量水的气流中,在至的升温过程中固体质量一直增加,由此可断定的来源之一是反应(填“①”或“②”)。若要判断另一个反应是否是的来源,必须进行的实验是。(6)、已知。研究表明,在相同温度下,用还原比直接用还原更有优势,从平衡移动原理角度解释原因:。17. 合成气(和)是重要的工业原料气。(1)、合成气制备甲醇:。的结构式为 , 估算该反应的需要(填数字)种化学键的键能数据。(2)、合成气经“变换”“脱碳”获得纯。
(5)、产生的可能反应:①或②。将放在含微量水的气流中,在至的升温过程中固体质量一直增加,由此可断定的来源之一是反应(填“①”或“②”)。若要判断另一个反应是否是的来源,必须进行的实验是。(6)、已知。研究表明,在相同温度下,用还原比直接用还原更有优势,从平衡移动原理角度解释原因:。17. 合成气(和)是重要的工业原料气。(1)、合成气制备甲醇:。的结构式为 , 估算该反应的需要(填数字)种化学键的键能数据。(2)、合成气经“变换”“脱碳”获得纯。①合成气变换。向绝热反应器中通入和过量的:
催化作用受接触面积和温度等因素影响,的比热容较大。过量能有效防止催化剂活性下降,其原因有。
②脱碳在钢制吸收塔中进行,吸收液成分:质量分数30%的吸收剂、(正价有)缓蚀剂等。溶液浓度偏高会堵塞设备,导致堵塞的物质是(填化学式)。减缓设备腐蚀的原理是。
(3)、研究与不同配比的铁铈载氧体[是活泼金属,正价有]反应,气体分步制备原理示意如图甲所示。相同条件下,先后以一定流速通入固定体积的 , 依次发生的主要反应:步骤Ⅰ
步骤Ⅱ
①步骤Ⅰ中,产物气体积分数、转化率、与x的关系如图乙所示。时,大于理论值2的可能原因有;时,通入标准状况下的至反应结束,的选择性 , 则生成标准状况下和的总体积为。


②时,新制载氧体、与反应后的载氧体的X射线衍射谱图如图丙所示(X射线衍射用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。步骤Ⅱ中,能与反应的物质有(填化学式)。

③结合图示综合分析,步骤Ⅰ中的作用、气体分步制备的价值:。
18. 化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式计算获得。(1)、盐酸浓度的测定:移取待测液,加入指示剂,用溶液滴定至终点,消耗溶液。①上述滴定操作用到的仪器有。
A.
 B.
B. C.
C. D.
D.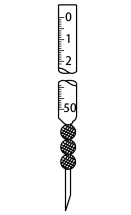
②该盐酸浓度为。
(2)、热量的测定:取上述溶液和盐酸各进行反应,测得反应前后体系的温度值()分别为 , 则该过程放出的热量为(c和分别取和 , 忽略水以外各物质吸收的热量,下同)。(3)、借鉴(2)的方法,甲同学测量放热反应的焓变(忽略温度对焓变的影响,下同)。实验结果见下表。序号
反应试剂
体系温度/
反应前
反应后
i
溶液
粉
a
b
ii
粉
a
c
①温度:bc(填“>”“<”或“=”)。
②(选择表中一组数据计算)。结果表明,该方法可行。
(4)、乙同学也借鉴(2)的方法,测量反应的焓变。查阅资料:配制溶液时需加入酸。加酸的目的是。
提出猜想:粉与溶液混合,在反应A进行的过程中,可能存在粉和酸的反应。
验证猜想:用试纸测得溶液的不大于1;向少量溶液中加入粉,溶液颜色变浅的同时有气泡冒出,说明存在反应A和(用离子方程式表示)。
实验小结:猜想成立,不能直接测反应A的焓变。
教师指导:鉴于以上问题,特别是气体生成带来的干扰,需要设计出实验过程中无气体生成的实验方案。
优化设计:乙同学根据相关原理,重新设计了优化的实验方案,获得了反应A的焓变。该方案为。
(5)、化学能可转化为热能,写出其在生产或生活中的一种应用。三、综合题
-
19. 乙炔加氢是除去乙烯中少量乙炔杂质,得到高纯度乙烯的重要方法。该过程包括以下两个主要反应:
反应1:
反应2:
(1)、25℃,101kPa时,反应 。(2)、一定条件下,使用某含Co催化剂,在不同温度下测得乙炔转化率和产物选择性(指定产物的物质的量/转化的乙炔的物质的量)如图所示(反应均未达平衡)。
①在范围内,乙炔转化率随温度升高而增大的原因为(任写一条),当温度由220℃升高至260℃,乙炔转化率减小的原因可能为。
②在120~240℃范围内,反应1和反应2乙炔的转化速率大小关系为(填“>”“<”或“=”),理由为。
(3)、对于反应1,反应速率与浓度的关系可用方程式表示(k为常数)。时,保持其他条件不变,测定了不同浓度时的反应速率(如下表)。当时,。实验组
一
二
(4)、以Pd/W或Pd为催化剂,可在常温常压下实现乙炔加氢,反应机理如下图所示(虚线为生成乙烷的路径)。以为催化剂时,乙烯的选择性更高,原因为。(图中“*”表示吸附态;数值为生成相应过渡态的活化能) 20. 在温和条件下,将转化为烃类具有重要意义。采用电化学-化学串联催化策略可将高选择性合成 , 该流程示意图如下:
20. 在温和条件下,将转化为烃类具有重要意义。采用电化学-化学串联催化策略可将高选择性合成 , 该流程示意图如下: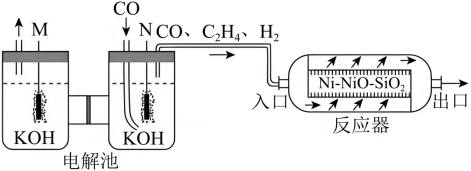
回答下列问题:
(1)、电解池中电极M与电源的极相连。(2)、放电生成的电极反应式为。(3)、在反应器中,发生如下反应:反应i:
反应ii:
计算反应的 , 该反应(填标号)。
A.高温自发 B.低温自发 C.高温低温均自发 D.高温低温均不自发(4)、一定温度下,和(体积比为)按一定流速进入装有催化剂的恒容反应器(入口压强为)发生反应i和ii。有存在时,反应ii的反应进程如图1所示。随着x的增加,的转化率和产物的选择性(选择性)如图2所示。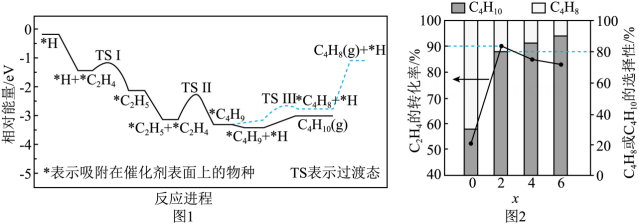
根据图1,写出生成的决速步反应式;的选择性大于的原因是。
②结合图2,当时,混合气体以较低的流速经过恒容反应器时,反应近似达到平衡,随着x的增大,的转化率减小的原因是;当时,该温度下反应ii的(保留两位小数)。0.16
21. 利用CaS循环再生可将燃煤尾气中的SO,转化生产单质硫,涉及的主要反应如下:I . CaS(s) +2SO2(g) =CaSO4(s)+S2(g) ΔH1
II. CaSO4(s) +4H2(g)=CaS(s)+ 4H2O(g) ΔH2
III. SO2(g)+3H2(g)=H,S(g)+2H2O(g) ΔH3
恒容条件下,按1mol CaS,1mol SO2和0.1mol H2投料反应。平衡体系中,各气态物种的lg n随温度的变化关系如图所示,n为气态物种物质的量的值。
已知:图示温度范围内反应Ⅱ平衡常数K=108基本不变。

回答下列问题:
(1)、 反应的焓变ΔH =((用含ΔH1 , ΔH2的代数式表示)。(2)、乙线所示物种为(填化学式)。反应Ⅲ的焓变ΔH30 (填“>”“<”或“=”)。(3)、T温度下,体系达平衡时,乙线、丙线所示物种的物质的量相等,若丁线所示物种为a mol,则S2为mol(用含a的代数式表示);此时,CaS与CaSO4物质的量的差值n(CaS)-n(CaSO4)=mol(用含a的最简代数式表示)。(4)、T2温度下,体系达平衡后,压缩容器体积S2产率增大。与压缩前相比,重新达平衡时,H2S与H2物质的量之比(填“增大”“减小”或“不变”), H2O 物质的量n(H2O)(填“增大”“减小”或“不变”)。四、流程题
-
22. 利用工业废气中的制备焦亚硫酸钠()的一种流程示意图如下。

已知:
物质
、
(1)、制已知:
由制的热化学方程式为。
(2)、制I.在多级串联反应釜中,悬浊液与持续通入的进行如下反应:
第一步:
第二步:
Ⅱ.当反应釜中溶液达到3.8~4.1时,形成的悬浊液转化为固体。
①Ⅱ中生成的化学方程式是。
②配碱槽中,母液和过量配制反应液,发生反应的化学方程式是。
③多次循环后,母液中逐渐增多的杂质离子是 , 需除去。
④尾气吸收器中,吸收的气体有。
(3)、理论研究、与的反应。一定温度时,在浓度均为的和的混合溶液中,随的增加,和平衡转化率的变化如图。
① , 与优先反应的离子是。
② , 平衡转化率上升而平衡转化率下降,结合方程式解释原因:。
23. 钛( )及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少量V、 和 的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗 中含有的几种物质的沸点:
物质
沸点/
136
127
57
180
回答下列问题:
(1)、已知 , 的值只决定于反应体系的始态和终态,忽略 、 随温度的变化。若 ,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是______________。 A、 B、 C、 D、(2)、 与C、 在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
A、 B、 C、 D、(2)、 与C、 在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:物质
分压/
①该温度下, 与C、 反应的总化学方程式为;
②随着温度升高,尾气中 的含量升高,原因是。
(3)、“除钒”过程中的化学方程式为;“除硅、铝”过程中,分离 中含 、 杂质的方法是。(4)、“除钒”和“除硅、铝”的顺序(填“能”或“不能”)交换,理由是。(5)、下列金属冶炼方法与本工艺流程中加入 冶炼 的方法相似的是______________。A、高炉炼铁 B、电解熔融氯化钠制钠 C、铝热反应制锰 D、氧化汞分解制汞