相关试卷
- 甘肃2026届下学期高三年级第二次模拟考试 化学试题
- 广西南宁市2026届高三下学期第二次适应性测试化学试题
- 四川南充市高2026届高三下学期高考适应性考试(二诊) 化学试卷
- 广西壮族自治区柳州市2026届高三上学期二模 化学试题
- 备考2026届高考 2021-2025全国各地真题汇编 专题14 化学实验综合
- 备考2026届高考 2021-2025全国各地真题汇编 专题13 生命活动的物质基础 有机合成
- 备考2026届高考 2021-2025全国各地真题汇编 专题11 盐类水解和沉淀溶解平衡
- 备考2026届高考 2021-2025全国各地真题汇编 专题10 弱电解质的电离平衡和溶液的酸碱性
- 备考2026届高考 2021-2025全国各地真题汇编 专题9 化学反应速率与化学平衡
- 备考2026届高考 2021-2025全国各地真题汇编 专题8 化学反应与电能
-
1、科学家们通过Ca原子和Bk原子相互轰击得到了第117号元素,元素符号为Ts,其稳定的核素为。核素的中子数为A、293 B、176 C、117 D、59
-
2、下列成语涉及的过程,不属于化学变化的是A、水滴石穿 B、百炼成钢 C、大浪淘沙 D、死灰复燃
-
3、
某小组通过分析镁与酸反应时的变化,探究镁与醋酸溶液反应的实质。
【资料】查阅醋酸溶液的资料发现,向冰醋酸中逐渐加水,溶液的导电性随加入水的体积的变化如图1所示。

图1
(1)用化学用语表示醋酸水溶液能导电的原因:。
(2)在a、b、c三点所代表的溶液中,由大到小的顺序为:;醋酸电离程度最大的是。(填“a”、“b”或“c”)。
【实验】在常温水浴条件下,进行实验 , 记录生成气体体积和溶液的变化:
Ⅰ.取光亮的镁屑(过量)放入溶液中;
Ⅱ.取光亮的镁屑放入溶液中;
Ⅲ.取光亮的镁屑放入溶液中。
【数据】


(3)起始阶段,导致Ⅱ、Ⅲ气体产生速率差异的主要因素不是 , 实验证据是。
(4)探究Ⅱ的反应速率大于Ⅲ的原因。
提出假设:能直接与反应。
进行实验Ⅳ:。
得出结论:该假设成立。
(5)探究醋酸溶液中与反应的主要微粒,进行实验Ⅴ。与Ⅱ相同的条件和试剂用量,将溶液换成含的与的混合溶液 , 气体产生速率与Ⅱ对比如下。
a.实验Ⅴ起始速率
b.实验Ⅱ起始速率
c.实验Ⅱ时速率
对比中的微粒浓度,解释其a与b、a与c气体产生速率差异的原因:。
(6)综合以上实验得出结论:
①镁与醋酸溶液反应时,均能与镁反应产生氢气;②。
(7)实验反思:附近,中仍在产生 , 但均基本不变,且 , 结合化学用语解释其原因:。
-
4、不对称分子梳M是一种性能优良的表面防污涂层材料,其合成路线如下图所示。

ⅰ.

ⅱ.
 (1)、A中不含环状结构,A分子中含有的官能团有。(2)、E→F的反应类型是。(3)、下列说法中正确的是(填字母)。
(1)、A中不含环状结构,A分子中含有的官能团有。(2)、E→F的反应类型是。(3)、下列说法中正确的是(填字母)。a.化合物D的同分异构体共有5种
b.化合物A、B、E均能使酸性褪色
c.化合物E的沸点低于化合物F
d.化合物G、I中均含手性碳原子
(4)、F+G→I的化学方程式是。(5)、化合物J的结构简式为。(6)、聚合物L的结构简式为。(7)、分子梳M的抗污性能与梳齿中的基团有关,为了测定分子梳中梳齿的“密度”(分子梳主链上接入的梳齿数与主链链节数之比),测得某M样品的核磁共振氢谱中,主链上所有a处H原子与梳齿中b处H原子的两组信号峰面积比 , 则梳齿2的密度为。 -
5、热电厂用碱式硫酸铝[Al2(SO4)3•Al2O3]吸收烟气中低浓度的二氧化硫。具体过程如下:(1)、碱式硫酸铝溶液的制备
往Al2(SO4)3溶液中加入一定量CaO粉末和蒸馏水,可生成碱式硫酸铝(络合物,易溶于水),同时析出生石膏沉淀[CaSO4·2H2O],反应的化学方程式为。
(2)、SO2的吸收与解吸。吸收液中碱式硫酸铝活性组分Al2O3对SO2具有强大亲和力,化学反应为:Al2(SO4)3·Al2O3(aq)+3SO2(g)Al2(SO4)3·Al2(SO3)3(aq) △H<0。工业流程如下图所示:
① 高温烟气可使脱硫液温度升高,不利于SO2的吸收。生产中常控制脱硫液在恒温40~60oC,试分析原因。
② 研究发现,I中含碱式硫酸铝的溶液与SO2结合的方式有2种:其一是与溶液中的水结合。其二是与碱式硫酸铝中的活性Al2O3结合,通过酸度计测定不同参数的吸收液的pH变化,结果如下图所示:

据此判断初始阶段,SO2的结合方式是。
比较x、y、z的大小顺序。
③ III中得到再生的碱式硫酸铝溶液,其n(Al2O3):n[Al2(SO4)3]比值相对I中有所下降,请用化学方程式加以解释:。
(3)、解吸得到较纯的SO2 , 可用于原电池法生产硫酸。
① 电极b周围溶液pH(填“变大”、“变小”或“不变”)
② 电极a的电极反应式是。
-
6、硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是的催化氧化: , 回答下列问题:(1)、钒催化剂参与反应的能量变化如图(a)所示,与反应生成和的热化学方程式为:。
 (2)、当和起始的物质的量分数分别为7.5%、10.5%和82%时,在和压强下,平衡转化率随温度的变化如图(b)所示。反应在时的 , 判断的依据是。影响的因素有。
(2)、当和起始的物质的量分数分别为7.5%、10.5%和82%时,在和压强下,平衡转化率随温度的变化如图(b)所示。反应在时的 , 判断的依据是。影响的因素有。 (3)、将组成(物质的量分数)为和的气体通入反应器,在一定的温度和压强下进行反应。平衡时,若转化率为 , 则的物质的量分数为。(4)、研究表明,催化氧化的反应速率方程为: , 式中:k为反应速率常数,随温度t升高而增大;为平衡转化率,为某时刻转化率,n为常数。在时,将一系列温度下的k、值代入上述速率方程,得到曲线,如图(c)所示。已知:图示温度范围催化剂活性变化不大。
(3)、将组成(物质的量分数)为和的气体通入反应器,在一定的温度和压强下进行反应。平衡时,若转化率为 , 则的物质的量分数为。(4)、研究表明,催化氧化的反应速率方程为: , 式中:k为反应速率常数,随温度t升高而增大;为平衡转化率,为某时刻转化率,n为常数。在时,将一系列温度下的k、值代入上述速率方程,得到曲线,如图(c)所示。已知:图示温度范围催化剂活性变化不大。
曲线上v最大值所对应温度称为该下反应的最适宜温度。时,v逐渐提高;后,v逐渐下降。原因是。
-
7、甲胺铅碘[]()和甲脒铅碘[](),均可用作太阳能电池的功能材料。已知:位于元素周期表的第六周期第族。(1)、第一电离能: (填“<”或“>”);基态原子的价电子排布式。(2)、与相比,中原子结合能力更强,原因是。(3)、下列说法正确的是(填序号)。
a.的最高化合价为
b.键角:
c.已知中所有原子位于同一平面,则N的杂化类型均为
(4)、两种材料具有相同的晶胞类型,如图所示。
①“
 ”代表或 , “
”代表或 , “ ”代表(填“”或“”)。
”代表(填“”或“”)。②与“
 ”距离最近且相等的“
”距离最近且相等的“ ”有个。
”有个。③若甲胺铅碘的晶胞边长为a
 , 则其晶体的密度为。(已知:1
, 则其晶体的密度为。(已知:1 , 阿伏加德罗常数的值用表示)
, 阿伏加德罗常数的值用表示)④研究发现,用少量有机二元胺的阳离子(如下)代替晶体表面部分 , 可提升电池的防潮性能,且效果:。a、b效果不同的可能原因是。
a.
 b.
b.
-
8、某学习小组为探究氯化铜与亚硫酸钠的反应,设计了如下实验:




溶液
溶液
橙黄色沉淀
(含、、)
白色沉淀()
已知:。
下列分析中,不正确的是
A、的溶液呈弱酸性 B、由实验可知,生成橙黄色沉淀的速率较快,而生成白色沉淀的反应趋势更大 C、取洗涤后的橙黄色沉淀于试管中,加入稀硫酸,若溶液变蓝,则说明橙黄色沉淀含有 D、本实验中,溶液和溶液的总反应离子方程式为: -
9、一种新型短路膜电池分离装置如下图所示。下列说法中,正确的是
 A、负极反应为: B、正极反应消耗 , 理论上需要转移电子 C、该装置用于空气中的捕获和分离,最终由出口A流出 D、短路膜和常见的离子交换膜不同,它既能传递离子,还可以传递电子
A、负极反应为: B、正极反应消耗 , 理论上需要转移电子 C、该装置用于空气中的捕获和分离,最终由出口A流出 D、短路膜和常见的离子交换膜不同,它既能传递离子,还可以传递电子 -
10、铑的配合物离子可催化甲醇羰基化,反应过程如图所示。

下列叙述不正确的是
A、是反应中间体 B、 中与配位的原子是I和O
C、甲醇羰基化反应为
D、其中为取代反应
中与配位的原子是I和O
C、甲醇羰基化反应为
D、其中为取代反应
-
11、室温下,下列实验方案能达到相应目的的是
选项
实验方案
目的
A
将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加溶液,观察溶液颜色变化
探究食品脱氧剂样品中有无价铁
B
用计测量等物质的量浓度的醋酸、盐酸的 , 比较溶液大小
证明是弱电解质
C
向浓中插入红热的炭,观察生成气体的颜色
证明炭可与浓反应生成
D
向淀粉溶液中加适量溶液,加热,冷却后加溶液至碱性,再加少量碘水,观察溶液颜色变化
探究淀粉溶液在稀硫酸和加热条件下是否水解
A、A B、B C、C D、D -
12、某小组探究的催化氧化,实验装置图如下。③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后,④中产生白烟,⑤中溶液变蓝。

下列分析正确的是
A、若②中只有不能制备 B、③、④中现象说明③中的反应是 C、④中白烟的主要成分是 D、⑤中溶液变蓝说明是稀硫酸与反应的催化剂 -
13、下列方程式与所给事实相符的是A、石灰乳浊液[]与溶液反应: B、室温下用稀溶解铜: C、溶液中通入少量: D、溶液中加入过量浓氨水:
-
14、下列说法不正确的是A、淀粉作为人类重要的能量来源,是由于它能发生水解产生葡萄糖供机体利用 B、纤维素能通过酯化反应得到醋酸纤维素,是由于纤维素分子中含有羟基 C、核糖核苷酸分子间脱水后聚合形成核糖核酸 D、石油经过分馏可得到煤油、柴油等,是利用了物质的溶解性差异
-
15、下列化学用语或图示表达不正确的是A、基态的简化电子排布式: B、的原子结构示意图:
 C、分子的空间结构:
C、分子的空间结构: D、的模型:
D、的模型:
-
16、铁红是颜料,什么什么自古以来使用很多的……(题干缺失)。(1)、赭红的主要成分是_______。A、 B、 C、 D、(2)、饱和氯化铁溶液说法正确的是_______。A、常温显中性 B、加铁粉变红褐色 C、遇沸水后得到胶体 D、加氨水有白色沉淀(3)、有关铁原子说法正确的是_______。(不定项)A、有4个不同能级的电子 B、有5个未成对电子 C、占据15个原子轨道 D、有26种能量不同的电子(4)、加热试管中固体至红热,则_______。(不定项)
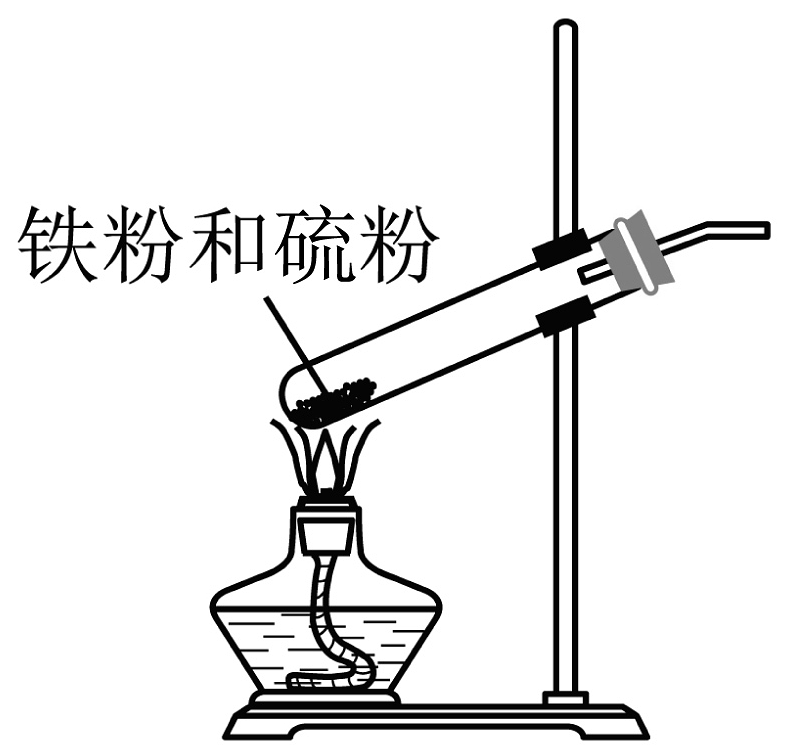 A、移开酒精灯后固体保持红热 B、S只做还原剂 C、主要产生的气体附产物为 D、最终得到黑色的(5)、内界为 , 配体有种(6)、 , 加水稀释至体积为原来的2倍,则。
A、移开酒精灯后固体保持红热 B、S只做还原剂 C、主要产生的气体附产物为 D、最终得到黑色的(5)、内界为 , 配体有种(6)、 , 加水稀释至体积为原来的2倍,则。A.增大 B.不变 C.减小
并用浓度商Q与平衡常数K的大小关系解释原因。
(7)、已知 , 求的分布系数。x
1
2
3
4
K
30.2
134.9
97.72
1.02
-
17、
工业从低品位锗矿中提取精锗,使用分步升温的方法:

(1)验证矿石中的锗元素可使用的方法为________。
A.原子发射光谱法 B.红外光谱法 C.X射线衍射
(2)既能和强酸反应,也能与强碱反应,由此推测是________氧化物。
已知矿中含有、煤焦油、等杂质,相关物质的熔、沸点如下表所示:
煤焦油
熔点
升华
沸点
(3)使用分段升温的原因是________。
(4)下图为在不同温度下,使用不同浓度的真空还原时,元素的萃出率,图可知真空还原采用的最佳温度及浓度为_______。
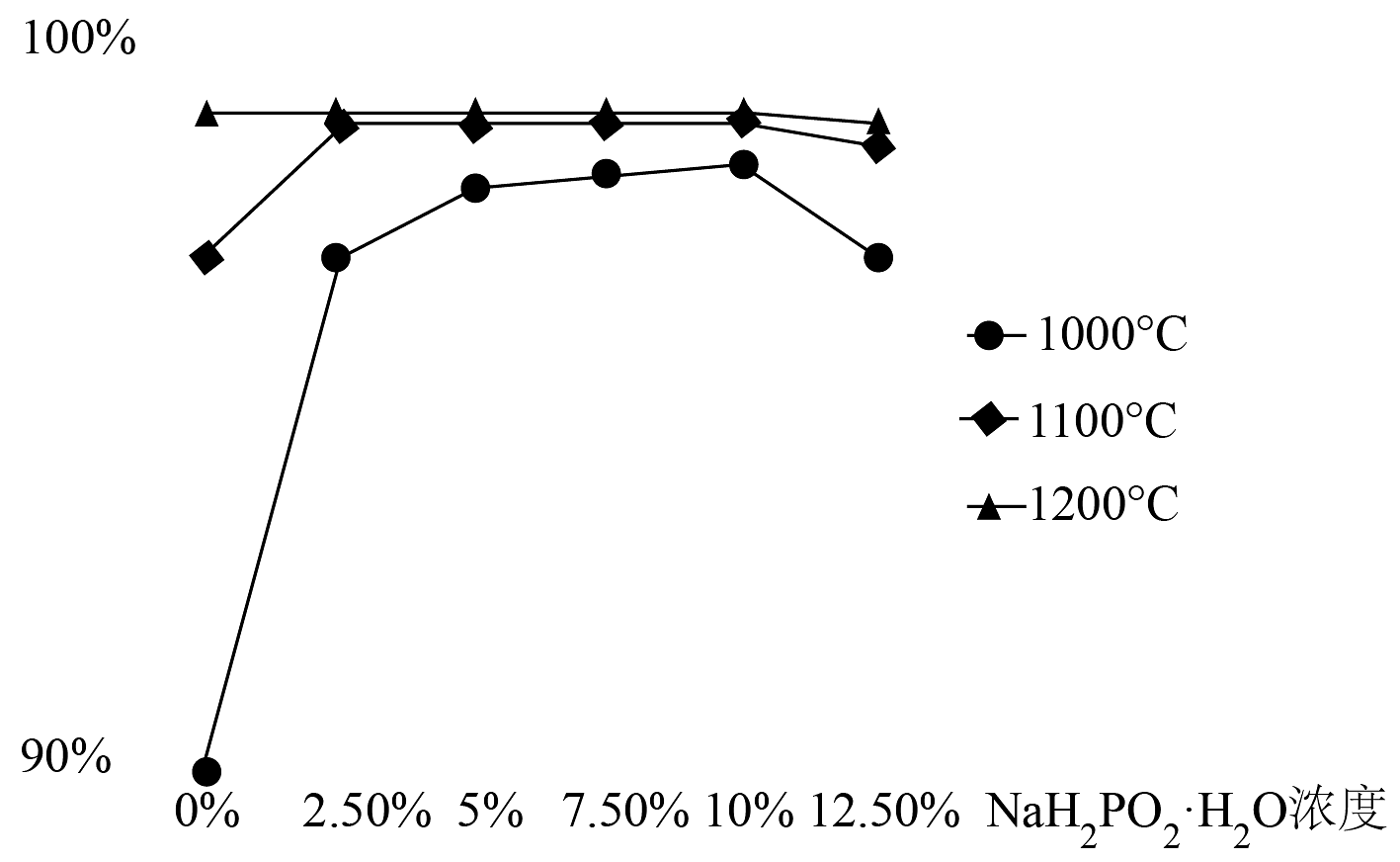
A. , 2.5% B. , 5.0% C. , 2.5% D. , 2.5% (5)真空还原阶段用除 , 产物还有等生成,写出该阶段的化学方程式________。
采用滴定法测定样品中元素含量的方法如下:
(以下实验过程根据回忆所得信息结合文献资料重新整合所得,仅供参考)
准确称取含锗矿石粉末,置于圆底烧瓶中。加入浓盐酸和溶液,加热至微沸(溶解)冷却后,加入 , 搅拌至溶液变为无色。将溶液转移至锥形瓶,用稀盐酸冲洗烧瓶并入锥形瓶中。
加入磷酸 , 冷却溶液至以下(冰水浴),用橡胶塞密封锥形瓶。向锥形瓶中加入淀粉溶液作为指示剂。用标准溶液滴定至滴定终点。
记录消耗的体积为。
(还原)
(主反应)
(终点反应)
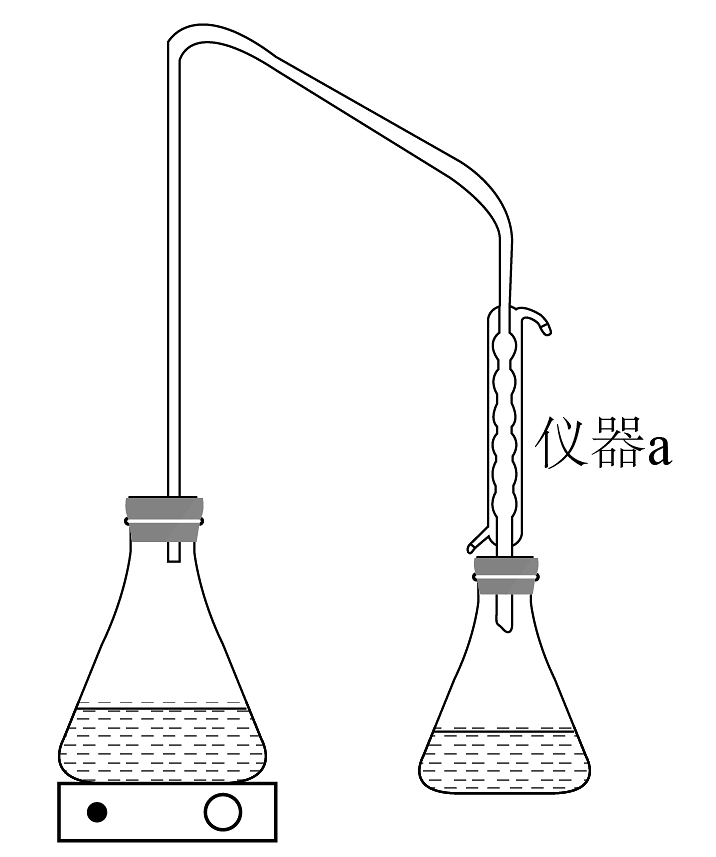
(6)装置a名称为_______。
A. 锥形瓶 B. 恒压滴液漏斗 C. 球形冷凝管 D. 滴定管 (7)滴定终点时,颜色由________变为________,半分钟不褪色。
(8)滴定时为什么要用橡胶塞塞紧锥形瓶________?(真空还原)
(9)已知 , 求样品(固体)中元素的质量分数【纯度】________(用c、V、m表示)。
(10)滴定结果纯度偏大,可能的原因是_______。
A. 未用标准溶液润洗滴定管 B. 未用将样品从冷凝管中洗入锥形瓶(仪器a) C. 滴定结束后,在滴定管尖嘴处出现气泡 D. 在常温下滴定(未保持在以下滴定) -
18、(以下题目中的流程根据回忆所得信息结合文献资料重新整合所得,仅供参考)
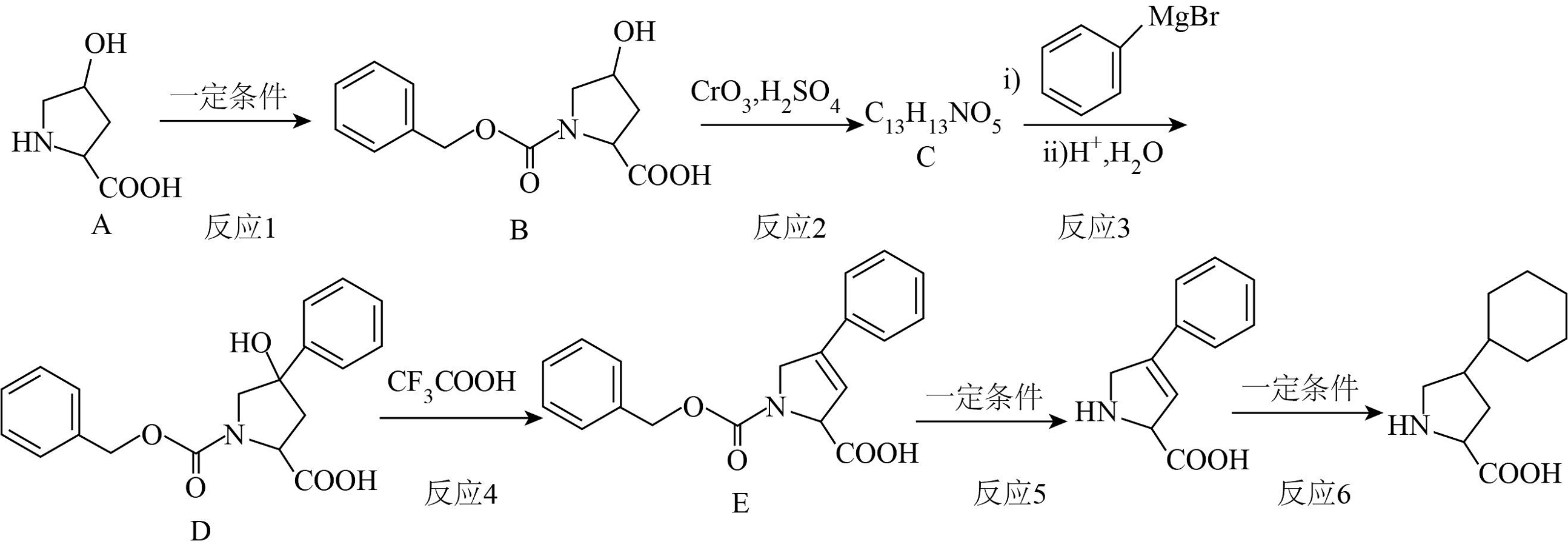
已知:
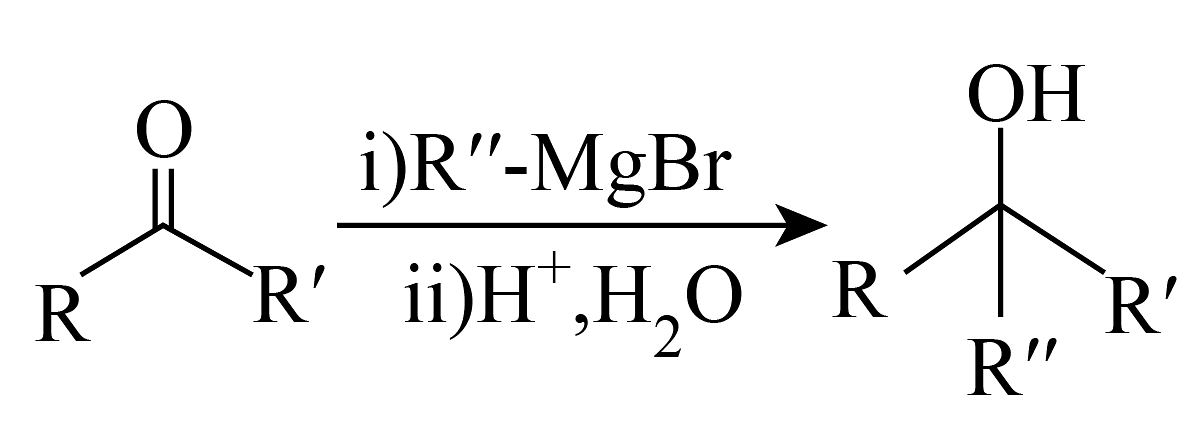 (1)、A中含氧官能团的结构简式为:。(2)、反应1的作用是:。(3)、反应2为(反应类型)。(4)、D中有_______个手性碳原子。A、1 B、2 C、3 D、4(5)、生成E的同时会生成其同分异构体H,H的结构简式为:。(6)、关于化合物E的说法中正确的是_______。A、碳的杂化方式有和两种 B、能与茚三酮反应 C、能与反应产生 D、能形成分子间氢键(7)、F的同分异构体I水解后生成J、K,写出一种符合条件的I即可。
(1)、A中含氧官能团的结构简式为:。(2)、反应1的作用是:。(3)、反应2为(反应类型)。(4)、D中有_______个手性碳原子。A、1 B、2 C、3 D、4(5)、生成E的同时会生成其同分异构体H,H的结构简式为:。(6)、关于化合物E的说法中正确的是_______。A、碳的杂化方式有和两种 B、能与茚三酮反应 C、能与反应产生 D、能形成分子间氢键(7)、F的同分异构体I水解后生成J、K,写出一种符合条件的I即可。i.J是有3个碳原子的α-氨基酸
ii.K遇溶液溶液能显色
iii.由核磁共振氢谱分析,K的苯环上有2种氢,个数比为
(8)、反应的反应条件是:。(9)、以和 为原料,合成
为原料,合成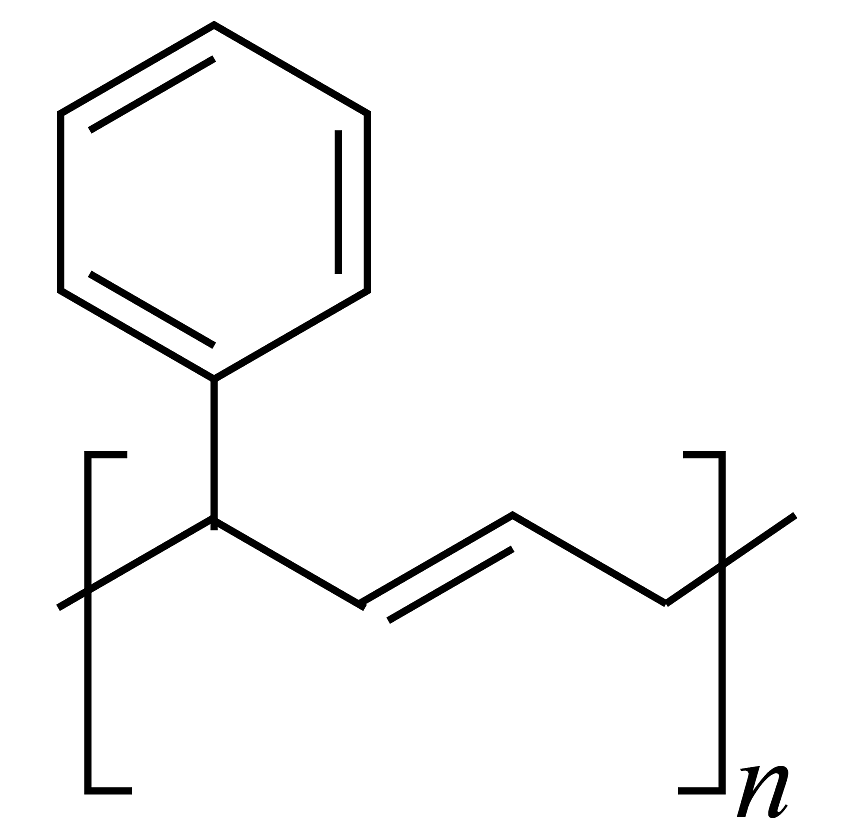 (无机试剂任选)。
(无机试剂任选)。 -
19、
(以下题目中的图片根据回忆所得信息结合文献资料重新整合所得,仅供参考)
(1)钨作灯丝与_______性质有关(不定项)。
A.延展性 B导电性 C.高熔点 D.高密度
(2)钨有金属光泽的原因________ (从微观角度解释)。(3)原子在晶胞中的_______位置。
A. 顶点 B. 棱上 C. 面上 D. 体心 (4)钨在周期表中的位置是_______。

A. 第五周期第ⅡB族 B. 第五周期第ⅣB族 C. 第六周期第ⅡB族 D. 第六周期第ⅥB族 (5)根据价层电子对斥理论,的价层电子对数是________。
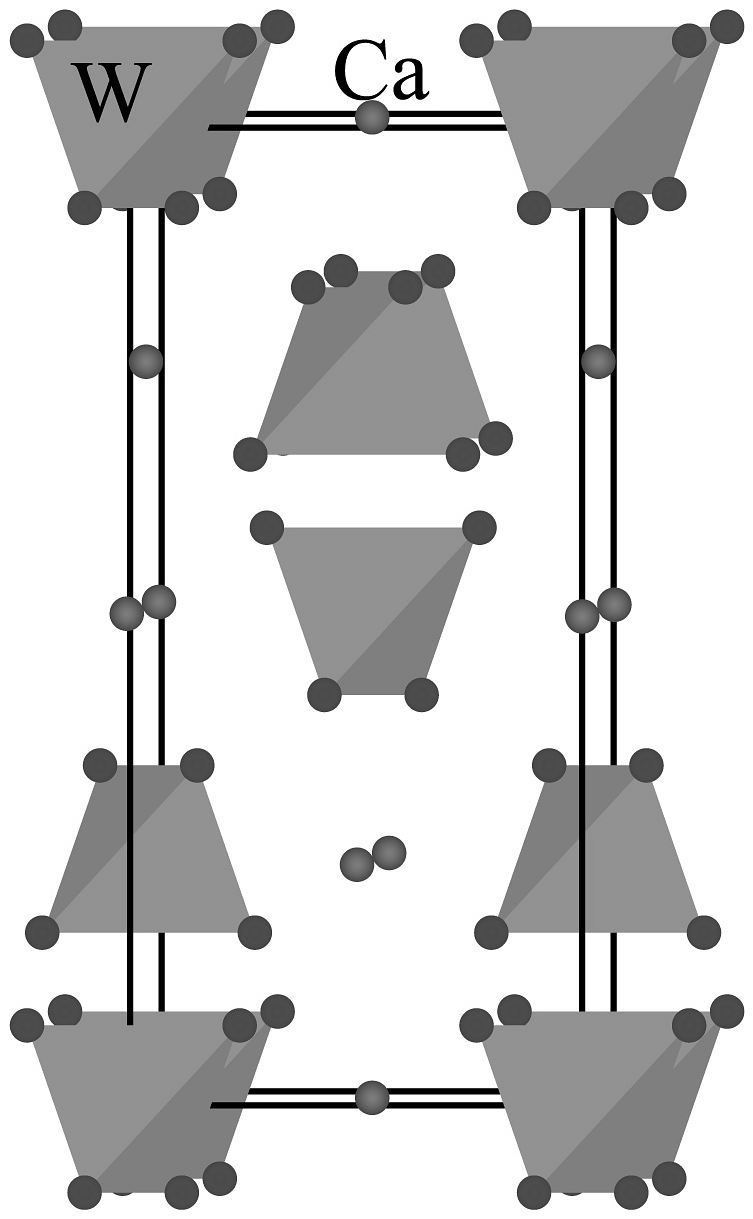
(6)图晶胞号O原子,若晶胞仅含1个完整四面体,组成该四面体的O编号是________。
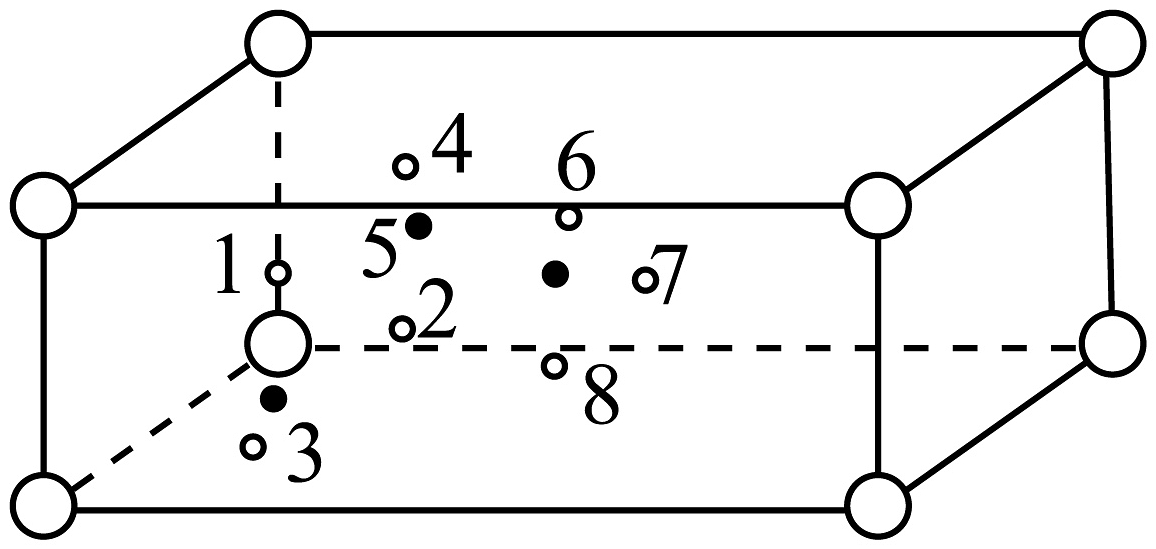
表格(各种矿石密度)。

(7)给出晶胞参数,求并说明“重石头”俗名依据________。(有V和M?)
电解制备是光电陶瓷材料
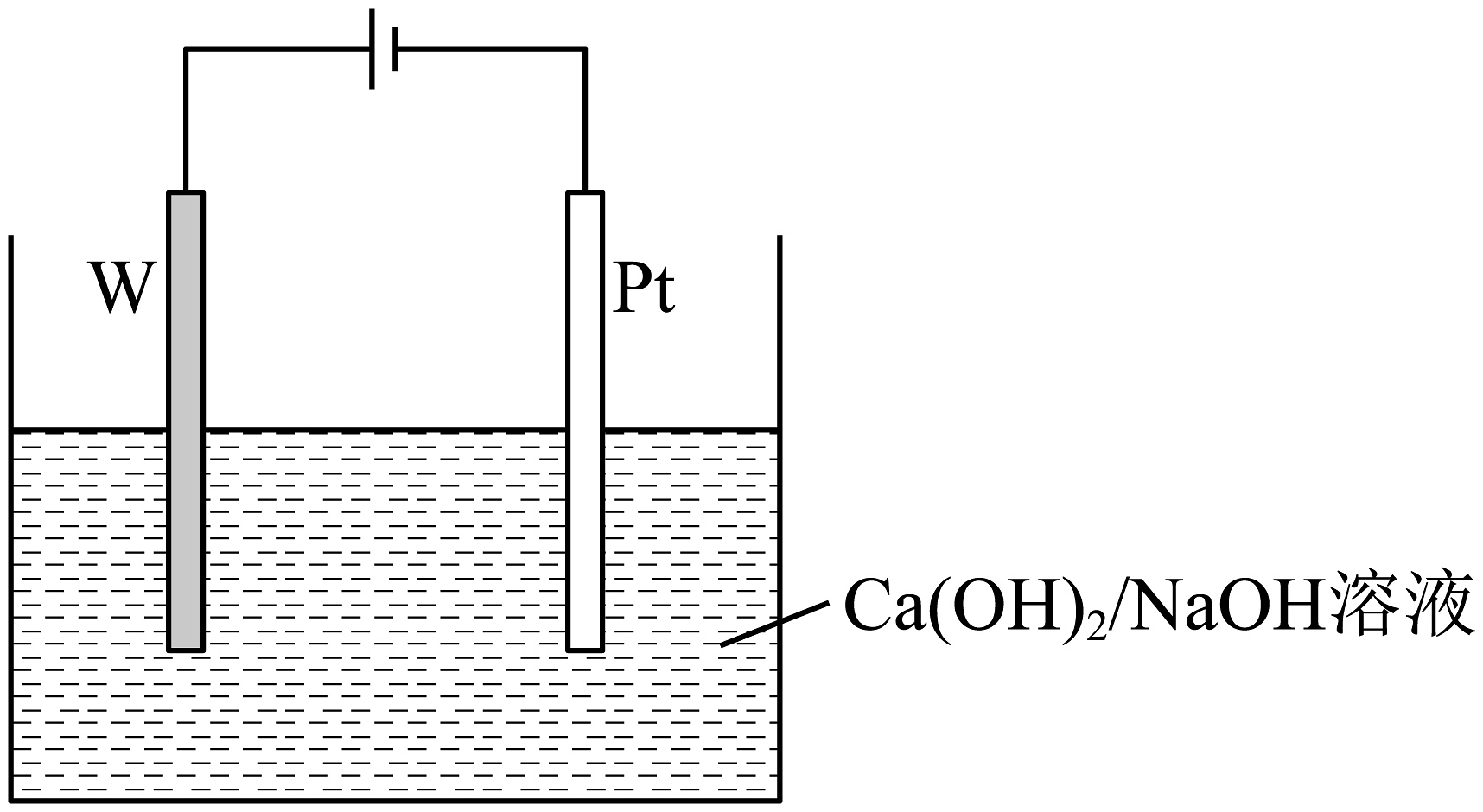
已知
(8)写出电解的阳极方程式________。
(9)为获取高纯产物,制备时需要不断通入的原因________。
-
20、
已知反应1
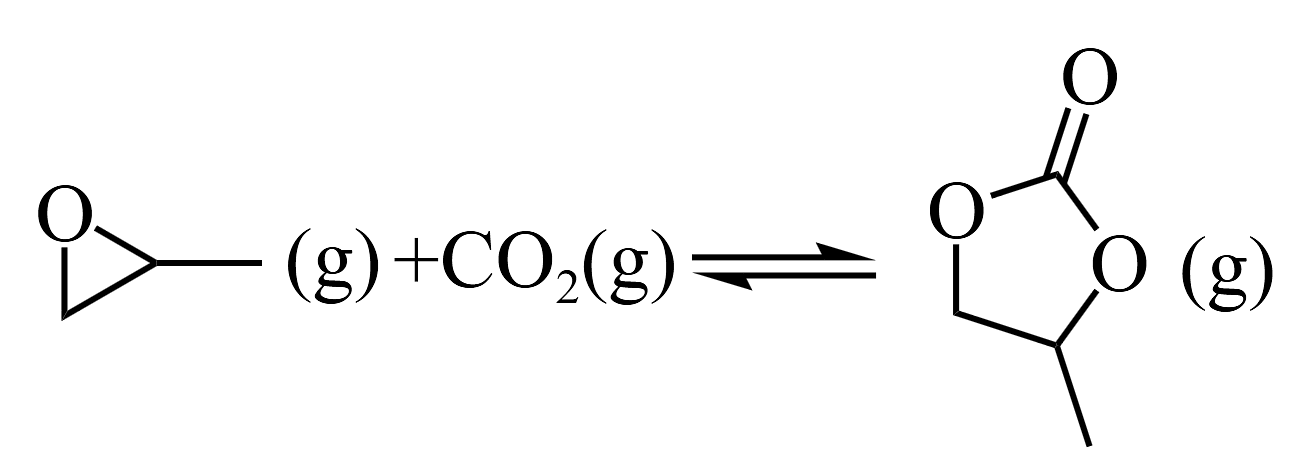 的
的反应2的
反应3的
反应4的
物质
环氧丙烷
(1)计算出_______。
A. B. 613.2 C. 395.2 D. (2)随温度T的变化趋势________。
(3)
 中电负性最大的是________。
中电负性最大的是________。A.C B.H C.O
(4)
 分了中键的数目为_______。
分了中键的数目为_______。A. 7 B. 12 C. 13 D. 14 已知:环氧丙烷生成
 会发生副反应
会发生副反应选择性=转化生成A的环氧丙烷/消耗环氧丙烷
M(环氧丙烷) ρ(环氧丙烷)
容器容积的高压反应釜反应后体积缩小为 , 选择性为95%,反应。
(5)求环氧丙烷的化学反应速率________(精确到小数点后2位)
(6)下列哪种操作可以使得活化分子的百分数变大_______。
A. 升高温度 B. 增大浓度 C. 压缩容器 D. 充入惰性气体 (7)碳酸丙烯酯相同时间内随温度变化如图所示,请解释产率随温度先升后下降的原因________。
(8)达到平衡的判据_______。
A. v正=v逆 B. 体系总质量不变 C. 气体体积不再变化 D. 混合气体密度(可能是摩尔质量)不变 (9)制备
 还有一种光气法,用
还有一种光气法,用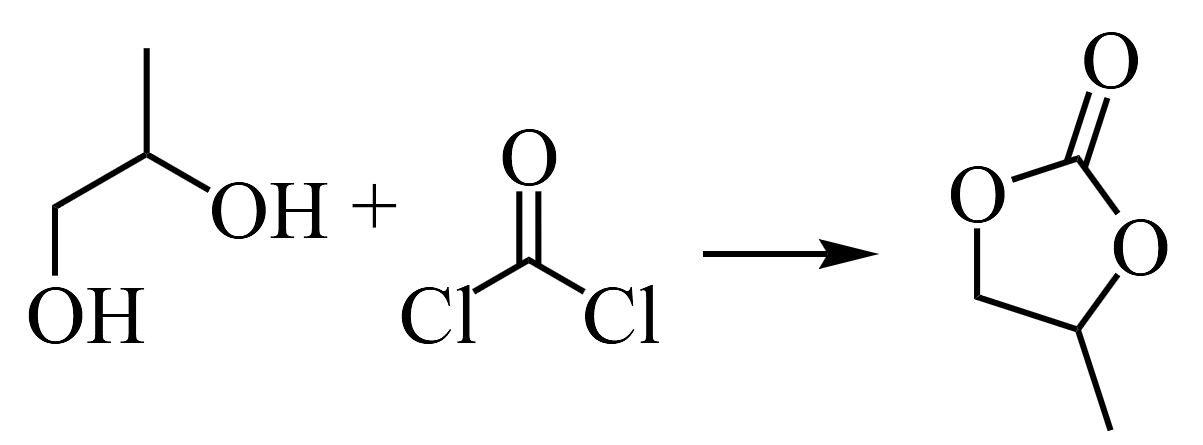 。请从绿色化学的角度解释,写出3点与光气-二醇法相比,法合成的优势________。
。请从绿色化学的角度解释,写出3点与光气-二醇法相比,法合成的优势________。