相关试卷
- 甘肃2026届下学期高三年级第二次模拟考试 化学试题
- 广西南宁市2026届高三下学期第二次适应性测试化学试题
- 四川南充市高2026届高三下学期高考适应性考试(二诊) 化学试卷
- 广西壮族自治区柳州市2026届高三上学期二模 化学试题
- 备考2026届高考 2021-2025全国各地真题汇编 专题14 化学实验综合
- 备考2026届高考 2021-2025全国各地真题汇编 专题13 生命活动的物质基础 有机合成
- 备考2026届高考 2021-2025全国各地真题汇编 专题11 盐类水解和沉淀溶解平衡
- 备考2026届高考 2021-2025全国各地真题汇编 专题10 弱电解质的电离平衡和溶液的酸碱性
- 备考2026届高考 2021-2025全国各地真题汇编 专题9 化学反应速率与化学平衡
- 备考2026届高考 2021-2025全国各地真题汇编 专题8 化学反应与电能
-
1、0.25 L NaOH溶液中溶有10 g NaOH,则此溶液的物质的量浓度为( )A、2 mol/L B、1 mol/L C、0.5 mol/L D、0.05 mol/L
-
2、火药制备是我国古代闻名世界的化学工艺,原理为2KNO3+S+3C=K2S+N2↑+3CO2↑。下列表示反应中相关微粒的化学用语正确的是A、K+的结构示意图:
 B、K2S的电子式:
C、CO2的结构式为:O=C=O
D、18O2和16O2互为同位素
B、K2S的电子式:
C、CO2的结构式为:O=C=O
D、18O2和16O2互为同位素
-
3、广东有许多具有地域特征的民间活动,下列各项描述中所涉及的化学知识错误的是
选项
民间活动
化学知识
A
喜庆节日,客家人喜欢用娘酒来款宴宾客
娘酒的酿造过程涉及氧化还原反应
B
广佛地区流行“叹”早茶
泡茶的过程涉及萃取操作
C
潮汕地区中秋夜“烧塔”时,人们把海盐撒向塔里,黄色火焰直冲云天
“黄色火焰”是因为NaCl受热分解
D
“豆腐节”是佛冈县元宵节独具特色的活动
制豆腐时涉及到胶体的聚沉
A、A B、B C、C D、D -
4、在一定条件,将1 mol N2O5放入1 L的容器中发生下列可逆反应:2N2O5(g) 4NO2(g)+O2(g),NO2的物质的量浓度c(NO2)随时间变化的实验数据如表所示:
时间/min
0
5
10
15
20
25
c(NO2)/(mol·L-1)
0
0.20
0.32
0.38
0.40
0.40
根据表中数据,该反应达到平衡时c(NO2)为
A、0.20 mol·L-1 B、0.32mol·L-1 C、0.38 mol·L-1 D、0.40 mol·L-1 -
5、丙烯酸的结构简式为CH2=CH-COOH,其对应的性质中不正确的是A、能与钠反应放出氢气 B、能与Na2CO3溶液反应 C、能与溴水发生取代反应 D、能与NaOH溶液反应
-
6、下列说法正确的是(NA表示阿伏加德罗常数的值)A、1 mol Fe粉与足量水蒸气反应生成的H2分子数目为NA B、常温时,11.2 L氮气所含有的原子数目为NA C、常温常压下,46 g的NO2气体含有的原子数目为3NA D、1 mol NO2与水反应时电子转移数目为NA
-
7、部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法错误的是
 A、a与d,a与e在酸性情况下反应,均可以得到b B、c为一种新型自来水消毒剂,代替b的原因是c的毒性更小 C、b的水溶液里加入CaCO3 , 沉淀溶解 D、消毒液可用于环境消毒,原理是先产生d,e的固体可用于实验室制O2
A、a与d,a与e在酸性情况下反应,均可以得到b B、c为一种新型自来水消毒剂,代替b的原因是c的毒性更小 C、b的水溶液里加入CaCO3 , 沉淀溶解 D、消毒液可用于环境消毒,原理是先产生d,e的固体可用于实验室制O2 -
8、下列物质的分类错误的是A、水、二氧化硫和干冰都属于氧化物( ) B、H2SO4、HNO3和H2CO3都属于酸 C、KNO3、CuSO4和NH4Cl都属于盐 D、烧碱、纯碱、熟石灰都属于碱
-
9、下列关于甲烷、乙烯、乙醇的说法正确的是A、都是难溶于水的物质 B、都可以从石油分馏的产物中获得 C、都能使酸性高锰酸钾溶液褪色 D、在一定条件下都可以发生氧化反应
-
10、在1 L 1 mol·L-1 Al2(SO4)3溶液中含有的物质的量浓度是A、1 mol·L-1 B、20 mol·L-1 C、3 mol·L-1 D、2 mol·L-1
-
11、下列各物质组中,所含两种物质化学键类型不同的是A、HCl和NH3 B、CaCl2和NaCl C、H2O2和Na2O2 D、NaCl和Na2O
-
12、下列关于能量变化的说法不正确的是A、冰融化成水吸收热量 B、化学键形成过程一定放出能量 C、化学键的断裂和形成是化学反应中能量变化的主要原因 D、生成物的总能量一定低于反应物的总能量
-
13、一种“即热即食型”快餐适合外出旅行时使用。它是利用两种物质发生化学反应对食物进行加热,这两种化学物质最合适的选择是A、浓硫酸与水 B、生石灰与水 C、熟石灰与水 D、氯化钠与水
-
14、如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池。下列叙述正确的是
 A、Zn是负极,发生还原反应 B、电子从锌片经外电路流向铜片 C、一段时间后溶液变蓝 D、铜片上无任何现象
A、Zn是负极,发生还原反应 B、电子从锌片经外电路流向铜片 C、一段时间后溶液变蓝 D、铜片上无任何现象 -
15、下列反应中,属于氧化还原反应的是( )A、SO2+H2O
 H2SO3
B、2NaHCO3 Na2CO3+ H2O+CO2↑
C、2Na+2H2O = 2NaOH+H2↑
D、Al(OH)3+3HCl = AlCl3+3H2O
H2SO3
B、2NaHCO3 Na2CO3+ H2O+CO2↑
C、2Na+2H2O = 2NaOH+H2↑
D、Al(OH)3+3HCl = AlCl3+3H2O
-
16、下列气体中不能用浓硫酸干燥的是A、SO2 B、NH3 C、H2 D、HCl
-
17、下列表示物质结构的化学用语或模型正确的是A、含 8 个中子的碳原子的核素符号:12C B、HF的电子式:
 C、Cl-的结构示意图:
C、Cl-的结构示意图: D、CH4的空间填充模型:
D、CH4的空间填充模型:
-
18、实验室里进行过滤和蒸发操作都要用到的仪器是A、烧杯 B、玻璃棒 C、蒸发皿 D、酒精灯
-
19、某乙烯燃料电池的工作原理如图所示。下列说法正确的是
 A、放电时,电子由电极b经外电路流向电极a B、电极a的电极反应式为 C、当有通过质子交换膜时,电极b表面理论上消耗的体积为 D、验证生成的操作:取反应后的左室溶液,加入新制 , 加热,观察现象
A、放电时,电子由电极b经外电路流向电极a B、电极a的电极反应式为 C、当有通过质子交换膜时,电极b表面理论上消耗的体积为 D、验证生成的操作:取反应后的左室溶液,加入新制 , 加热,观察现象 -
20、在温和条件下,将转化为烃类具有重要意义。采用电化学-化学串联催化策略可将高选择性合成 , 该流程示意图如下:
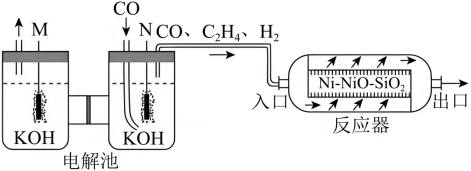
回答下列问题:
(1)、电解池中电极M与电源的极相连。(2)、放电生成的电极反应式为。(3)、在反应器中,发生如下反应:反应i:
反应ii:
计算反应的 , 该反应(填标号)。
A.高温自发 B.低温自发 C.高温低温均自发 D.高温低温均不自发(4)、一定温度下,和(体积比为)按一定流速进入装有催化剂的恒容反应器(入口压强为)发生反应i和ii。有存在时,反应ii的反应进程如图1所示。随着x的增加,的转化率和产物的选择性(选择性)如图2所示。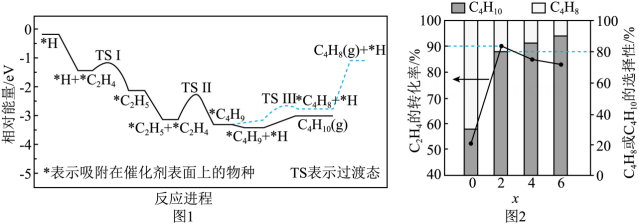
根据图1,写出生成的决速步反应式;的选择性大于的原因是。
②结合图2,当时,混合气体以较低的流速经过恒容反应器时,反应近似达到平衡,随着x的增大,的转化率减小的原因是;当时,该温度下反应ii的(保留两位小数)。0.16