-
1、为探究铜的化学性质,某同学借助氧气传感器在密闭装置中进行如图所示实验,观察实验现象并分析氧气含量随时间变化的曲线图。其中终点D(203,615%)表示时间为203秒时,装置中氧气含量为6.15%。结合图示判断下列说法错误的是
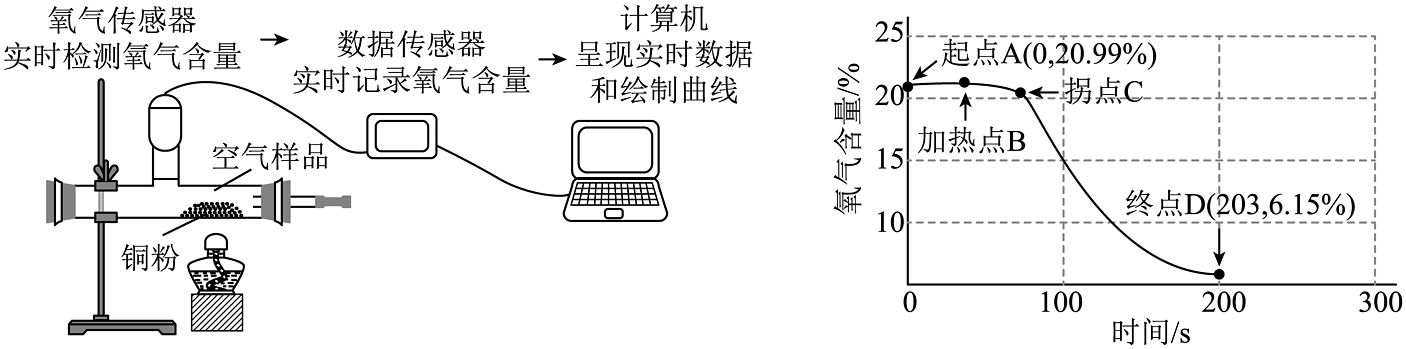 A、加热前的空气样品中氧气含量为20.99% B、铜在加热条件下能与氧气发生化学反应 C、加热时要先预热再固定在铜粉处加热 D、拐点C至终点D所对应的时间范围内,装置内物质的总质量逐渐减少
A、加热前的空气样品中氧气含量为20.99% B、铜在加热条件下能与氧气发生化学反应 C、加热时要先预热再固定在铜粉处加热 D、拐点C至终点D所对应的时间范围内,装置内物质的总质量逐渐减少 -
2、基于问题设计实验方案是实验探究活动的重要环节。下列实验方案中合理的是
选项
实验问题
实验方案
A
鉴别氮气和二氧化碳
将带火星的木条伸入盛有气体的试管中,观察现象
B
除去KCl中的
溶解,过滤,洗涤、干燥
C
验证Cu、Al的金属活动性
将洁净的铝丝浸入溶液中,观察现象
D
稀释浓硫酸
取水倒入浓硫酸中,并用玻璃棒不断搅拌
A、A B、B C、C D、D -
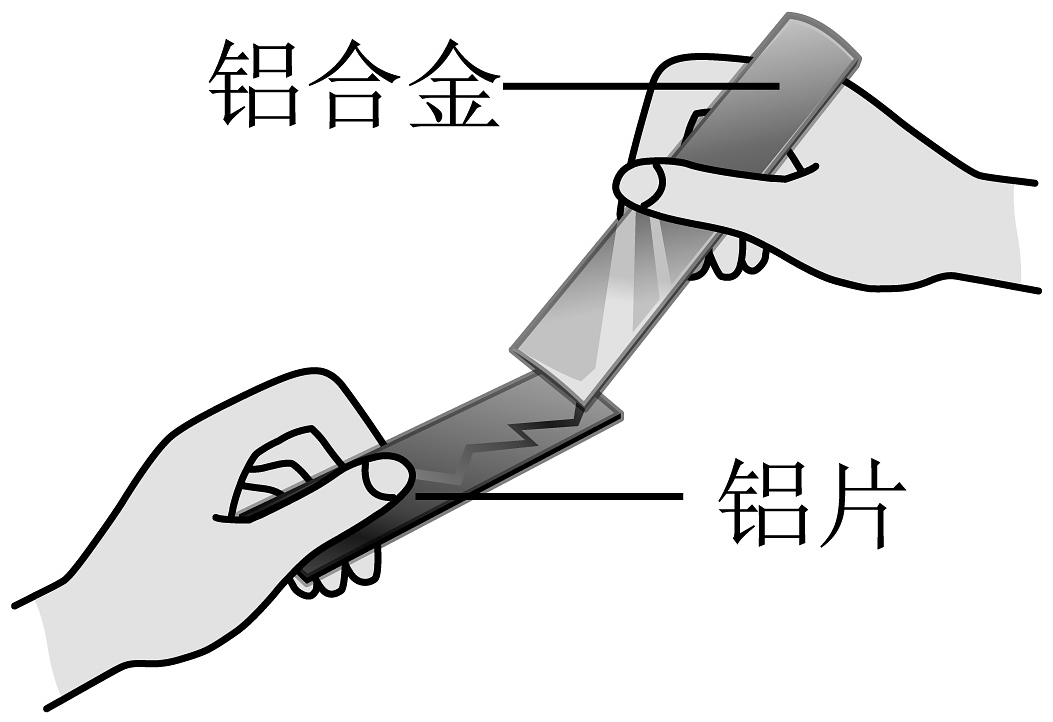
3、下列实验能达到实验目的的是A、比较合金与其组分金属的硬度
 B、探究不同催化剂的催化效果
B、探究不同催化剂的催化效果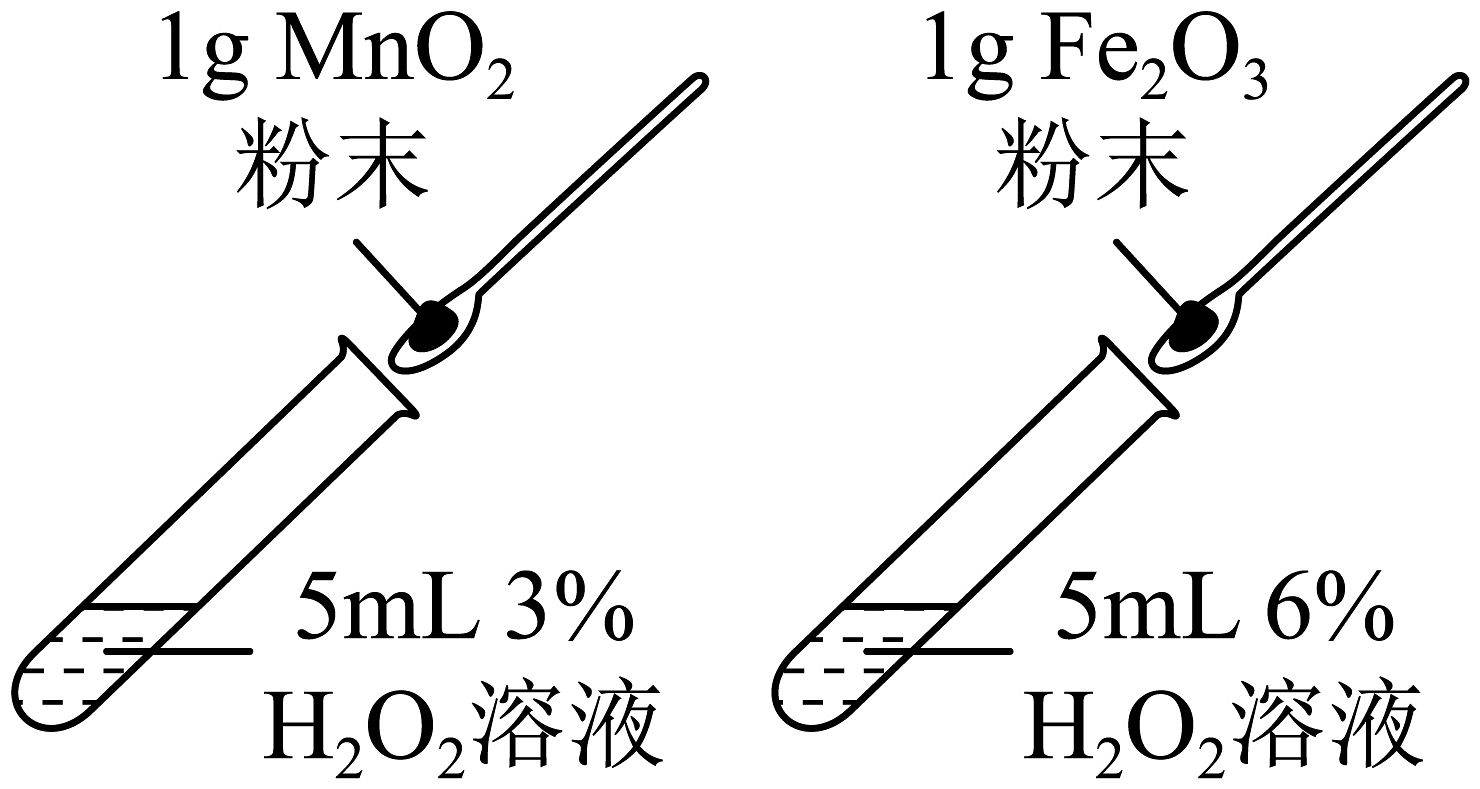 C、证明铜生锈与、和有关
C、证明铜生锈与、和有关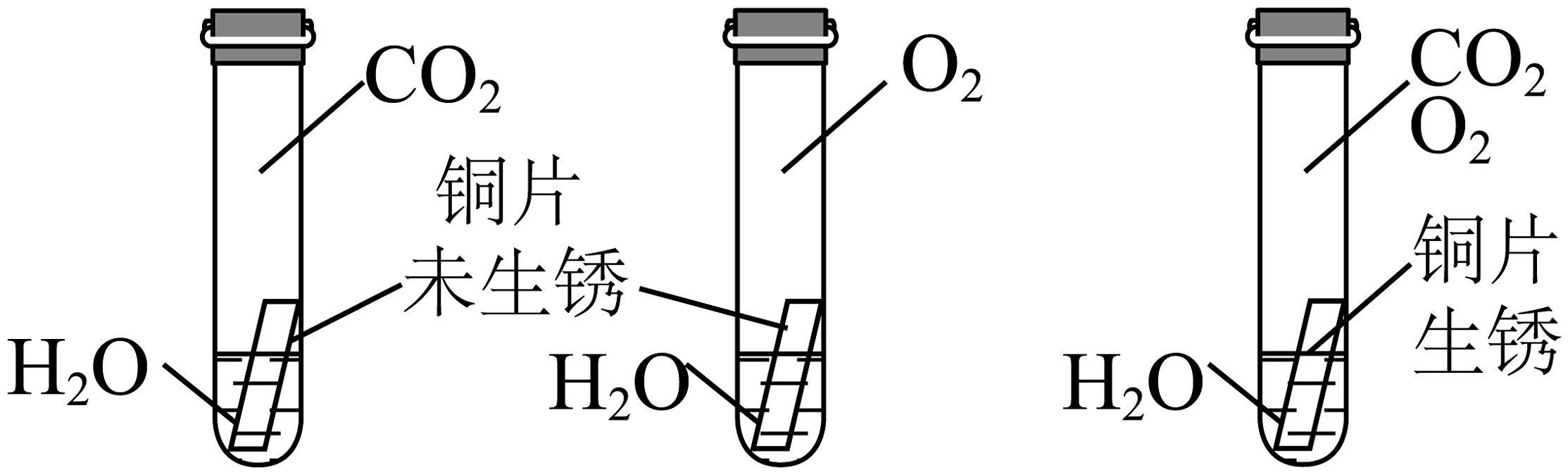 D、验证质量守恒定律
D、验证质量守恒定律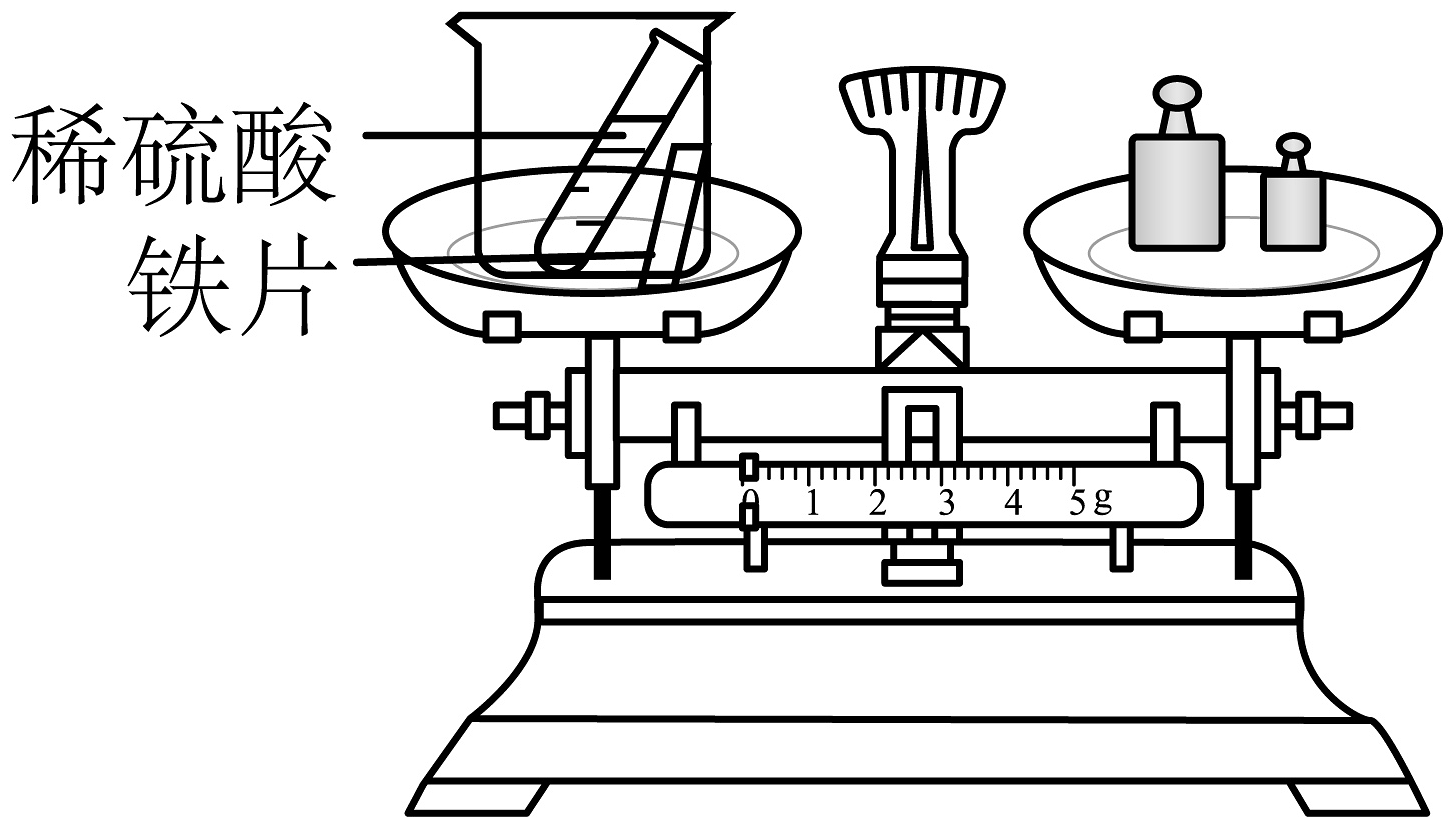
-
4、、KCl可用作钾肥,对大豆的生长具有重要的作用。、KCl的溶解度随温度变化的曲线如图所示,下列有关说法正确的是
 A、溶解度比KCl的大 B、在70℃时,将的饱和溶液降温至40℃,析出 C、d点对应的溶液为饱和溶液 D、e点对应的KCl饱和溶液中溶质的质量分数为40%
A、溶解度比KCl的大 B、在70℃时,将的饱和溶液降温至40℃,析出 C、d点对应的溶液为饱和溶液 D、e点对应的KCl饱和溶液中溶质的质量分数为40% -
5、臭氧()是一种常见的消毒剂。对氧气无声放电可获得臭氧,实验装置和反应的微观示意图如下所示。下列说法正确的是
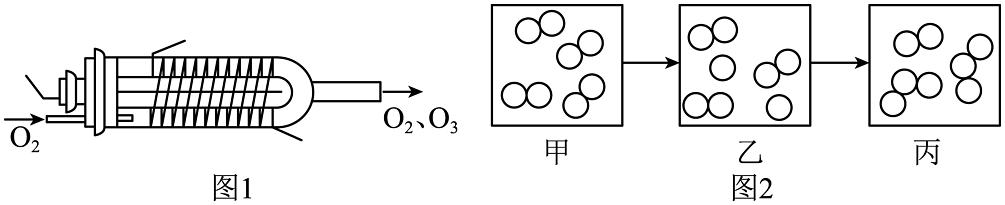 A、图2乙中的粒子均可保持氧气的化学性质 B、图2甲和丙表示的都是纯净物 C、参加反应的反应物和生成物的分子个数比为 D、该反应是化合反应
A、图2乙中的粒子均可保持氧气的化学性质 B、图2甲和丙表示的都是纯净物 C、参加反应的反应物和生成物的分子个数比为 D、该反应是化合反应 -
6、在“天宫课堂”中,航天员王亚平展示了“锆金属熔化与凝固”实验。下图呈现了锆元素在元素周期表中的信息及其原子结构示意图,据此判断,下列说法正确的是
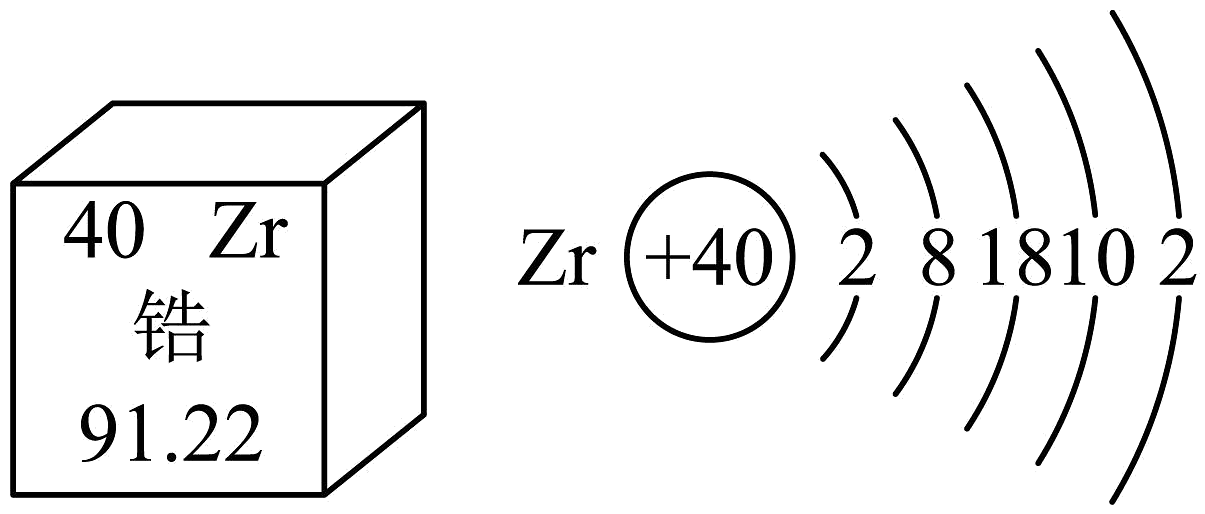 A、锆原子在化学变化中容易得到电子 B、锆元素的相对原子质量为91.22g C、锆原子的中子数为40 D、锆元素是金属元素
A、锆原子在化学变化中容易得到电子 B、锆元素的相对原子质量为91.22g C、锆原子的中子数为40 D、锆元素是金属元素 -
7、华东理工大学在钙钛矿太阳能电池研究领域取得重要突破,创新性地采用单层石墨烯与聚甲基丙烯酸甲酯的复合结构,相关成果处于国际领先水平。聚甲基丙烯酸甲酯的单体为甲基丙烯酸甲酯(化学式 , 结构如图所示),下列关于甲基丙烯酸甲酯()的说法正确的是
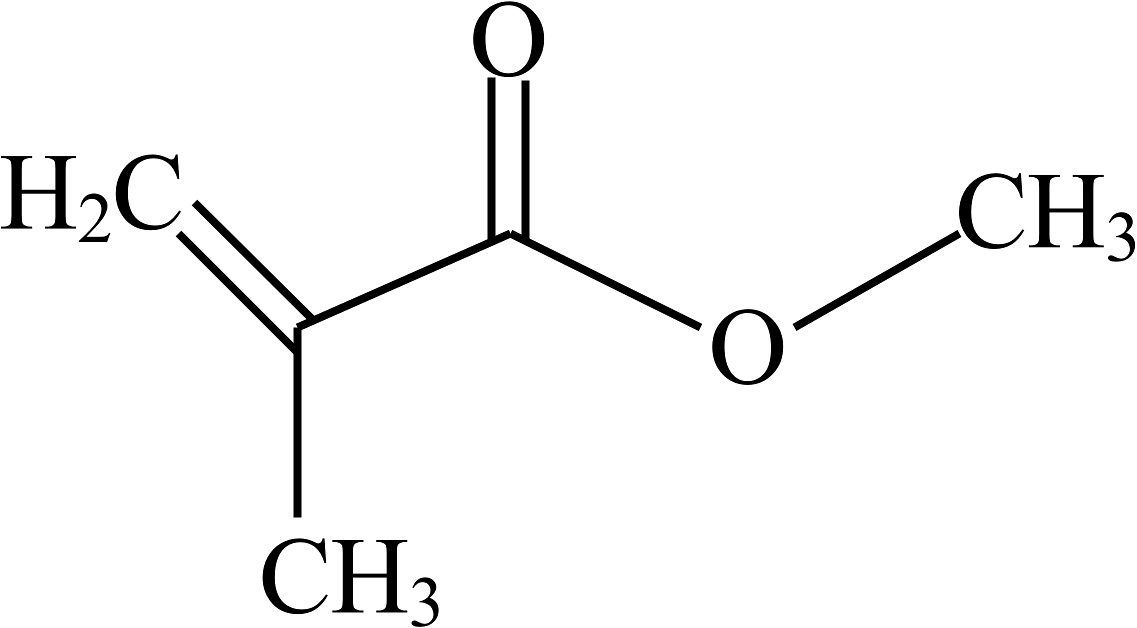 A、由15个原子构成 B、属于氧化物 C、氢元素的质量分数最大 D、碳、氧元素质量比为
A、由15个原子构成 B、属于氧化物 C、氢元素的质量分数最大 D、碳、氧元素质量比为 -
8、嫦娥六号在月球背面展示的国旗的原材料是玄武岩。玄武岩的组成元素有硅、铝、铁、钙、氧等,下列说法及用语表达正确的是
 A、地壳中含量第一的金属元素:Si B、亚铁离子: C、2个钙原子: D、1个氧分子:
A、地壳中含量第一的金属元素:Si B、亚铁离子: C、2个钙原子: D、1个氧分子: -
9、安全是生产生活中的第一要素。2025年春节期间,四川一“小孩哥”将点燃的爆竹扔进化粪池,引发剧烈爆炸,造成路面严重损毁、多辆车辆受损。下列有关安全知识的说法正确的是
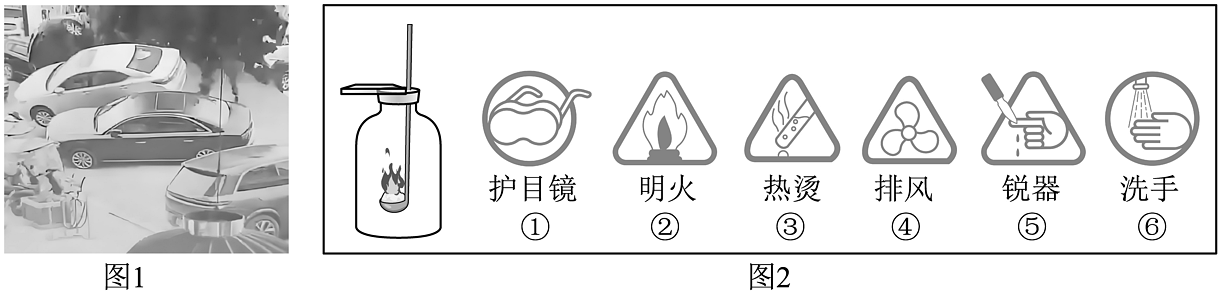 A、用甲醛溶液长期浸泡食物 B、炒菜时油锅中的油着火,可用水浇灭 C、化粪池、面粉加工厂、煤矿井等场所都必须严禁烟火 D、关于硫的燃烧的实验说明,无需标注图2中的③④
A、用甲醛溶液长期浸泡食物 B、炒菜时油锅中的油着火,可用水浇灭 C、化粪池、面粉加工厂、煤矿井等场所都必须严禁烟火 D、关于硫的燃烧的实验说明,无需标注图2中的③④ -
10、以生活垃圾焚烧的飞灰(主要成分为 , 以及少量的、、含化合物等杂质)为原料,通过下列过程制备轻质碳酸钙并回收铜。
 (1)、“浸取”时用溶质质量分数为的溶液浸取飞灰,浸出量随时间变化如图所示。
(1)、“浸取”时用溶质质量分数为的溶液浸取飞灰,浸出量随时间变化如图所示。
①飞灰中与反应的化学方程式为。
②单位时间内,提高浸出量的措施有。
③上图中后,浸出量不升反降的原因是。
(2)、“碳化”过程中生成的化学方程式为。(3)、上述流程中可循环利用的物质有。(4)、每年我国生活垃圾焚烧产生的飞灰中钙元素约为160万吨,钙元素的利用率约为 , 计算理论上每年可获得轻质碳酸钙的质量(写出计算过程) -
11、青铜器是我国古代文明的重要载体。(1)、《周礼·考工记》中记载了铸造各类青铜器的配方。铜和青铜的相关性质见下表。
铜
青铜(含的锡)
青铜(含的锡)
熔点
布氏硬度
350~45
160~200
2000~250
注:布氏硬度的数字越大,表示物质越硬。
①从性能上看,古代常用青铜而非铜铸造工具、武器等的优点有。
②青铜剑身要求锋利坚硬,因此剑身处含锡量要偏(填“高”或“低”)。
(2)、某同学设计实验探究铜锈蚀的条件(如图所示)。一段时间后试管A、B、C中的铜片无明显现象,试管D中的铜片出现了锈蚀现象。
①试管C中加入的气体X是。
②试管D中产生 , 的化学方程式为。
(3)、刚出土的青铜器表面一般都会覆盖一层或多层不同颜色和种类的锈蚀产物。根据对青铜器的锈蚀作用不同,分为无害锈与有害锈。无害锈是指能保护铜基体的锈层,如、等。有害锈会危害青铜器的寿命,如、等。①可表示为 , 则。
②根据有害锈的成分推测该青铜器埋藏的环境中还存在(填离子符号)。
③不稳定,在含氧、潮湿的环境中易转化为和 , 该反应的化学方程式为。
-
12、
盐碱地是重要的土地资源之一。兴趣小组进行了一系列综合实践活动。
【调查土壤的酸碱性】
查阅资料:盐碱地是指土壤中含有过量的氯化钠、硫酸钠、碳酸钠等物质,导致土壤盐分高、碱性强。
(1)硫酸钠中阴离子的符号为________。
(2)采集土壤样本并多次测定其浸出液的约为10。
①测定的操作:用玻璃棒蘸取溶液滴在试纸上,与________相比较。
②部分物质的水溶液中滴加无色酚酞试液后的现象如下表所示。导致盐碱地土壤呈碱性的物质是________(填化学式)。
氯化钠溶液
硫酸钠溶液
碳酸钠溶液
滴加酚酞后溶液的颜色
无色
无色
红色
(3)当植物细胞液浓度大于外界溶液浓度时细胞会吸水,反之则细胞会失水。从生物学角度分析普通植物难以在盐碱地中存活的原因是________。
【设计盐碱地的改良方案】
(4)淡水灌溉减少盐分。某同学模拟淡水灌溉,向的碳酸钠溶液()中不断加入蒸馏水,并测量溶液的变化。在图中画出溶液随加水体积的变化曲线。

(5)施用改良剂——石膏(主要成分为硫酸钙)降低碱性。向的碳酸钠溶液中持续滴加硫酸钙悬浊液至过量,测得混合物的从10.5降为8.5左右。(已知:硫酸钙微溶于水,水溶液呈中性。)
①硫酸钙悬浊液与碳酸钠溶液发生反应的化学方程式为________。
②所得混合物呈弱碱性的原因是________。
-
13、阅读下列材料,回答相关问题。
臭氧()在常温常压时是一种淡蓝色气体,可溶于水,并与水反应生成氧气。在空气中,臭氧的含量非常少。空气中每百万个分子中,臭氧分子不到10个。根据所在位置不同,臭氧既可能会保护地球上的生物,也可能会伤害地球上的生物。大气中,每天都有一些臭氧形成,也有一些臭氧被破坏,其微观示意图如图所示。
科学家发现氟利昂等制冷剂在紫外线的照射下能分解出氯原子()破坏臭氧层,发生的反应为:I.;Ⅱ.。
 (1)、臭氧属于(填“单质”或“氧化物”)。(2)、臭氧和水反应可表示为 , 则X为。(3)、从分子、原子的角度叙述生成臭氧分子的过程。(4)、破坏臭氧的过程中发生改变的是(填字母)。
(1)、臭氧属于(填“单质”或“氧化物”)。(2)、臭氧和水反应可表示为 , 则X为。(3)、从分子、原子的角度叙述生成臭氧分子的过程。(4)、破坏臭氧的过程中发生改变的是(填字母)。a.原子总数 b.分子种类 c.元素种类 d.物质总质量
(5)、氟利昂破坏臭氧层的总反应方程式为。 -
14、某小组进行的性质和制取实验。(1)、利用干冰设计并进行了如下实验探究的性质。

①步骤(Ⅰ)设计的目的是。
②步骤(Ⅱ)中产生白雾的原因是干冰升华(填“吸热”或“放热”)。该白雾是。
③步骤(Ⅲ)中使紫色石蕊试液变红的物质是(填化学式)。
(2)、用大理石和稀盐酸反应制二氧化碳。可供选择的实验装置如图1所示。
①仪器a的名称是。
②制取的化学方程式为。
③发生装置可选用(填字母)。
④用装置D收集气体,将导管伸入瓶底的目的是。
(3)、用图2所示装置测量大理石和稀盐酸反应体系的温度,并用电子天平连续称量反应体系的总质量。测得反应过程中温度和质量随时间的变化如图3所示。
①图2所示装置制取气体,停止反应的操作是。
②图3中时,单位时间内体系总质量减小幅度较大的原因是。
-
15、人类出行方式的演变与化学技术的发展密不可分。(1)、蒸汽机时代以蒸汽汽车、蒸汽火车等为主要交通工具,首次大规模利用化石燃料。
①煤炭燃烧产生、等气体,说明煤炭中一定存在的元素有。
②燃煤产生的上述气体直接排放会导致酸雨的是。
(2)、内燃机革命将燃料升级为汽油(主要成分为)、柴油等石油分馏产品,使热效率提升至。①分子中碳、氢原子个数比为(填最简整数比)。
②内燃机汽车尾气中含有、等有害气体,可用催化转化器转化为无毒的和排放。该反应中氮元素化合价发生的变化为。
(3)、现代,锂电池电动车、氢能自行车等逐渐走进普通人的生活。①锂电池工作时能量转化的主要方式为。
②氢能棒是氢能自行车快速实现换氢补能的关键所在。纯净水理论上能为氢能棒补充的质量为。
(4)、未来,绿色化将重塑可持续出行图景。①固态电池:氮化锂可应用于固态电池。已知中质量比 , 则。
②氨燃料:液氨()燃烧生成氮气和水,该反应的化学方程式为。
-
16、为实现的资源化利用,将捕集的分别转化为甲、乙、丙等燃料,反应过程如图所示。下列说法不正确的是
 A、产物甲的化学式为 B、第一步是在催化剂表面失去转化为 C、第二步分别转化为甲、乙、丙时均生成了丁 D、已知生成1个乙分子时有2个参加反应,则生成1个丙分子时,需要有4个参加反应
A、产物甲的化学式为 B、第一步是在催化剂表面失去转化为 C、第二步分别转化为甲、乙、丙时均生成了丁 D、已知生成1个乙分子时有2个参加反应,则生成1个丙分子时,需要有4个参加反应 -
17、常温下,向和的混合溶液中逐滴加入一滴管溶液,产生红褐色沉淀,搅拌后沉淀消失;继续滴加三滴管溶液,搅拌后仍有沉淀。下列说法正确的是
 A、滴加溶液前,烧杯内溶液中的阳离子只有 B、滴加溶液至沉淀完全时,烧杯内溶液中一定有 C、滴加溶液的过程中,烧杯内溶液的酸性逐渐增强 D、滴加溶液的过程中,烧杯内溶液中含有的数目不断减少
A、滴加溶液前,烧杯内溶液中的阳离子只有 B、滴加溶液至沉淀完全时,烧杯内溶液中一定有 C、滴加溶液的过程中,烧杯内溶液的酸性逐渐增强 D、滴加溶液的过程中,烧杯内溶液中含有的数目不断减少 -
18、将镁条和稀盐酸先后加入如图1所示的装置中(装置气密性良好),用压强传感器测得密闭容器内压强与时间的关系如图2所示。下列说法正确的是
 A、刚注入盐酸瞬间压强迅速上升是因为产生大量 B、bc段反应速率比ab段反应速率快 C、cd段压强减小是因为温度降低 D、a点和c点溶液中的溶质均只有
A、刚注入盐酸瞬间压强迅速上升是因为产生大量 B、bc段反应速率比ab段反应速率快 C、cd段压强减小是因为温度降低 D、a点和c点溶液中的溶质均只有 -
19、某实验小组设计了如下实验探究过氧化氢分解中二氧化锰的作用。下列说法不正确的是
 A、实验甲中带火星的木条未复燃是因为过氧化氢常温下不分解 B、实验甲、乙说明能加快过氧化氢分解 C、实验乙、丙说明反应前后的化学性质不变 D、要说明是过氧化氢分解的催化剂,还需称量实验前后的质量
A、实验甲中带火星的木条未复燃是因为过氧化氢常温下不分解 B、实验甲、乙说明能加快过氧化氢分解 C、实验乙、丙说明反应前后的化学性质不变 D、要说明是过氧化氢分解的催化剂,还需称量实验前后的质量 -
20、为了证明氢氧化钠和盐酸确实发生了化学反应,下列实验方案的设计合理的是A、向稀氢氧化钠溶液中逐滴加入稀盐酸,测溶液 B、向稀氢氧化钠溶液中加入足量稀盐酸,用玻璃棒蘸取所得溶液,加热蒸干 C、向氢氧化钠固体中逐滴加入稀盐酸,测溶液温度 D、向稀氢氧化钠溶液中逐滴加入稀盐酸,检验混合液中是否含有和