沪教版(全国)初中化学九年级下册期末考试模拟测验卷B卷
试卷更新日期:2026-05-08 类型:期末考试
一、选择题(每题1分,共20分)
-
1. “节能减排、低碳生活”主旨在节约能源和利用清洁能源,减少的排放,下列不符合该主题的是A、利用水力发电 B、发展电动汽车 C、焚烧大量秸秆 D、使用LED节能灯2. 农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如图所示。下列说法错误的是( )
 A、实验操作顺序为④②①⑤③ B、选用100mL量筒量取所需水的体积 C、需称量NaCl的质量为16.0g D、如图操作会导致所配溶液质量分数偏大3. 把下列常见物质分别放入足量水中,充分搅拌,不能形成溶液的是:( )A、面粉 B、醋酸 C、食盐 D、蔗糖4. 下图为某反应的微观示意图。关于该反应的说法正确的是( )
A、实验操作顺序为④②①⑤③ B、选用100mL量筒量取所需水的体积 C、需称量NaCl的质量为16.0g D、如图操作会导致所配溶液质量分数偏大3. 把下列常见物质分别放入足量水中,充分搅拌,不能形成溶液的是:( )A、面粉 B、醋酸 C、食盐 D、蔗糖4. 下图为某反应的微观示意图。关于该反应的说法正确的是( ) A、该反应为置换反应 B、参加反应的a与b的微粒个数比为5:4 C、四种物质均由分子构成 D、b、c、d中氧元素化合价相同5. 用括号内的物质不能区分的一组是( )A、NaCl、NaOH、NH4NO3 三种固体 (水) B、K2CO3、Na2SO4、BaCl2三种溶液 (稀硫酸) C、铁粉、碳粉、氧化铜粉末 (稀盐酸) D、NaOH、NaCl、Na2SO4三种溶液 (酚酞)6. 某化学学习小组的同学讨论辨析以下说法,其中错误的是( )A、梦天舱燃烧科学柜采用甲烷作燃料首次“点火”成功,其反应前后元素种类不变 B、升高温度或减小压强,气体的溶解度均会减小 C、夜间厨房发生煤气泄漏时,应立即开灯检查并打开门窗通风 D、盐酸、硫酸都能使石蕊溶液变红,是因为溶液中都含有氢离子7. 下列有关铁及其化合物的转化关系中,不能实现的是( )A、FeFe3O4 B、Fe2O3FeCl3 C、Fe(NO3)3FeCl3 D、FeFeSO48. 下列实验操作不能达到实验目的的是
A、该反应为置换反应 B、参加反应的a与b的微粒个数比为5:4 C、四种物质均由分子构成 D、b、c、d中氧元素化合价相同5. 用括号内的物质不能区分的一组是( )A、NaCl、NaOH、NH4NO3 三种固体 (水) B、K2CO3、Na2SO4、BaCl2三种溶液 (稀硫酸) C、铁粉、碳粉、氧化铜粉末 (稀盐酸) D、NaOH、NaCl、Na2SO4三种溶液 (酚酞)6. 某化学学习小组的同学讨论辨析以下说法,其中错误的是( )A、梦天舱燃烧科学柜采用甲烷作燃料首次“点火”成功,其反应前后元素种类不变 B、升高温度或减小压强,气体的溶解度均会减小 C、夜间厨房发生煤气泄漏时,应立即开灯检查并打开门窗通风 D、盐酸、硫酸都能使石蕊溶液变红,是因为溶液中都含有氢离子7. 下列有关铁及其化合物的转化关系中,不能实现的是( )A、FeFe3O4 B、Fe2O3FeCl3 C、Fe(NO3)3FeCl3 D、FeFeSO48. 下列实验操作不能达到实验目的的是选项
实验目的
主要实验操作
A
鉴别食醋和酒精
取样,闻气味
B
除去铜粉中少量的铁粉
用磁铁吸引
C
分离 CaCl2 和 CaCO3 粉末
滴加足量的稀盐酸,然后蒸发结晶
D
除去CO中少量的CO2气体
通入石灰乳(浆)
A、A B、B C、C D、D9. 晾晒海水可以得到粗盐(含有氯化镁等杂质),氯化钠和氯化镁(不含结晶水)的溶解度曲线如图,下列叙述错误的是( ) A、海水晒盐是通过蒸发结晶的方法获得粗盐 B、氯化镁溶液从t℃降温到20℃一定会析出氯化镁晶体 C、20℃时,氯化钠饱和溶液中溶质和溶剂的质量比为9:25 D、t℃时,不可能配制成溶质质量分数相等的氯化钠、氯化镁的饱和溶液10. 向盛有一定质量表面被氧化的镁条的烧杯中,慢慢加入一定浓度的盐酸。下列图象能正确反映其对应变化关系的是( )A、
A、海水晒盐是通过蒸发结晶的方法获得粗盐 B、氯化镁溶液从t℃降温到20℃一定会析出氯化镁晶体 C、20℃时,氯化钠饱和溶液中溶质和溶剂的质量比为9:25 D、t℃时,不可能配制成溶质质量分数相等的氯化钠、氯化镁的饱和溶液10. 向盛有一定质量表面被氧化的镁条的烧杯中,慢慢加入一定浓度的盐酸。下列图象能正确反映其对应变化关系的是( )A、 B、
B、 C、
C、 D、
D、
二、填空题(共4题,共30分)
-
11. 以化合价为纵坐标,物质类别为横坐标,绘制的图像叫“价类二维图”。如图是碳元素的“价类二维图”,图中A、B、D、E分别表示不同的物质。

回答下列问题:
(1)、A的单质有多种,写出其中一种的名称。(2)、B、D可相互转化,B和(填化学式)在一定条件下发生化合反应能生成D。(3)、科学家将D进行转化实现资源化利用,其中一种方法是:D+4H2CH4+2X,X的化学式为。(4)、D、E可相互转化,若E是由三种元素组成,写出D→E的一个化学方程式。12. 如图是A、B、C三种固体物质在水中的溶解度曲线,回答下列问题。 (1)、℃时,三种物质的溶解度由小到大的顺序是;(2)、在温度不变的条件下,将C的不饱和溶液变为饱和溶液的方法是(写一种即可)(3)、若A物质中含有少量的B物质,可通过的方法提纯A。13. 2023年4月,考古学家在兵马俑彩绘的研究中发现了绝美“中国紫”。其原料有石英(主要成分是)、石绿(一种铜锈)、硫酸钡和一氧化铅等。(1)、请用化学用语填空:
(1)、℃时,三种物质的溶解度由小到大的顺序是;(2)、在温度不变的条件下,将C的不饱和溶液变为饱和溶液的方法是(写一种即可)(3)、若A物质中含有少量的B物质,可通过的方法提纯A。13. 2023年4月,考古学家在兵马俑彩绘的研究中发现了绝美“中国紫”。其原料有石英(主要成分是)、石绿(一种铜锈)、硫酸钡和一氧化铅等。(1)、请用化学用语填空:①2个氧原子。
②硫酸根离子。
③标出一氧化铅(PbO)中Pb的化合价:。
(2)、芯片的主要成分是硅,下图是工业上以石英砂(主要成分是)为主要原料制取高纯硅的流程。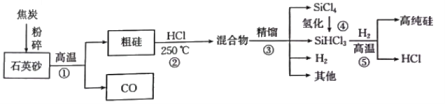
查阅资料:“精馏”是蒸馏的一种,其原理是利用混合物中各成分的沸点不同,将物质分离出来。
①硅的结构与金刚石相似,都是由(选填“分子”“原子”或“离子”)构成的。
②流程中将焦炭粉碎的目的是。
③步骤①中有关反应的化学方程式为。
④为了使资源综合利用,上述流程中可循环使用的物质是(写一种)。
14. 2023年12月,几场大雪给人们的生活带来一些不便,但是它也有很多好处。我们应该善于利用雪的资源,保护生态环境,享受到雪带来的乐趣。(1)、①抓起少量雪,紧紧地握在手心里,雪很快融化成水。雪融化过程中,变化的只是水分子之间的和排列方式。②风雪过后,大型铲雪车日夜轰鸣。铲雪车的铲斗是用锰钢制造的,其中至少含有锰、碳、铁、铬等元素,同时也说明了合金与组成它的纯金属相比,优点之一是硬度(填“大”或“小”)。
③为防止道路结冰,雪后可向路面撒融雪剂。融雪剂有多种,一类是以醋酸钾(CH3COOK)为主要成分的有机融雪剂。196g醋酸钾(CH3COOK)中含碳元素的质量为g。
④乙酸钾可由氢氧化钾或碳酸钾与乙酸发生化学反应制备:2CH3COOH+K2CO3=2CH3COOK+CO2↑+X,则X的化学式为;
⑤环保型的融雪剂多为不含或少含MgCl2、CaCl2的混合物,不合理使用上述含钙、镁化合物的融雪剂的危害是(选填“A、B或C”之一)
A.产生污染性气体 B.使水质硬化 C.难以溶解,不便于清理
(2)、如图是KNO3和NH4Cl的溶解度曲线。试回答下列问题:
①t1℃时,向50g水中加入25g NH4Cl固体,经搅拌充分溶解,所得溶液中溶质与溶剂的质量之比为(填最简整数比)。
②在t2℃时,KNO3的溶解度NH4Cl的溶解度(选填“大于”“等于”“小子”之一)。
③t2℃时,KNO3饱和溶液中溶质的质量分数是(计算结果精确至0.1%)。
④t2℃时,分别将KNO3和NH4Cl两物质的饱和溶液降温至t1℃,降温后两溶液中所含溶质质量大小关系为AB(选填“大于”、“小于”、“等于”或“不能确定”)。
三、推断题(共6分)
-
15. 有ABCDE五种物质,它们之间的转化关系如下图所示。已知A、B组成元素相同,且常温下均为液体:甲是黑色粉末,D在空气中燃烧时产生淡蓝色火焰,组成乙单质的元素原子核内有6个质子, E能使澄清石灰水变浑浊。请回答:
 (1)、甲在该反应中的作用是。(2)、写出的符号表达式为。(3)、经过操作②能得出的一条结论:B是由组成的。(4)、的过程属于(填基本反应类型)。
(1)、甲在该反应中的作用是。(2)、写出的符号表达式为。(3)、经过操作②能得出的一条结论:B是由组成的。(4)、的过程属于(填基本反应类型)。四、流程题(共9分)
-
16. 铁黄(FeOOH)是一种颜料,以某硫铁矿废渣(主要成分 , 含有少量的 , 其余成分不考虑)为原料,制取铁黄,以下是制取工艺流程。
注:铁黄不与水反应,不与水和反应
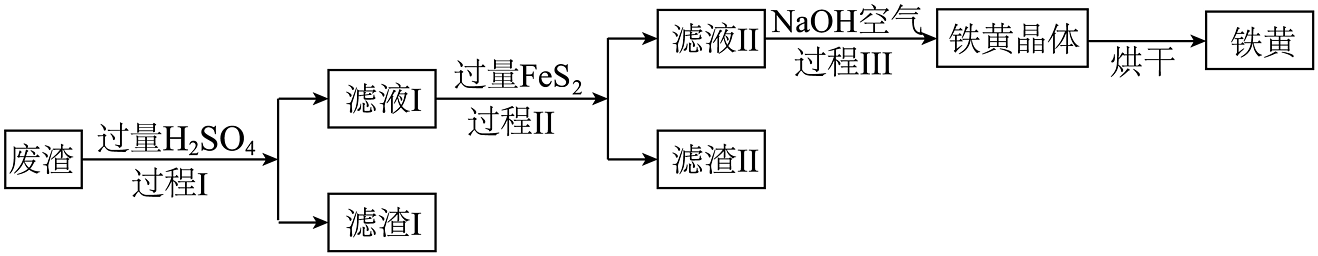 (1)、过程Ⅰ的化学方程式为 , 滤渣Ⅰ中的物质有(填化学式);(2)、过程Ⅱ的操作名称为;(3)、过程Ⅲ中的化学方程式为 , 该反应属于反应(填基本反应类型);(4)、①FeOOH随着温度的升高,可以加热分解成 , 写出其反应的化学方程式;
(1)、过程Ⅰ的化学方程式为 , 滤渣Ⅰ中的物质有(填化学式);(2)、过程Ⅱ的操作名称为;(3)、过程Ⅲ中的化学方程式为 , 该反应属于反应(填基本反应类型);(4)、①FeOOH随着温度的升高,可以加热分解成 , 写出其反应的化学方程式;②温度不同时,生成的颜色如下表:
温度/℃
400
700
750
800
颜色
橘红
鲜红
鲜红
暗红
如果思考乐希希同学想获得鲜红的 , 应把温度控制在。
五、综合题(共13分)
-
17. 请回答下列问题。(1)、钢铁的生产和使用是人类文明和社会进步的一个重要标志。早在春秋战国时期,我国劳动人民就开始生产和使用铁器。随着科学技术的发展,钢铁的冶炼技术水平日益提高,中国的钢铁产量居世界首位。某炼铁厂以焦炭(主要成分为C)、赤铁矿、空气等为主要原料炼铁,反应过程如下:

①在C、CO2、CO三种物质中,碳元素表现的最高化合价是价。CO2和CO化学性质不同的微观实质是。
②写出步骤②中发生反应的化学方程式。
③步骤③中一氧化碳作了该反应的剂。
(2)、我国化学家侯德榜在氨碱法的基础上创立了“侯氏制碱法”。工业上采用侯氏制碱法生产纯碱(Na2CO3),主要流程如下图:
其生产过程中有下列反应:NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl;2NaHCO3Na2CO3+H2O+CO2↑
①下列有关叙述正确的是(选填序号之一)。
A.在加压条件下向饱和氨盐水中通二氧化碳,能加速NaHCO3的生成
B.析出NaHCO3晶体后的溶液为NaHCO3的不饱和溶液
C.该条件下NaHCO3的溶解度比NH4Cl的大
D.第一步反应中,析出NaHCO3晶体后的溶液中只有一种溶质
②用的分离方法将生成的NaHCO3晶体从溶液中分离出来。
(3)、溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度。甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:
①甲、乙两种物质中溶解度受温度影响较大的是物质(填“甲”“乙”之一),若乙溶液中混有少量甲,可用(填“降温结晶”“蒸发结晶”之一)方法提纯乙。
②t2℃时,若将25g甲物质加到40g水中,所得甲溶液中溶质和溶液的质量比为(填最简整数比)。
③将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,所得甲物质溶液的溶质质量分数乙物质溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
④t2℃时,将等质量的甲、乙两物质的饱和溶液(均无固体物质剩余)降温到t1℃,溶液的质量较大的是物质的溶液(填“甲”“乙”之一)。
六、实验探究题(共2题,共17分)
-
18. 请结合下图回答问题:
 (1)、仪器①的名称:。(2)、实验室制CO2的反应化学方程式为 , 为方便控制反应的发生和停止,应选择的发生装置是(选填序号)。(3)、FeS2和O2在加热条件下可反应生成SO2如图是实验室利用FeS2制取SO2的装置。
(1)、仪器①的名称:。(2)、实验室制CO2的反应化学方程式为 , 为方便控制反应的发生和停止,应选择的发生装置是(选填序号)。(3)、FeS2和O2在加热条件下可反应生成SO2如图是实验室利用FeS2制取SO2的装置。
①装置J用于收集SO2 , 说明SO2气体的密度(选“小于”或“大于”)空气。
②用化学方程式表示实验中NaOH溶液的作用。
19. 天然气是一种常用的家庭燃料。某同学在帮妈妈做饭时,对天然气在空气中完全燃烧的产物产生浓厚兴趣。他在老师的帮助下展开如下探究。请你回答下列问题。【查阅资料】
天然气的主要成分是甲烷(CH4)。甲烷是①一种无色、无味的气体,②密度比空气小,③极难溶于水,④具有可燃性,燃烧时火焰明亮并呈蓝色。甲烷和空气按一定比例混合,遇明火会发生爆炸。
 (1)、以上信息中,属于甲烷物理性质的是(填序号)。(2)、【提出问题】
(1)、以上信息中,属于甲烷物理性质的是(填序号)。(2)、【提出问题】甲烷在空气中完全燃烧,产物是什么?
【猜想与假设】
根据甲烷的元素组成,推测甲烷在空气中完全燃烧生成二氧化碳和一种一定含元素的物质。做出这一推测的理论依据是。(3)、【收集证据】
点燃纯净的甲烷,在火焰上方罩一只干冷的烧杯,烧杯内壁出现 , 用手触摸烧杯壁有发烫的感觉。将烧杯迅速翻转,倒入少量澄清石灰水,振荡,观察到澄清石灰水变浑浊。(4)、【获得结论】甲烷在空气中完全燃烧,产物是二氧化碳和水。
点燃甲烷,发生反应的化学方程式为。(5)、为了及时发现天然气泄露,可在燃气中添加乙硫醇作加臭剂。乙硫醇是最臭的物质之一,空气中仅含五百亿分之一时,其臭味就可嗅到。用分子的观点解释人们闻到臭味的原因是。(6)、为防止天然气泄漏造成危险,应在厨房安装天然气泄漏报警器,安装位置应在燃气灶附近墙壁的(选填“上方”或“下方”)。七、计算题(共5分)
-
20. 兴趣小组做了氢氧化钠溶液和硫酸铜溶液反应的定量实验,向192g硫酸铜溶液中逐滴加入氢氧化钠溶液,所加氢氧化钠溶液与生成沉淀的质量关系如图所示:

化学方程式为:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
(1)、恰好完全反应时,生成沉淀为g。(2)、请计算硫酸铜溶液中溶质的质量。(3)、请计算恰好完全反应时,所得不饱和溶液中溶质的质量分数。
-
-
-