-
1、回答“氧气的实验室制取”实验中的相关问题。
 (1)、仪器a的名称是。(2)、实验室用加热高锰酸钾的方法制取O2。
(1)、仪器a的名称是。(2)、实验室用加热高锰酸钾的方法制取O2。①该反应的化学方程式为;
②用该方法制取O2的发生装置应选择图1中的装置(填序号)。
(3)、将图2中的仪器组装成收集装置,与选择的发生装置相连,制取氧气。实验完成后,老师对“组装收集装置”和“收集气体”的过程进行点评,上述两个过程中的一些错误操作,可能会影响收集到氧气的浓度,例如“未验满就停止收集”。请再写出两点可能导致收集到氧气的浓度偏低的错误操作:。 -
2、中科院李灿院士团队在二氧化碳制甲醇(化学式为CH3OH,甲醇是内燃机的理想燃料之一)的研究方面取得了新进展,该反应的微观示意图如下。
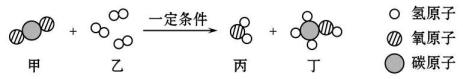 (1)、 图中表示CH3OH的是(填序号)。(2)、该反应的化学方程式为。(3)、若该反应生成的两种物质中氧元素的总质量为16g,则参加反应的氢气的质量为g(可能用到的相对原子质量: H——1 C——12 O——16)。(4)、该反应的应用价值是(答一条)。
(1)、 图中表示CH3OH的是(填序号)。(2)、该反应的化学方程式为。(3)、若该反应生成的两种物质中氧元素的总质量为16g,则参加反应的氢气的质量为g(可能用到的相对原子质量: H——1 C——12 O——16)。(4)、该反应的应用价值是(答一条)。 -
3、在农业生产中,可利用不同溶质质量分数的NaCl溶液选种。
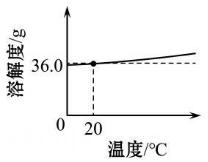 (1)、NaCl在水中的溶解有限度。右图为NaCl的溶解度曲线。
(1)、NaCl在水中的溶解有限度。右图为NaCl的溶解度曲线。①NaCl的溶解度随温度升高而;
②20℃时, NaCl的溶解度是 g。
(2)、若用NaCl固体和水配制100kg溶质质量分数为16%的NaCl溶液, 需要NaCl固体的质量是 kg。 -
4、五行传千载,变化藏其中。“‘金、木、水、火、土’五行相生相克”是古人对物质及物质之间关系最朴素的认知。
 (1)、木生火 (木燃烧生成火)。木柴能燃烧,从“燃烧的条件”分析,木柴是。(2)、火生土 (火燃烧后变成灰烬)。将秸秆晒干烧灰,……即得到草木灰 (含有碳酸钾)。碳酸钾属于“氮肥”“磷肥”“钾肥”中的肥。(3)、土生金(矿石冶炼得到金属)。“火法炼锌”过程中应用的原理之一为: 其反应类型是反应。(4)、金生水(金属能凝聚水蒸气而成水)。水蒸气在温度较低的金属表面液化成水,该过程中水分子间的间隔变。(5)、水生木(用水灌溉,树木生长)。除水外,再写一条影响植物生长的因素:。(6)、与现代化学理论相比, “五行学说”具有一定的局限性。试举一例说明其局限性: 。
(1)、木生火 (木燃烧生成火)。木柴能燃烧,从“燃烧的条件”分析,木柴是。(2)、火生土 (火燃烧后变成灰烬)。将秸秆晒干烧灰,……即得到草木灰 (含有碳酸钾)。碳酸钾属于“氮肥”“磷肥”“钾肥”中的肥。(3)、土生金(矿石冶炼得到金属)。“火法炼锌”过程中应用的原理之一为: 其反应类型是反应。(4)、金生水(金属能凝聚水蒸气而成水)。水蒸气在温度较低的金属表面液化成水,该过程中水分子间的间隔变。(5)、水生木(用水灌溉,树木生长)。除水外,再写一条影响植物生长的因素:。(6)、与现代化学理论相比, “五行学说”具有一定的局限性。试举一例说明其局限性: 。 -
5、铁和铁合金作为金属材料一直被广泛应用。(1)、钢是铁合金。钢的硬度比纯铁。(2)、写出一种生活中的铁制品:。(3)、铁能与空气中的水和发生化学反应生成铁锈(主要成分是 因此,生活中我们应采取相应措施防止铁制品生锈。(4)、用CuSO4配制波尔多液时,不能使用铁制容器,原因是 铁可以把铜从CuSO4溶液中置换出来,说明铁的金属活动性比铜。
-
6、元素周期表是学习和研究化学的重要工具。结合元素周期表(部分)回答下列问题。
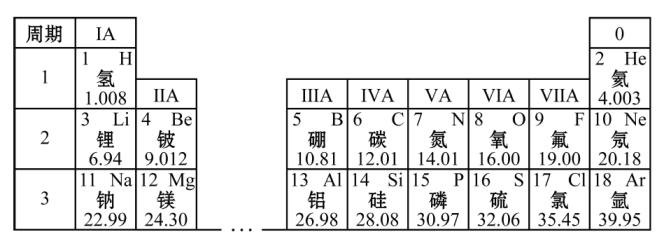 (1)、用化学用语填空:
(1)、用化学用语填空:①磷元素的符号;② 2个氧原子。
(2)、 13号元素的相对原子质量是。(3)、在我国近代化学启蒙者徐寿与他人合译的《化学鉴原》中,元素名称用字有规律,从偏旁就可以知道它们属于哪一类元素,如钠元素属于元素。(4)、含碳的化合物种类繁多,其中二氧化碳的化学式为CO2。请你根据以上内容,结合二氧化碳的化学式,写出获取的三条信息:。 -
7、元素化合价和物质类别是认识物质的两个重要维度。右图是硫元素“价类二维图”。下列说法错误的是( )
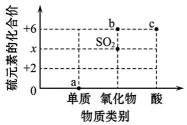 A、x为 +3 B、SO3对应的点是b点 C、a点对应的物质在氧气中燃烧生成 SO2 D、锌与c点对应物质的稀溶液反应能生成氢气
A、x为 +3 B、SO3对应的点是b点 C、a点对应的物质在氧气中燃烧生成 SO2 D、锌与c点对应物质的稀溶液反应能生成氢气 -
8、 某医用冷敷袋的内部结构如右下图。使用时挤压冷敷袋,内包装膜破裂,里面的水接触到夹层中的NH4NO3 , 温度降低。下列说法错误的是( )
 A、用于制作外包装袋的塑料属于金属材料 B、与外包装袋相比,内包装膜更易破裂 C、NH4NO3溶于水时吸热使温度降低 D、运输、储存该医用冷敷袋时应防止挤压
A、用于制作外包装袋的塑料属于金属材料 B、与外包装袋相比,内包装膜更易破裂 C、NH4NO3溶于水时吸热使温度降低 D、运输、储存该医用冷敷袋时应防止挤压 -
9、化学小组利用“沉降”“过滤”“吸附”等方法净化伊通河水样。向水样中加入明矾沉降后,再使用下图简易净水装置进行净化处理。下列说法错误的是( )
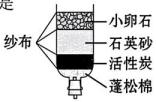 A、明矾可使水样中悬浮的杂质较快沉降。 B、小卵石、石英砂可过滤水样中的不溶性杂质 C、活性炭可吸附水样中的异味 D、经该图装置净化处理后的水样是纯净物。
A、明矾可使水样中悬浮的杂质较快沉降。 B、小卵石、石英砂可过滤水样中的不溶性杂质 C、活性炭可吸附水样中的异味 D、经该图装置净化处理后的水样是纯净物。 -
10、生产中用氧炔焰切割金属,其反应原理: x 的值是( )A、1 B、2 C、3 D、4
-
11、 与“粗盐中难溶性杂质的去除”实验有关的图标中,表示“进行化学实验需戴好护目镜”的是( )A、
 B、
B、 C、
C、 D、
D、
-
12、 2025年中国环境日的主题是“美丽中国我先行”。下列做法不符合这一主题的是( )A、积极植树造林 B、践行节约用水 C、坚持绿色出行 D、随意丢弃垃圾
-
13、 取用一定量的液体试剂时,常用量筒量出体积。下列读数的方法正确的是( )A、
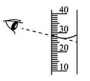 B、
B、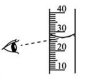 C、
C、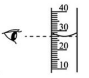 D、
D、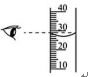
-
14、 下列饮品,每100mL中蛋白质含量较多的是( )A、菊花茶 B、纯牛奶 C、矿泉水 D、苹果汁
-
15、 人类的生活离不开空气。空气中可供给呼吸的气体是( )A、氮气 B、氧气 C、稀有气体 D、二氧化碳
-
16、 《天工开物》记载了古代制砖的工艺。下列制砖环节中,材料发生化学变化的是( )A、择地取土 B、入模定型 C、烧坯成砖 D、修整轮廓
-
17、
硫氧粉(化学式为Na2SO3)是一种易溶于水的固体,在食品、印染等行业中有着广泛应用,但易被氧气氧化为Na2SO4。化学兴趣小组对硫氧粉开展了以下探究。
资料1:Na2SO3与稀硫酸、稀盐酸能发生类似于Na2CO3与稀硫酸、稀盐酸的反应。
资料2:BaSO3与BaSO4均为白色沉淀,BaSO3能溶于盐酸,BaSO4不能溶于盐酸。
资料3:SO2与NaOH溶液能发生类似于CO2与NaOH溶液的反应;SO2还能使品红溶液褪色。

【认识类别】
(1)图1表示硫元素化合价与物质类别的关系图,图中点(填字母)所对应的物质是。
I、探究硫氧粉的性质
【实验1】
(2)探究硫氧粉与酸的反应。小组同学用如图2所示的装置①进行实验:打开活塞,向硫氧粉中加入稀硫酸,将产生的气体通入图2的装置(选②或③),通过现象可知气体中有点所对应的物质,请写出与稀硫酸反应的化学方程式。
【实验2】探究硫氧粉与盐的反应。小组甲同学进行了如图3所示的实验:取少量硫氧粉于试管中加水,振荡使其全部溶解;再向其中加入适量的溶液,振荡。
【实验现象】试管中产生白色沉淀。
【实验结论】能与发生反应生成沉淀。
【实验3】
(3)小组乙同学认为白色沉淀中可能含有硫酸钡。请设计实验验证之并完成实验报告。
实验步骤
实验现象
实验结论
向实验2后的试管中继续加入
白色沉淀中含有硫酸钡
II、探究硫氧粉的制备
【制备原理】小组同学经查阅资料得知:可将持续通入到溶液中制备硫氧粉。
【组成分析】
(4)制备过程中溶液组成的变化如图4所示。

①反应初期(B点以前)反应的化学方程式为。
②的通入量控制在点时,使得产量最高。
III、测定硫氧粉中的含量
【确定成分】小组同学取了一瓶久置的工业硫氧粉,经查阅资料确定其成分为Na2SO3、和。
【进行测定】小组同学根据成分设计了如图5所示的实验流程进行了含量测定。

已知:过氧化氢溶液只与硫氧粉中Na2SO3反应并将其转化为。
说明:操作1和2均为过滤、洗涤、干燥和称量。
【得出结论】
(5)经计算可知样品中的质量分数为。
【反思评价】使用硫氧粉时需要注意密封保存。
-
18、如图所示,是初中化学中的常见物质,分别是由、、、、、、、、、中的一种或几种元素组成。J为单质,、、、由两种元素组成,其余物质均由三种元素组成,其中、的物质种类相同。、、、分别加入水中,得到的溶液都呈碱性,其中的俗称是火碱。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物和反应条件已略去。
 (1)、写出化学式:A , H。(2)、写出反应的化学方程式:。(3)、写出反应的化学方程式:。
(1)、写出化学式:A , H。(2)、写出反应的化学方程式:。(3)、写出反应的化学方程式:。 -
19、硫酸锌可作为食品添加剂。工业上常用菱锌矿(主要成分是 , 并含少量的、和等)生产硫酸锌,生产流程如下图所示(假设每一步骤反应均完全)。
 (1)、将块状菱锌矿粉碎的目的是。(2)、氧化过程中硫酸参与反应,转化为 , 同时有生成,写出该过程的化学反应方程式。(3)、除铜过程中金属是 , (填化学式,下同)滤渣中含有的金属单质有。(4)、锌与稀硫酸反应也可以获得硫酸锌,现要制备硫酸锌,需要溶质质量分数为9.8%的稀硫酸多少克?(写出计算过程)
(1)、将块状菱锌矿粉碎的目的是。(2)、氧化过程中硫酸参与反应,转化为 , 同时有生成,写出该过程的化学反应方程式。(3)、除铜过程中金属是 , (填化学式,下同)滤渣中含有的金属单质有。(4)、锌与稀硫酸反应也可以获得硫酸锌,现要制备硫酸锌,需要溶质质量分数为9.8%的稀硫酸多少克?(写出计算过程) -
20、
航天器中通常使用氢氧化锂(化学式为)固体吸收来降低其浓度净化空气。化学小组对氢氧化锂开展了以下项目式学习。
已知:和的化学性质相似。
任务一:认识的性质
(1)请写出固体吸收的化学反应方程式________。
(2)、均可作的吸收剂。相同条件下,两种吸收剂的质量与吸收的最大质量的关系如图所示。据图分析,选用作航天器吸收剂的原因是________。

任务二:了解的制备
工业上用电解法制得含的溶液,在保护下将混合溶液蒸发结晶,可得到晶体。和在不同温度时的溶解度如下表所示。已知:电解法制得的溶液中,的质量分数为10%、的质量分数为5%。
温度/℃
20
30
40
50
60
溶解度
12.8
12.9
13.0
13.3
13.8
109
118
129
146
177
(3)20℃时,将溶液恒温蒸发溶剂,当剩余水的质量为时,所得溶液是的________(填“饱和”或“不饱和”)溶液。
(4)从该溶液获取时选用蒸发结晶法而不选用冷却结晶法的理由是________;在蒸发结晶中的作用是________。
任务三:配制溶液
工业上可用溶质质量分数为1%的溶液的去除金属表面的油污。现配制溶质质量分数为1%的溶液,实验步骤如下图所示:

(5)进行溶液配制的正确操作顺序是______(填序号)。
A. ④⑤①②③ B. ①②③④⑤ C. ③④①②⑤ D. ②①④③⑤ (6)转移已配好的溶液时,有少量溶液溅出,则所配制的溶液溶质质量分数________。(填“偏大”或“偏小”或“无影响”)