相关试卷
- 备战2026中考2021-2025中考化学专题汇编精选 专题10 燃烧及灭火 能源的开发利用
- 沪教(全国)版初中化学九年级下学期期中模拟测试卷A卷
- 沪教(全国)版初中化学九年级下学期期中模拟测试卷B卷
- 人教版初中化学九年级下册期中考试模拟测验卷A卷
- 人教版初中化学九年级下册期中考试模拟测验卷B卷
- 科粤版初中化学九年级下册期中模拟测试卷A卷
- 科粤版初中化学九年级下册期中模拟测试卷B卷
- 备战2026中考2021-2025中考化学专题汇编精选 专题09 碳和碳的氧化物
- 备战2026中考2021-2025中考化学专题汇编精选 专题08 质量守恒定律和化学方程式
- 湖南省岳阳市2026年初中化学学业水平考试适应性测试
-
1、化学变化的本质特征是A、有颜色变化 B、有气体放出 C、发光、发热 D、有新物质生成
-
2、科学家经过多年研究证明,有一些同学爱吃的小包装零食中,含一定量的有毒、有害、致病的化学物质,如某些油炸食品中含有致癌物质丙烯酰胺(C3H5ON)。请你根据丙烯酰胺(C3H5ON)的化学式计算后填写:
(1)丙烯酰胺(C3H5ON)的相对分子质量为_________________;
(2)碳元素和氧元素的质量比是____________________;
(3)氧元素的质量分数为_________________。
(4)142克丙烯酰胺(C3H5ON)中碳元素的质量为__________克。
-
3、根据下列实验装置图,回答问题。
 (1)、图中仪器a的名称是。(2)、用高锰酸钾制取氧气的文字表达式为 , 应用的发生装置为(填字母序号,下同)。(3)、用二氧化锰和过氧化氢溶液制取氧气,应选择的发生装置为。(4)、为了获得较为干燥的氧气,应选用的收集装置为。(5)、铁丝在氧气中燃烧实验中,集气瓶中要预留一些水,原因是 , 该实验的现象是。
(1)、图中仪器a的名称是。(2)、用高锰酸钾制取氧气的文字表达式为 , 应用的发生装置为(填字母序号,下同)。(3)、用二氧化锰和过氧化氢溶液制取氧气,应选择的发生装置为。(4)、为了获得较为干燥的氧气,应选用的收集装置为。(5)、铁丝在氧气中燃烧实验中,集气瓶中要预留一些水,原因是 , 该实验的现象是。 -
4、水是生命之源,也是人类最宝贵的资源。用你学过的化学知识回答下列问题:(1)、从物质的分类角度分析,水不属于(填字母)。
a.单质 b.氧化物 c.化合物 d.纯净物
(2)、欲除去水中不溶性杂质,需进行的操作是。(3)、硬水中含有较多可溶性钙、镁化合物,硬水会给生活和生产带来许多麻烦。生活中可用方法来降低水的硬度。(4)、根据如下图回答下列问题:
试管A中的气体的名称是 , 写出电解水反应的文字表达式 , 该实验证明水是由组成的。
(5)、通常向自然界中的水投放高铁酸钠(化学式为 Na2FeO4)杀菌消毒,高铁酸钠中铁元素的化合价为 。(6)、我国有关部门规定,净化后进入用户的饮用水含铁<0.3mg·L-1 , 含铜<1.0mg·L-1。其中的“铁、铜”指的是___________(填正确选项前的字母)。A、原子 B、分子 C、元素 -
5、根据下列粒子的结构示意图,回答问题。

(1)达到稳定结构的粒子是(填序号,下同);
(2)表示同一种元素的粒子是;
(3)在化学反应中容易失去电子的粒子是;
(4)表示阴离子的是;
(5)B微粒变为稳定结构后,质子数为 , 核外有个电子层;
(6)C、E形成的化合物的化学式为。
-
6、用化学用语填空:(1)、4个硝酸根离子;(2)、5个水分子;(3)、3个亚铁离子;(4)、标出氧化钙中钙元素的化合价;(5)、保持二氧化碳化学性质最小的粒子是。
-
7、下图是表示某气体分子的示意图,图中“
 ”和“
”和“ ”分别表示两种不同质子数的原子,其中可以表示单质的是 A、
”分别表示两种不同质子数的原子,其中可以表示单质的是 A、 B、
B、 C、
C、 D、
D、
-
8、学习化学需要进行化学实验。下列实验操作错误的是A、
 滴加液体
B、
滴加液体
B、 添加酒精
C、
添加酒精
C、 加热液体
D、
加热液体
D、 放置试管
放置试管
-
9、下列变化与其他变化有本质区别的是( )A、酒精燃烧 B、粉笔折断 C、灯泡发光 D、玻璃破碎
-
10、下列实验操作中,错误的是A、
 B、
B、 C、
C、 D、
D、
-
11、发现元素周期律的科学家是A、拉瓦锡 B、张青莲 C、门捷列夫 D、阿伏加德罗
-
12、分类是学习化学的重要方法,下列分类正确的是A、纯净物:水蒸气、五氧化二磷 B、混 合 物:洁净的空气、铁水 C、化合物:二氧化碳、硫 D、氧化物:高锰酸钾、氧化铁
-
13、实验室有一瓶含杂质的氯酸钾,某兴趣小组的同学利用该药品和二氧化锰制取氧气(杂质不溶于水也不参加反应),实验数据如下图,请回答下列问题:
 (1)、a=g。(2)、小组同学欲从反应后的剩余固体中回收二氧化锰,主要操作步骤为加水溶解、、洗涤、干燥。(3)、计算受热分解的氯酸钾的质量(写出计算过程)。
(1)、a=g。(2)、小组同学欲从反应后的剩余固体中回收二氧化锰,主要操作步骤为加水溶解、、洗涤、干燥。(3)、计算受热分解的氯酸钾的质量(写出计算过程)。 -
14、某化学兴趣小组利用图a所示装置,探究分子运动及其特点,利用相对湿度传感器测定等体积的冷水和热水上方空气的湿度,实验结果如图b,下列说法错误的是
 A、该实验不仅能证明分子在不断运动,还能证明分子运动速率和温度的关系 B、曲线①为烧杯A上方测定的实验数据 C、该创新实验凸显了数字化实验的优势而且绿色环保 D、液面上方水分子间隔大于液面下方水分子间隔
A、该实验不仅能证明分子在不断运动,还能证明分子运动速率和温度的关系 B、曲线①为烧杯A上方测定的实验数据 C、该创新实验凸显了数字化实验的优势而且绿色环保 D、液面上方水分子间隔大于液面下方水分子间隔 -
15、月球的土壤中吸附着数百万吨的氦(He-3),其原子核中质子数为2,中子数为1,下列关于氦(He-3)元素的说法正确的是A、原子核外电子数为3 B、原子的质量为2 C、原子的核电荷数为3 D、原子的相对原子质量为3
-
16、规范的实验操作是实验成功的保证,请回答下列问题。(1)、胶头滴管用过后应 , 再去吸取其他试剂。(2)、倾倒细口瓶里的液体后,标签被腐蚀、字迹模糊,原因可能是。(3)、取用7.2mL蔗糖水需要用到的仪器有(填序号)。
①5mL量筒②10mL量筒③20mL量筒④胶头滴管⑤玻璃棒
-
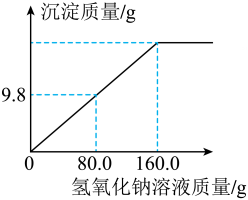
17、在化学校本实验活动中,小明同学取100.0g硫酸铜溶液置于烧杯中,再向烧杯中逐滴加入质量分数为10.0%的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。回答下列问题:
 (1)、用已知浓度和质量分数的溶液配制一定质量和质量分数的稀溶液,实验步骤:
(1)、用已知浓度和质量分数的溶液配制一定质量和质量分数的稀溶液,实验步骤:
Ⅰ.计算;Ⅱ.量取;Ⅲ.混匀;Ⅳ.装瓶。该取液体的体积时,视线应与量筒内液体保持水平;(2)、恰好完全反应时,生成沉淀的质量为g;(3)、恰好完全反应时,计算所得溶液中溶质质量分数。(写出计算过程,结果精确到0.1%) -
18、草木灰中含有碳酸钾,还可能含有硫酸钾、硫酸钾中的一种或两种。某化学兴趣小组对草木灰的成分进行了探究。
【作出猜想】草木灰中可能含有碳酸钾、硫酸钾中的一种或两种。
(1)、【设计实验】小组同学取适量草木灰于烧杯中,加入足量蒸馏水浸泡、搅拌、过滤,得到澄清草木灰水,备用。
甲同学:取少量草木灰水置于试管中,滴加足量稀硫酸,有大量气泡产生。由此得出草木灰中含有碳酸钾,发生反应的化学方程式为。
乙同学:取少量草木灰水于试管中,滴加足量氯化钡溶液,产生白色沉淀,结合甲同学的实验,得出草木灰中含有硫酸钾和碳酸钾的结论。
(2)、【提出质疑】丙同学认为乙同学结论不正确,理由是(用化学方程式表示)。(3)、【探究实验】请你和同组同学一起设计实验方案,帮助乙同学得到实验结论(将实验操作及实验现象填入相应的空格中):
实验操作
实验现象
实验结论
草木灰中含有硫酸钾和硫酸钾
(4)、【拓展应用】活动二:草木灰中碳酸钾含量的测定(假设草木灰中其他成分遇稀硫酸不产生气体)
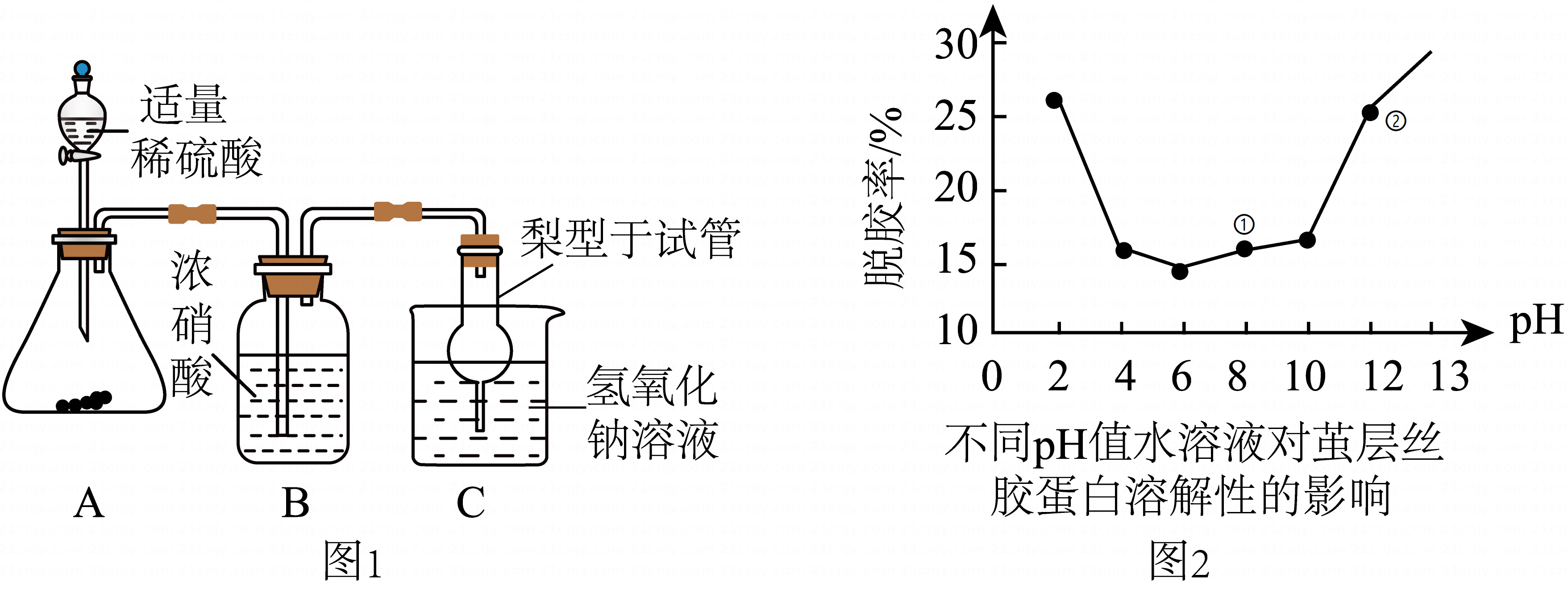
丁同学称取一定质量活动一剩余的草木灰,利用已检查好气密性的图1装置进行定量实验,测得草木灰中碳酸钾的质量分数为10.0%,查阅资料后,发现测得的数值偏小,可能的原因是。
 (5)、【拓展应用】
(5)、【拓展应用】脱胶率越高,所得的丝帛越顺滑亮丽,根据图2分析,清洗油烟机坠油时,选用(填序号)洗涤剂效果更好。
-
19、化学是一门以实验为基础的科学。结合所学知识回答下列问题:
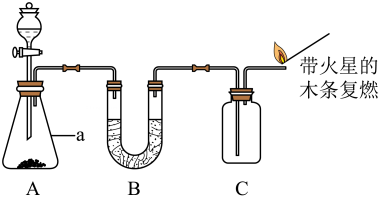 (1)、仪器a的名称。(2)、由图判断,装置A中反应的化学方程式为;下列与实验有关的图标,在该实验中无需标注的是(填序号)。
(1)、仪器a的名称。(2)、由图判断,装置A中反应的化学方程式为;下列与实验有关的图标,在该实验中无需标注的是(填序号)。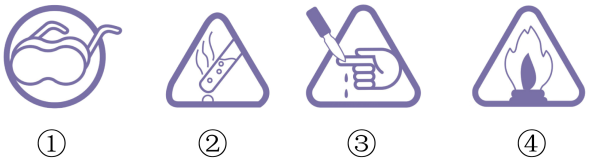 (3)、可用装置C收集气体,说明该气体可能具有的物理性质是。
(3)、可用装置C收集气体,说明该气体可能具有的物理性质是。 -
20、锌是维持生命活动的重要元素之一,目前工业上主要采用“酸法”冶炼锌,一兴趣小组以菱锌矿(主要成分是ZnCO3 , 还含有少量的SiO2和为原料制备锌,其工艺流程图如下。回答下列问题:
 (1)、菱锌矿属于(填“纯净物”或“混合物”)。(2)、由此流程可推知SiO2的性质有( )(填字母序号)。A、难溶于水 B、化学性质很活泼 C、不能与稀硫酸反应(3)、“酸浸”时,金属氧化物发生反应的化学方程式为。(4)、操作1、操作Ⅱ为过滤,滤后果汁滤纸(灰色部分代表滤纸),滤液分布的情况最接近图中的( )。A、
(1)、菱锌矿属于(填“纯净物”或“混合物”)。(2)、由此流程可推知SiO2的性质有( )(填字母序号)。A、难溶于水 B、化学性质很活泼 C、不能与稀硫酸反应(3)、“酸浸”时,金属氧化物发生反应的化学方程式为。(4)、操作1、操作Ⅱ为过滤,滤后果汁滤纸(灰色部分代表滤纸),滤液分布的情况最接近图中的( )。A、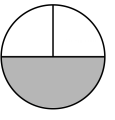 B、
B、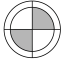 C、
C、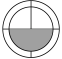 (5)、已知Fe2+和Zn2+开始沉淀和沉淀完全时的pH如下列表格所示,“除杂”过程中加入ZnO的目的是 , 通过调节溶液的pH使Fe+沉淀完全而Zn2+不沉淀,则pH的范围是。
(5)、已知Fe2+和Zn2+开始沉淀和沉淀完全时的pH如下列表格所示,“除杂”过程中加入ZnO的目的是 , 通过调节溶液的pH使Fe+沉淀完全而Zn2+不沉淀,则pH的范围是。