备战2026中考2021-2025中考化学专题汇编精选 专题10 燃烧及灭火 能源的开发利用
试卷更新日期:2026-04-21 类型:二轮复习
一、选择题
-
1. 人类社会的发展离不开能源。下列不属于化石能源的是( )A、石油 B、煤 C、天然气 D、氢能2. 下列图标中,表示“禁止吸烟”的是A、
 B、
B、 C、
C、 D、
D、 3. 分析推理是化学学习中常用的思维方法,下列说法正确的是( )A、试剂瓶中的溶液在使用时不慎洒出一部分,剩余溶液的溶质质量分数减小 B、可燃物在有限空间燃烧能发生爆炸,面粉粉尘在仓库内遇明火也可能发生爆炸 C、氧气、氢气只含一种元素均属于单质,所以含一种元素的物质一定是单质 D、二氧化锰是氯酸钾分解反应的催化剂,任何分解反应都可用二氧化锰做催化剂4. 利用红磷和白磷进行燃烧条件探究,实验装置如下图所示。下列说法不正确的是( )
3. 分析推理是化学学习中常用的思维方法,下列说法正确的是( )A、试剂瓶中的溶液在使用时不慎洒出一部分,剩余溶液的溶质质量分数减小 B、可燃物在有限空间燃烧能发生爆炸,面粉粉尘在仓库内遇明火也可能发生爆炸 C、氧气、氢气只含一种元素均属于单质,所以含一种元素的物质一定是单质 D、二氧化锰是氯酸钾分解反应的催化剂,任何分解反应都可用二氧化锰做催化剂4. 利用红磷和白磷进行燃烧条件探究,实验装置如下图所示。下列说法不正确的是( ) A、a处物质为白磷 B、红磷的着火点高于80℃ C、a、b两点对比说明燃烧需要氧气 D、c处通入氧气白磷能燃烧5. 我国科研人员研制出一种新型催化剂,在这种催化剂作用下,氢气可以转化为汽油,主要转化过程如图所示(部分生成物已略去)。X是一种常见气体氧化物。下列说法正确的是( )
A、a处物质为白磷 B、红磷的着火点高于80℃ C、a、b两点对比说明燃烧需要氧气 D、c处通入氧气白磷能燃烧5. 我国科研人员研制出一种新型催化剂,在这种催化剂作用下,氢气可以转化为汽油,主要转化过程如图所示(部分生成物已略去)。X是一种常见气体氧化物。下列说法正确的是( ) A、X是 B、转化过程中催化剂的质量减少 C、从环保角度考虑,和氢气相比,汽油是更理想的燃料 D、过程Ⅰ中还有水生成,产物CO和质量比是1:16. 和在一定条件下转化为(反应过程如图所示,虚线处部分中间产物略去),可实现的再利用。下列说法错误的是
A、X是 B、转化过程中催化剂的质量减少 C、从环保角度考虑,和氢气相比,汽油是更理想的燃料 D、过程Ⅰ中还有水生成,产物CO和质量比是1:16. 和在一定条件下转化为(反应过程如图所示,虚线处部分中间产物略去),可实现的再利用。下列说法错误的是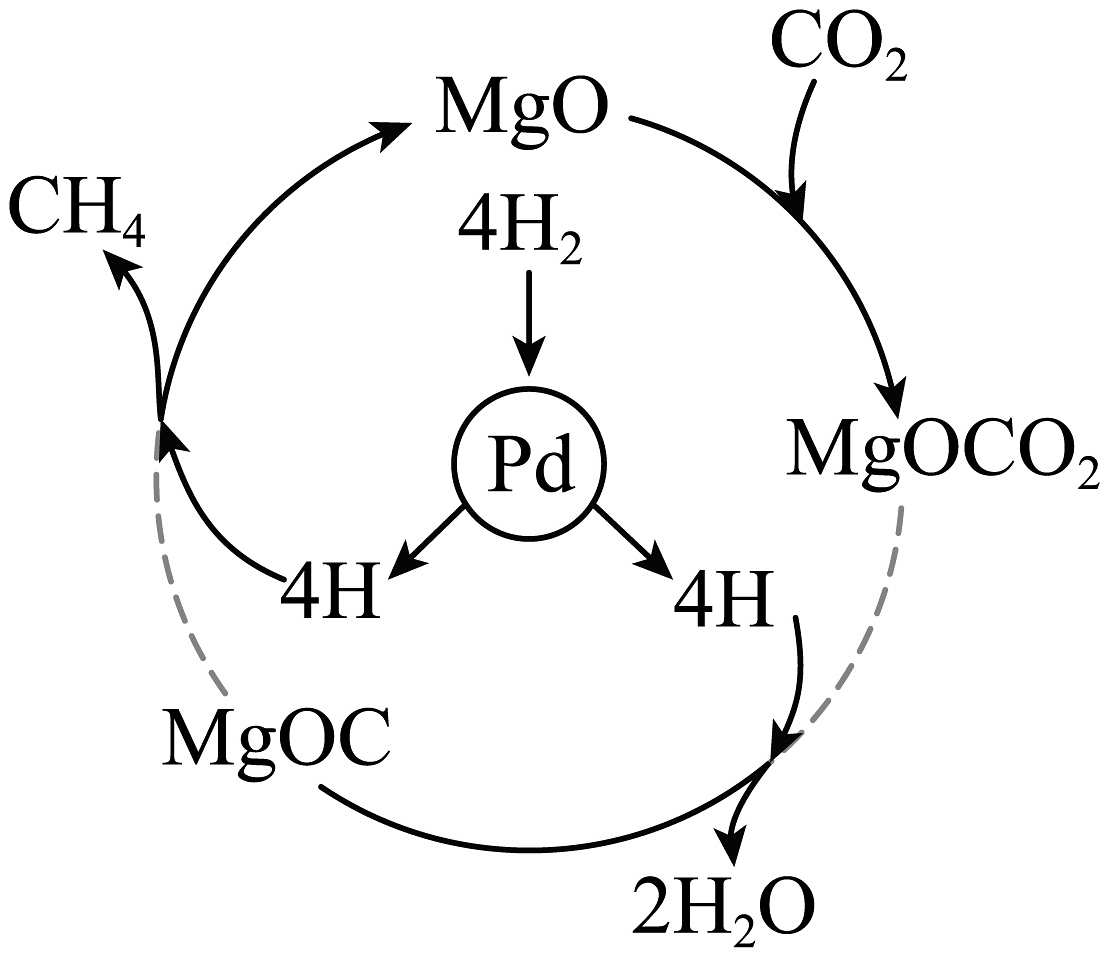 A、是一种清洁能源 B、MgO起催化作用 C、参加反应的和质量比是 D、该反应中,除外另一种生成物为7. 为探究燃烧的条件,利用可调节温度的电炉设计如图所示装置进行实验.已知白磷的着火点是 , 红磷的着火点是 , 氯化钠不是可燃物.下列说法错误的是
A、是一种清洁能源 B、MgO起催化作用 C、参加反应的和质量比是 D、该反应中,除外另一种生成物为7. 为探究燃烧的条件,利用可调节温度的电炉设计如图所示装置进行实验.已知白磷的着火点是 , 红磷的着火点是 , 氯化钠不是可燃物.下列说法错误的是 A、当温度为时,只有①处白磷燃烧 B、为控制变量,①②③④处所取白磷、红磷、氯化钠的质量应相等 C、当温度为时,②处红磷燃烧、③处红磷不燃烧,说明燃烧需要氧气 D、当温度升至时,④处氯化钠可能燃烧8. 用氧气传感器测量蜡烛在密闭容器内燃烧至熄灭过程中,容器内氧气含量的变化如图所示:
A、当温度为时,只有①处白磷燃烧 B、为控制变量,①②③④处所取白磷、红磷、氯化钠的质量应相等 C、当温度为时,②处红磷燃烧、③处红磷不燃烧,说明燃烧需要氧气 D、当温度升至时,④处氯化钠可能燃烧8. 用氧气传感器测量蜡烛在密闭容器内燃烧至熄灭过程中,容器内氧气含量的变化如图所示: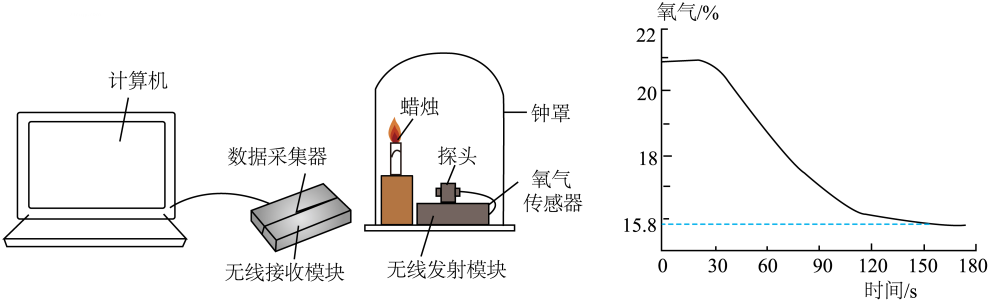
下列分析错误的是( )
A、蜡烛熄灭时钟罩内O2的体积分数为15.8% B、蜡烛在60s时比90s时燃烧更旺 C、用干粉灭火器灭火降低了可燃物周围O2的浓度 D、油锅着火用锅盖盖灭后,锅内氧气完全被消耗二、填空题
-
9. 合成氨是20世纪伟大的成就之一。研究氨气的组成、性质及用途具有重要意义。(1)、液氨可用作制冷剂。构成氨分子的微粒是氮原子和。液态的氨转化为氨气的过程中,氨分子间的距离(填“变大”或“变小”)。(2)、反应8NH3+3Cl2=6NH4Cl+N2可用于检查输送氯气的管道是否泄漏。
①N的质子数为7,核外第一层有2个电子,则第二层有个电子。由Cl转化为Cl﹣的过程中,Cl(填“得到电子”或“失去电子”)。
②中H的化合价为+1价,则N的化合价为价。
(3)、NH3在能源与环境领域应用广泛。①NH3燃烧生成N2和H2O,未来可用作化石燃料的替代能源,从产物的角度分析,作为燃料NH3相比于CH4的优点是。
②NH3可用于烟气脱硝,如4NH3+6R5N2+6H2O,R的化学式为。
10. 新能源的开发和利用促进了能源结构向多元、清洁和低碳转变。(1)、目前,人类利用的能量大多来自化石燃料,如石油、天然气和。在有石油的地方,一般都有天然气存在,天然气的主要成分是甲烷,其化学式为。(2)、做饭时,天然气燃烧不充分,锅底易出现黑色物质,此时可调(填“小”或“大”)燃气灶的进风口,使燃料充分燃烧,节约能源。(3)、我国研制出一种新型催化剂,在这种催化剂作用下,二氧化碳可以转化为汽油,主要转化过程如图所示(部分生成物已略去)。
①催化剂在化学反应前后化学性质和不变。
②过程I中反应生成的另外一种物质为生活中常见的氧化物,该反应的化学方程式为。
(4)、随着科学技术的发展,氢能源的开发利用已取得很大进展。氢气作为燃料的优点是(答一点即可)。11. 燃料的使用推动了人类社会的发展。(1)、燃料变迁过程:木柴(热值12 kJ/g)→煤(热值 34 kJ/g)→天然气(热值 55 kJ/g)①木柴的热值比煤(填“高”或“低”)。
②为使煤充分燃烧,可采取的一种方法是
③用电火花引燃气态燃料,为燃料燃烧提供的条件是
④从达成“碳中和”的目标分析,用天然气(CH4)替代煤(C)作燃料的理由是
(2)、氢气是未来理想的能源。

①2024年6月,我国首次实现利用海上风电电解海水制氢。电解18kg的水,理论上能得到氢气的质量为kg.
②用单壁碳纳米管可储存氢气如图1,该过程中不变的微观粒子是。另一种储氢方式如图2,
 与
与 的质量比是
的质量比是③从不同视角思考,设计一种理想燃料,需要考虑的因素有(答两点)。
三、综合题
-
12. 我国科学家利用太阳光在某种新型催化剂表面高效分解水后,再利用某种高效催化剂将二氧化碳转化成有机物X。反应过程如图所示,回答下列问题:
 (1)、反应①、②使用的催化剂在反应前后的和化学性质都没有发生变化。(2)、反应①的能量转化形式中存在光能转化为能 ,产生的H2、O2的体积比约为。(3)、反应②的化学方程式: , 则X的化学式为;可用(填试剂名称)检验反应后的气体中是否还含有CO2。(4)、反应②生成的水全部循环利用,为使该过程持续发生,反应①需要不断补充水,其原因是。13. 造纸术是中国古代四大发明之一,氯氧化钾是造纸的重要原料。我国古代制造氢氧化钾的主要流程如图所示,其原理是将干燥的木料烧成灰(含),再向灰汁中加入石灰浆,充分反应后,进一步提纯得到氢氧化钾。
(1)、反应①、②使用的催化剂在反应前后的和化学性质都没有发生变化。(2)、反应①的能量转化形式中存在光能转化为能 ,产生的H2、O2的体积比约为。(3)、反应②的化学方程式: , 则X的化学式为;可用(填试剂名称)检验反应后的气体中是否还含有CO2。(4)、反应②生成的水全部循环利用,为使该过程持续发生,反应①需要不断补充水,其原因是。13. 造纸术是中国古代四大发明之一,氯氧化钾是造纸的重要原料。我国古代制造氢氧化钾的主要流程如图所示,其原理是将干燥的木料烧成灰(含),再向灰汁中加入石灰浆,充分反应后,进一步提纯得到氢氧化钾。 (1)、操作①的名称是。(2)、“制浆池”中发生反应的基本类型是 , 从能量变化的角度分析该反应为(填“放热”或“吸热”)反应。(3)、“反应池”中发生反应的化学方程式是。14. 碳及其化合物的综合利用使世界变得更加绚丽多彩。(1)、Ⅰ.碳的多样性
(1)、操作①的名称是。(2)、“制浆池”中发生反应的基本类型是 , 从能量变化的角度分析该反应为(填“放热”或“吸热”)反应。(3)、“反应池”中发生反应的化学方程式是。14. 碳及其化合物的综合利用使世界变得更加绚丽多彩。(1)、Ⅰ.碳的多样性金刚石和C60的化学性质相似,但物理性质却存在着很大差异。原因是。
(2)、从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于(填“单质”或“化合物”)。(3)、Ⅱ.“碳中和”的实现“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。
CO2的过度排放会造成的加剧。结合生活实际,列举可为实现“碳中和”做出直接贡献的一种措施:。
(4)、工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。①NaOH吸收。NaOH溶液吸收CO2生成 NaHCO3的化学方程式为。
②CaO吸收。CaC2O4在高温下分解制得疏松多孔的CaO,同时产生CO、CO2。该反应所得CO、CO2的分子个数之比为。
(5)、CO2与H2在一定条件下转化为CH4(反应过程如图所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中,除CH4外另一种生成物为(填化学式),MgO的作用是。
②天然气(主要成分为CH4)已成为居民的生活用气,是因为CH4在空气中燃烧时(填“吸收”或“放出”)热量。
四、实验探究题
-
15. 实验探究是学习化学的重要方法。请根据下列实验装置图回答问题。
 (1)、装置A中仪器a的名称是。(2)、实验室用过氧化氢溶液制取 , 用大理石和稀盐酸制取。二者都可以选用的发生装置是(填装置序号,下同),用排空气法收集两种气体都可以选用的收集装置是。(3)、实验室用过氧化氢溶液和制取 , 反应的化学方程式是 , 用装置C收集生成的纯度偏低,原因可能是(填序号)。
(1)、装置A中仪器a的名称是。(2)、实验室用过氧化氢溶液制取 , 用大理石和稀盐酸制取。二者都可以选用的发生装置是(填装置序号,下同),用排空气法收集两种气体都可以选用的收集装置是。(3)、实验室用过氧化氢溶液和制取 , 反应的化学方程式是 , 用装置C收集生成的纯度偏低,原因可能是(填序号)。①制取装置气密性不好
②收集前,集气瓶中未注满水
③收集完成时,集气瓶中仍有少量水
(4)、向盛有80℃热水的装置F的试管中放入白磷,然后将通入试管中与白磷接触,白磷燃烧(白磷着火点为40℃)。水能灭火,但试管中的白磷却在水中燃烧,请从可燃物燃烧的条件分析,原因是。16. 化学是能源科学、环境科学、航空航天工程等现代科学技术的基础。(1)、社会发展离不开优质能源开发。下列属于可再生能源的是(填字母)。a. 煤
b.石油
c. 氢气
d. 天然气
(2)、能源转型是人类进步的驱动力,家用燃料的变迁承载了社会文明发展的需求。某兴趣小组通过调查家用燃料的变迁与合理使用,绘制了下图所示的家用燃料变迁图。请完成下列问题。

①点燃煤时常用柴草引燃,说明可燃物燃烧需要的条件之一是
②天然气主要成分是甲烷。甲烷完全燃烧的化学方程式为
③天然气作为一种比较清洁的燃料,已经走进城乡居民生活。与燃煤相比,使用天然气可以减少的空气污染物是(填一种即可)。
(3)、CO2捕集是实现低碳目标的一种有效手段,某捕集CO2工艺流程如下图所示。
①捕捉室中采用“喷淋”方式加入NaOH溶液,请叙述“喷淋”方式的优点。
②写出反应分离室中生成NaOH的化学方程式。
③以上工艺流程中不涉及的化学反应基本类型是
(4)、新能源在我国航天科技领域有着广泛的应用,火箭发射卫星时常用液氢和液氧作推进剂。要将卫星送达预定轨道,某型火箭至少需要燃烧220kg的液氢才能提供足够的能量。理论上该火箭需要携带液氧的质量是多少?17.氢能作为极具发展潜力的多元化能源,在我国经济发展中具有重要的地位。某校实践小组的同学们对此产生了浓厚的兴趣,他们对氢气的制取方法、应用优势、储存手段和发展前景等展开了项目式问题探究。
任务一:调查氢能制取方法
【咨询专家】小组同学通过数字化平台向专家进行咨询,知道了氢气可用多种工艺过程制备,方法有电解水制氢和工业副产品制氢等。
【模型构建】用可再生能源电解水制氢,将是应用广泛、技术成熟的一种手段。过程如图:

【交流讨论】
(1)近年来,能用来发电的可再生能源有。
(2)化石燃料也可用于氢的制取,但不足之处有。
任务二:探究氢能应用优势
【提出问题】氢气作为理想能源的原因是什么?
【进行实验】
(3)设计纯净氢气与天然气燃烧的对比实验
实验步骤
实验现象
实验结论
①分别在带尖嘴的导管口点燃氢气和天然气,在火焰上方罩一个干冷的小烧杯
均有水生成
②迅速把①中的烧杯倒过来,分别注入少量澄清石灰水,振荡
罩在天然气火焰上方烧杯内的澄清石灰水变浑浊,而氢气火焰上方的烧杯内无变化
【反思评价】
(4)通过上述实验对比,氢气作为燃料的优点是。
(5)在理想状态下,小组同学通过图1实验,将测得的实验数据绘制成的图像如图2所示,分析图像,可得出的结论是。

任务三:调研氢能储存手段
【查阅资料】
(6)我国绿氢规模化储存是商业化应用的基本保障,为了进行大量储存,通常将氢气转化为液氢,从微观角度分析,发生改变的是。
任务四:展望氢能发展前景
【市场调研】
(7)目前,氢燃料电池在公共交通中应用已较为成熟,其工作原理如图3所示,发生反应的化学方程式为 , 未来,氢能将在航空、航天、电力和建筑领域大力推广。

成果分享:通过问题探究,大家对氢能有了较为全面的认识。氢气作为一种理想的新型能源,其产业链包括“制—储—输—用”四个主要环节。因此,降本增效、规模化发展,将是我国经济增长和服务民生的一项重要举措。
五、计算题
-
18. 氢气是清洁能源。硼氢化钠(NaBH)作为一种环境友好的固体储氢材料,可与水反应生成氢气,化学方程式为NaBH4+2H2O=NaBO2+4H2↑。(1)、氢气被称为清洁能源的原因是(2)、某工厂生产燃料电池需要12t氢气,理论上需要NaBH4的质量是多少(写出计算过程)?