相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、某有机化合物由原子序数依次增大的短周期主族元素W、X、Y、Z组成,Y、Z同主族且Z的原子序数是Y的2倍,该化合物的质谱图如下,为139时,其碎片离子组成为。
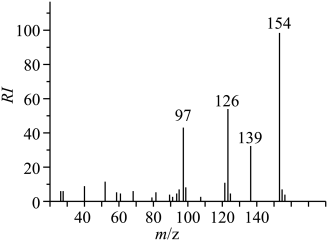
下列叙述正确的是( )
A、原子半径: B、简单氢化物沸点: C、化合物、、均为直线形分子 D、溶液与溶液混合,无明显现象 -
2、的无限长链状结构截取部分如图所示,下列说法不正确的是( )
 A、中含有共价键 B、为原子晶体 C、的熔沸点比低 D、水解产生
A、中含有共价键 B、为原子晶体 C、的熔沸点比低 D、水解产生 -
3、向溶液中滴加黄血盐可制得普鲁士蓝,向溶液中滴加赤血盐可制得滕氏蓝。经科学家研究发现,两者具有相同的结构。其晶胞由8个如图所示的小立方体构成(未标出),晶胞参数为。下列关于普鲁士蓝和滕氏蓝说法错误的是( )
 A、滕氏蓝和普鲁士蓝均为离子晶体 B、由图及滕氏蓝的化学式可知,应位于晶胞体心 C、测定晶体的结构常采用X射线衍射法 D、设滕氏蓝的式量为 , 则滕氏蓝晶体的密度为
A、滕氏蓝和普鲁士蓝均为离子晶体 B、由图及滕氏蓝的化学式可知,应位于晶胞体心 C、测定晶体的结构常采用X射线衍射法 D、设滕氏蓝的式量为 , 则滕氏蓝晶体的密度为 -
4、高氯酸钾是一种强氧化剂,易溶于水。以氯化钠为原料制备高氯酸钾的一种流程如图:

下列说法错误的是( )
A、“电解”步骤中,电解槽内宜使用阳离子交换膜 B、“高温分解”反应中氧化剂和还原剂的物质的量之比为1:3 C、本实验条件下,在水中的溶解度比小 D、母液中的溶质经分离、提纯可制得食盐 -
5、阿司匹林具有解热镇痛作用,科研工作者在一定条件下合成长效缓释阿司匹林,从而减少了对肠胃的刺激和每天吃药次数。下列说法正确的是( )
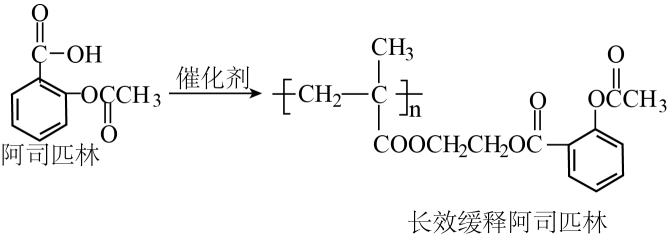 A、阿司匹林与足量的反应,最多消耗 B、阿司匹林与长效缓释阿司匹林可通过红外光谱区别 C、阿司匹林和长效缓释阿司匹林中碳原子的杂化方式不同 D、长效缓释阿司匹林与溶液反应,最多消耗
A、阿司匹林与足量的反应,最多消耗 B、阿司匹林与长效缓释阿司匹林可通过红外光谱区别 C、阿司匹林和长效缓释阿司匹林中碳原子的杂化方式不同 D、长效缓释阿司匹林与溶液反应,最多消耗 -
6、由实验操作和现象,可得出相应正确结论的是( )
实验操作
现象
结论
A
向苯酚的样品加入浓溴水,振荡
未出现白色沉淀
样品中不含苯酚
B
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的悬浊液
无砖红色沉淀
蔗糖未发生水解
C
在火焰上灼烧搅拌过某无色溶液的玻璃棒
火焰出现黄色
不能确定溶液中含有Na元素
D
向装有电石的圆底烧瓶中缓慢滴加饱和食盐水
产生的气体使酸性高锰酸钾溶液褪色
与反应生成
A、A B、B C、C D、D -
7、化学物质与人类生产活动、生命健康密切相关。下列说法错误的是( )A、卤水点豆腐的过程涉及蛋白质的变性 B、食盐、白糖是常见的食品调味剂,也可用作防腐剂 C、核苷酸聚合生成多聚核苷酸的过程中发生了酯化反应 D、氨基酸分子通过肽键相互连接,形成蛋白质的一级结构
-
8、宏观辨识与微观探析是化学学科核心素养之一。下列对应离子方程式书写错误的是( )A、硫代硫酸钠溶液中滴入稀硫酸: B、向氨水中滴入少量硫酸铜溶液: C、向烧碱溶液中加入一小段铝片: D、等浓度和溶液等体积混合:
-
9、2021年9月24日,中科院天津工业生物技术研究所成果“无细胞化学酶系统催化合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设为阿伏加德罗常数的值。
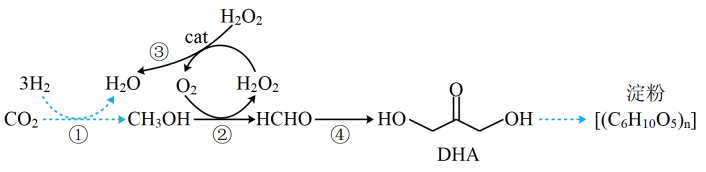
下列说法错误的是( )
A、分子中杂化的原子数为 B、反应②中生成标准状况下 , 转移电子数为 C、与DHA的混合物中含氧原子数为 D、淀粉完全水解消耗 -
10、湖北省博物馆的镇馆之宝——曾侯乙编钟由青铜所铸。下列说法错误的是( )A、青铜属于合金,硬度比纯铜大 B、青铜器露置于空气中会发生电化学腐蚀而“生锈” C、“青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定 D、现代工艺采用电解精炼提纯铜,用纯铜作阳极、粗铜作阴极
-
11、化学与生产、生活和科技密切相关。下列说法正确的是( )A、用来生产电闸、灯口等产品的酚醛树脂属于聚酯类化合物 B、“问天”实验舱采用砷化镓太阳能电池,砷化镓具有良好的导电性 C、太阳电池翼采用的碳纤维框架和玻璃纤维框架均为无机非金属材料 D、天然橡胶硫化后转变为网状结构,硫化程度越高,强度和弹性越大
-
12、美乐托宁(G)具有抗氧化、抗炎、抑制肿瘤生长等作用。它的一种合成路线如下:
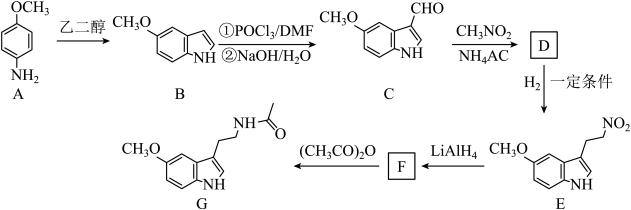
已知:
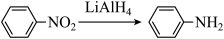
回答下列问题:
(1)、A中不含氧元素的官能团的名称是。的反应类型是。(2)、D的结构简式为。(3)、的反应方程式为。(4)、化合物的相对分子质量比大14,符合下列条件的的同分异构体有种(不考虑立体异构)。①芳香族化合物
②稀溶液遇到溶液显紫色
③苯环上只有两个取代基
其中核磁共振氢谱有4组峰,峰面积之比为的结构简式为。
(5)、4-甲氧基乙酰苯胺(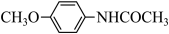 )是重要的精细化工中间体,根据上述路线中的相关知识,写出由苯甲醚(
)是重要的精细化工中间体,根据上述路线中的相关知识,写出由苯甲醚(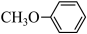 )制备4-甲氧基乙酰苯胺的合成路线(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线(其他试剂任选)。 -
13、邻硝基苯甲醛(
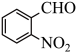 )是一种精细化工产品。实验室以邻硝基苯甲醇(
)是一种精细化工产品。实验室以邻硝基苯甲醇( )为原料,利用物质在水相和有机相两相中溶解性不同制备得到,实验装置(夹持仪器已略去)和反应原理分别如图1和图2所示。
)为原料,利用物质在水相和有机相两相中溶解性不同制备得到,实验装置(夹持仪器已略去)和反应原理分别如图1和图2所示。已知:1.部分物质的性质
物质
溶解性
熔点/℃
沸点/℃
水
邻硝基苯甲醛
微溶
易溶
70
270
邻硝基苯甲醇
难溶
易溶
43
153
TEMPO—COOH
易溶
难溶
—
—
2.
 +NaHSO3
+NaHSO3 (易溶于水)
(易溶于水)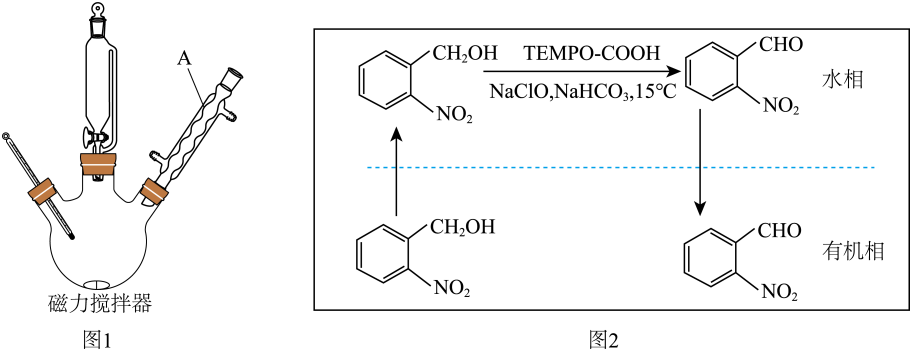 (1)、Ⅰ.制备:向三颈瓶中依次加入15.3g邻硝基苯甲醇、10.0mL二氯甲烷和磁子,搅拌,待固体全部溶解后,再依次加入的水溶液和饱和溶液。保持温度 , 逐滴加入足量水溶液,持续反应。经一系列操作得到粗产品。
(1)、Ⅰ.制备:向三颈瓶中依次加入15.3g邻硝基苯甲醇、10.0mL二氯甲烷和磁子,搅拌,待固体全部溶解后,再依次加入的水溶液和饱和溶液。保持温度 , 逐滴加入足量水溶液,持续反应。经一系列操作得到粗产品。
仪器的名称为 , 作用是。(2)、控制反应温度为的方法是。(3)、滴加水溶液生成产品的化学方程式为。该步反应要逐滴加入的目的是。(4)、Ⅱ.提纯:在粗产品中加入饱和溶液,充分反应后分液,在水层中加入氢氧化钠溶液,待固体完全析出后,进行抽滤、洗涤、干燥至恒重,得13.0g产品。
氢氧化钠溶液的作用是。(5)、本次实验的产率为(计算结果保留3位有效数字)。(6)、该制备采用两相反应体系可以大幅提高邻硝基苯甲醛的产率,原因是。 -
14、氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi),在性质上表现出从典型非金属元素到典型金属元素的完整过渡。回管下列问题:(1)、羟胺(NH2OH)的水溶液呈碱性,其碱性原理与氨水相似,同浓度两种溶液的碱性较强的是(填“NH2OH”或“NH3”),原因是。(2)、氢键的形成对物质的密度、熔沸点、粘稠性等产生影响。市售82%磷酸是粘稠状的液体,黏度较大的原因是。(3)、南开大学某课题组成功合成无机二茂铁的类似物[FeP8]2- , 结构如图所示,环状结构与苯相似,中的大键表示为。(分子中的大π键可用表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)
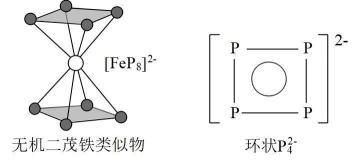 (4)、超盐晶体PH4AlBr4由超碱和超卤素组成。比较与PH3键角大小:PH3(填“”、“<”或“=”),原因是。(5)、钼酸铋(Bi2MoO6)可用于光催化水的分解,其立方晶胞结构(未画出氧原子)如图所示,晶胞参数为a pm、a pm、c pm。
(4)、超盐晶体PH4AlBr4由超碱和超卤素组成。比较与PH3键角大小:PH3(填“”、“<”或“=”),原因是。(5)、钼酸铋(Bi2MoO6)可用于光催化水的分解,其立方晶胞结构(未画出氧原子)如图所示,晶胞参数为a pm、a pm、c pm。
①若原子1的分数坐标为( , , 0),原子2的分数坐标为。
②设NA为阿伏加德罗常数的值,Bi2MoO6的摩尔质量为M。Bi2MoO6晶体的密度为g/cm3 (列计算式)。
-
15、硒是人体不可缺少的微量元素,铈是稀土元素中丰度最大的元素,它们的化合物在生产、生活中有着广泛的应用。回答下列问题:
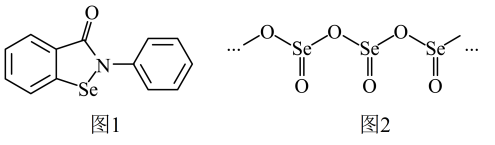 (1)、基态Se原子的核外价电子轨道表示式为。(2)、“依布硒”是一种有机硒化物,具有良好的抗炎活性,其结构简式如图1所示。“依布硒”中原子的杂化类型为 , 元素Se、O、N的第一电离能由大到小的顺序为。(3)、硒的某种链状聚合氧化物结构如图2所示,其化学式为。(4)、与具有相似的结构,室温时,是一种气体。沸点高低:(填“>”或“<”或“=”),原因是。(5)、二硫键和二硒键是重要的光响应动态共价键,其光响应原理如图3所示。已知光的波长与其能量成反比,则图中实现光响应的波长:(填“>”或“<”或“=”)。
(1)、基态Se原子的核外价电子轨道表示式为。(2)、“依布硒”是一种有机硒化物,具有良好的抗炎活性,其结构简式如图1所示。“依布硒”中原子的杂化类型为 , 元素Se、O、N的第一电离能由大到小的顺序为。(3)、硒的某种链状聚合氧化物结构如图2所示,其化学式为。(4)、与具有相似的结构,室温时,是一种气体。沸点高低:(填“>”或“<”或“=”),原因是。(5)、二硫键和二硒键是重要的光响应动态共价键,其光响应原理如图3所示。已知光的波长与其能量成反比,则图中实现光响应的波长:(填“>”或“<”或“=”)。 (6)、二氧化铈()氧载体具有良好的储氧放氧能力,可用于甲烷化学链重整,其原理如下图所示。
(6)、二氧化铈()氧载体具有良好的储氧放氧能力,可用于甲烷化学链重整,其原理如下图所示。
中 , 和个数比为。
-
16、某实验小组探究酸对平衡的影响。将溶液(接近无色)和溶液等体积混合,得到红色溶液,取两等份红色溶液,进行如下操作并记录现象。下列结论错误的是( )
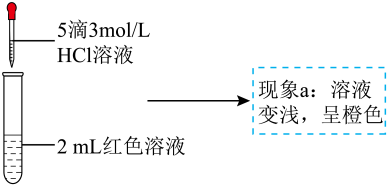
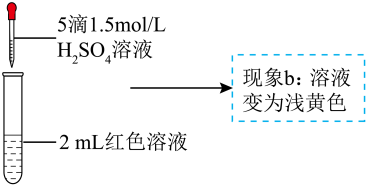
实验a 实验 b
查阅资料:(黄色);(无色)
A、、、都属于难电离的微粒 B、中的配位键由原子提供孤电子对 C、现象中使溶液呈橙色的微粒可能是和 D、改变或 , 平衡会发生移动 -
17、下列实验方案能达到实验目的的是( )
选项
实验方案
实验目的
A
在2mL2%氨水中滴加溶液
配制银氨溶液
B
在淀粉溶液中加入适量20%硫酸,加热,冷却后加NaOH溶液至中性,再滴加碘水,溶液变蓝
证明淀粉未完全水解
C
加热溴乙烷与NaOH溶液的混合物一段时间,取少量冷却后的上层溶液,加入足量稀硝酸后滴入溶液,产生沉淀
证明溴乙烷发生的是取代反应
D
在丙烯醛()中加入碱性的新制悬浊液,加热后产生砖红色沉淀;取上层清液,加入溴水,溴水褪色
证明丙烯醛中含有醛基和碳碳双键
A、A B、B C、C D、D -
18、将6.8gX完全燃烧生成和8.96L(标准状况)。X的质谱图、核磁共振氢谱图与红外光谱图如图所示。下列关于的叙述错误的是( )

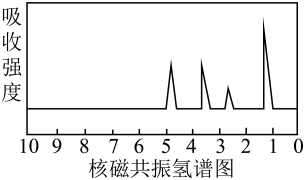
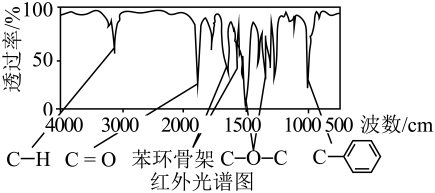 A、的化学式为 B、分子中有四种化学环境不同的氢原子 C、的官能团一定为醚键和羰基 D、可能是
A、的化学式为 B、分子中有四种化学环境不同的氢原子 C、的官能团一定为醚键和羰基 D、可能是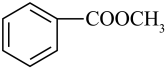
-
19、高分子可用于制备聚合物离子导体,合成路线如下:
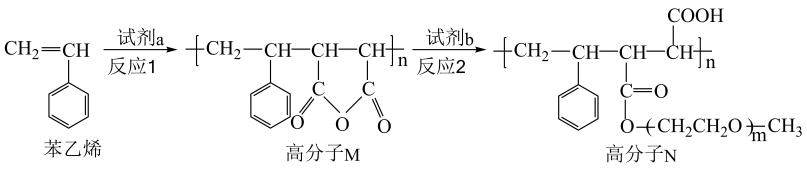
下列说法错误的是( )
A、苯乙烯分子中所有原子可能共平面 B、反应1为加聚反应,反应2为取代反应 C、试剂为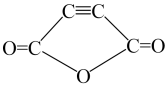 D、试剂为
D、试剂为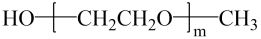
-
20、calebinA可用于治疗阿尔茨海默症,其结构如图。下列关于calebinA的说法正确的是( )
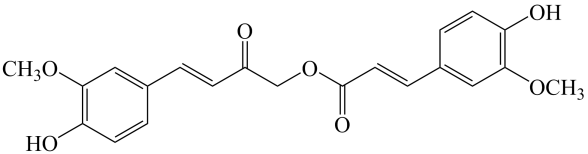 A、该物质与溶液反应,最多消耗 B、该物质与加成,最多消耗 C、该物质与溴水反应,最多消耗 D、该物质苯环上的一氯代物有3种
A、该物质与溶液反应,最多消耗 B、该物质与加成,最多消耗 C、该物质与溴水反应,最多消耗 D、该物质苯环上的一氯代物有3种