相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、分子式为C6H12O且能发生银镜反应的有机化合物有(不考虑立体异构)( )A、5种 B、6种 C、7种 D、8种
-
2、仅用一种试剂即可将酒精、苯酚溶液、己烯、甲苯4种无色液体区分开来,这种试剂是( )A、FeCl3溶液 B、KMnO4溶液 C、溴水 D、金属钠
-
3、下列实验操作及现象、结论表述不合理的是( )
选项
实验操作及现象
结论
A
向和无水乙醇的混合溶液中加入1-溴丁烷和几片碎瓷片并微热,将产生的气体通入酸性溶液,溶液褪色
1-溴丁烷发生消去反应生成了烯烃
B
向鸡蛋清溶液中滴入浓硝酸,产生白色沉淀,加热后沉淀变黄色
鸡蛋清蛋白质中含有苯环
C
向酸性溶液中通入乙烯至过量,溶液紫红色褪去
酸性溶液能氧化乙烯
D
向溴水中加入苯,振荡后静置,水层颜色变浅
苯能将溴从水中萃取出来
A、A B、B C、C D、D -
4、W、X、Y、Z为原子序数依次增大的短周期元素,四种元素组成的无机盐溶于盐酸有无色无味的气体生成,离子与具有相同的核外电子数,下列叙述正确的是( )A、分子的空间结构为三角锥形 B、原子半径: C、X单质只有4种同素异形体 D、W、Y、Z三种元素形成的化合物都是酸
-
5、乙酰水杨酸(又称阿司匹林)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,其结构如图所示。下列说法错误的是( )
 A、该物质含有两种官能团 B、能发生氧化、取代、加成、消去反应 C、分子中最少有7个碳原子共平面 D、该有机化合物最多与氢氧化钠发生反应
A、该物质含有两种官能团 B、能发生氧化、取代、加成、消去反应 C、分子中最少有7个碳原子共平面 D、该有机化合物最多与氢氧化钠发生反应 -
6、下列说法正确的是( )A、三氯乙酸的酸性小于二氯乙酸的,是因为的极性小于的极性 B、易溶于溶液,可用“相似相溶”规律解释 C、冰浮在水面,是由于水分子之间形成氢键使冰晶体中水分子间的空隙增大 D、键长 , 因此稳定性
-
7、下列有机物命名正确的是( )

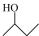
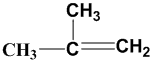
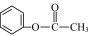
A.2-乙基丙烷
B.3-丁醇
C.2-甲基丙烯
D.苯甲酸甲酯
A、A B、B C、C D、D -
8、下列反应的离子方程式不正确的是( )A、向苯酚钠溶液中通入少量:2
 + CO2+H2O2
+ CO2+H2O2 +CO32-
B、乙醛与新制氢氧化铜悬浊液混合后加热:
C、向盛有硫酸铜溶液的试管里加入过量氨水,得到深蓝色溶液:
D、乙酸乙酯与溶液混合后加热:
+CO32-
B、乙醛与新制氢氧化铜悬浊液混合后加热:
C、向盛有硫酸铜溶液的试管里加入过量氨水,得到深蓝色溶液:
D、乙酸乙酯与溶液混合后加热:
-
9、下列叙述正确的是( )A、氧原子电子的电子云轮廓图:
 B、表示3p能级有4个轨道
C、基态N原子电子排布的轨道表示式:
B、表示3p能级有4个轨道
C、基态N原子电子排布的轨道表示式: D、金属产生焰色的原因是金属原子发生电子跃迁
D、金属产生焰色的原因是金属原子发生电子跃迁
-
10、设为阿伏加德罗常数的值,下列叙述正确的是( )A、分子中含有键数目为 B、标准状况下,己烷所含C原子数目为 C、苯乙烯(
 )中含有碳碳双键数为
D、的配位键数目为
)中含有碳碳双键数为
D、的配位键数目为
-
11、下列操作能达到实验目的的是( )
A
B
C
D


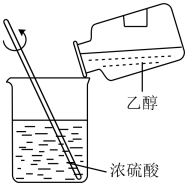

用酒精萃取碘水中的碘
蒸馏实验中将蒸气冷凝为液体
混合浓硫酸和乙醇
证明乙炔可使酸性高锰酸钾溶液褪色
A、A B、B C、C D、D -
12、下列有关化学用语的表述不正确的是( )A、乙烷的空间填充模型:
 B、的结构式:
C、乙醇的分子式:
D、分子间的氢键:
B、的结构式:
C、乙醇的分子式:
D、分子间的氢键:
-
13、化学与生活密切相关,下列说法不合理的是( )A、蔗糖分子结构被修饰后得到的三氯蔗糖可供糖尿病患者使用 B、硫酸铵、硫酸铜、氢氧化钠和乙醇均能使蛋白质变性 C、甲醛的水溶液可用于消毒和制作生物标本 D、石墨晶体中存在范德华力,常用作润滑剂
-
14、实验小组同学探究用新制氢氧化铜检验葡萄糖的适宜条件。
资料:ⅰ.葡萄糖在碱的作用下,可以生成黄色物质;随着温度升高,可聚合为颜色更深(如棕色)的聚合物。
ⅱ.Cu2O、CuO均溶于氨水,生成、;Cu不溶于氨水。
(1)、探究NaOH溶液的用量对该反应的影响。编号
实验Ⅰ
实验Ⅱ
实验方案


实验现象
加热,无明显现象,
静置后未见砖红色沉淀
加热、静置后,
底部有砖红色沉淀
①实验Ⅱ中,葡萄糖转化为。
②分析实验Ⅱ能生成砖红色沉淀但实验Ⅰ不能生成砖红色沉淀的原因:
a.电极反应式:
ⅰ.还原反应:
ⅱ.氧化反应:。
b.依据电极反应式分析实验Ⅱ有砖红色沉淀生成的可能原因:随增大,氧化性减弱,但是。
(2)、探究葡萄糖溶液的用量和水浴温度(加热时间约1min,冷却后过滤)对该反应的影响。实验方案
现象
温度


50℃
得到较多砖红色沉淀;滤液呈极浅黄色
得到大量砖红色沉淀;滤液呈浅橙色
70℃
得到较多砖红色沉淀;滤液呈棕黄色
得到大量砖红色沉淀并伴有少量黑色沉淀;滤液呈棕色
100℃
得到较多砖红色沉淀;滤液呈红棕色
得到大量黑色沉淀;滤液呈深棕色
①经检验,实验Ⅳ中产生的黑色沉淀中含有Cu。检验方法是:取实验Ⅳ中70℃时产生的沉淀,洗涤,(填操作和现象)。
②分析实验Ⅲ未产生黑色Cu的原因,同学提出两种假设:
假设a:葡萄糖物质的量少,无法将Cu(Ⅱ)还原为Cu单质。
假设b:(补充完整)。
经定量分析可知假设a不成立。
(3)、综合以上实验,用新制氢氧化铜检验葡萄糖时,为了能更好地观察到试管内产生砖红色沉淀,将宜采用的条件填入下表。温度/℃
NaOH溶液
葡萄糖溶液
条件
2mL10%NaOH溶液
-
15、某治疗胃溃疡的药物中间体N,可通过如下合成路线制得。
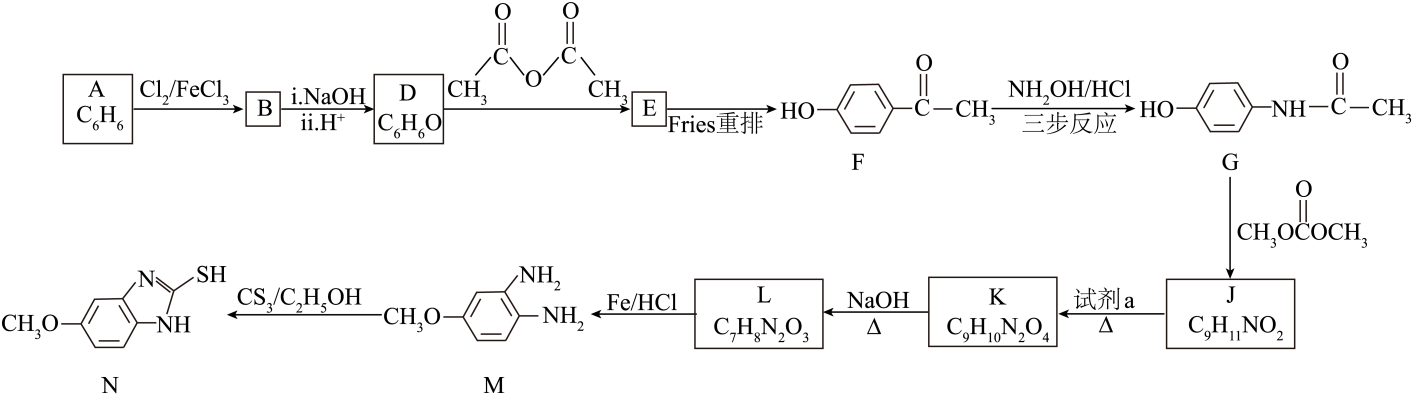
资料:“重排”指有机物分子中的一个基团迁移到另外一个原子上,其分子式不变。
(1)、A→B的反应类型是。(2)、按官能团分类,D的类别是。(3)、E含有酯基。E的结构简式是。(4)、写出符合下列条件的F的同分异构体:(写出2种)。ⅰ.在一定条件下可以发生银镜反应
ⅱ.核磁共振氢谱有4组峰,峰面积比为1:2:2:3
(5)、F与反应生成G的过程如下。
已知:ⅰ.发生加成反应时,断开键。
ⅱ.同一个碳上连着一个羟基和一个氨基(或取代的氨基)时不稳定,易脱水生成亚胺(
 )。
)。写出P、Q的结构简式:、。
(6)、J含有醚键。试剂a是。(7)、K与NaOH反应得到L的化学方程式是。 -
16、不同空腔尺寸的瓜环可以通过形成超分子从气体或溶液中识别不同分子并选择性吸附。瓜环[7]的一种合成路线如下。
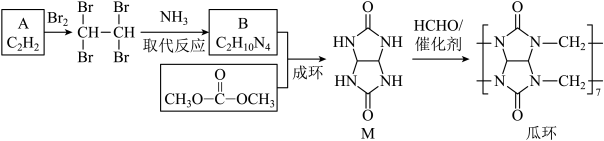 (1)、A的名称是。(2)、1,1,2,2-四溴乙烷与反应生成B的化学方程式是。此反应过程需要加入远远过量的 , 目的有:
(1)、A的名称是。(2)、1,1,2,2-四溴乙烷与反应生成B的化学方程式是。此反应过程需要加入远远过量的 , 目的有:①减少副反应,提高生成物纯度。
②。
(3)、推测“成环”反应中生成M和。(4)、瓜环[7]的分子结构模型如下图所示。
①下列关于瓜环[7]的说法正确的是(填序号)。
a.含有的官能团是酰胺基
b.含有2种不同化学环境的氢原子
c.分子间存在范德华力和氢键
d.空腔尺寸以及具有负电性的氧原子端口使其具有对特定分子的识别能力
②M与HCHO生成瓜环[7]的化学方程式是。
(5)、提出一种测定瓜环[n]中n值的方案:。 -
17、有机物中的(键较难断裂,活化键是有机反应研究的热点之一、由
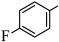 经两步反应合成
经两步反应合成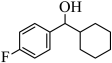 , 均需使键活化,步骤如下
, 均需使键活化,步骤如下 (1)、铬、铁位于元素周期表中的(填序号)。
(1)、铬、铁位于元素周期表中的(填序号)。a.s区 b.d区 c.p区 d.ds区
(2)、 转化为
转化为 的过程中,键中的(填“”或“”)键断裂,发生加成反应,转化为键。 (3)、利用有机金属框架(MOF)构筑双铁催化剂,制备过程的核心结构变化如下。
的过程中,键中的(填“”或“”)键断裂,发生加成反应,转化为键。 (3)、利用有机金属框架(MOF)构筑双铁催化剂,制备过程的核心结构变化如下。注:代表+2价铁,代表+3价铁。

①
 与的相对分子质量相差较大,但二者的沸点却极为接近(相差1℃左右),原因有:
与的相对分子质量相差较大,但二者的沸点却极为接近(相差1℃左右),原因有:ⅰ.的极性强于
 ;
;ⅱ.。
②易被氧化为 , 结合价层电子排布解释原因:。
(4)、铜铬催化剂的主要成分是CuCl、和(甲基硼酸)等,能有效抑制副产物的生成。①中B的杂化轨道类型是。
②已知:和均为一元弱酸。推测 (填“>”或“<”)
-
18、氨硼烷()是一种具有研究价值的固体储氢材料。
已知:含氢19.5%,白色晶体,熔点为104℃。可溶于水和甲醇等溶剂中。常温常压下能够稳定存在。在催化剂存在的情况下,能够快速与水反应。
元素
H
B
N
电负性
2.1
2.0
3.0
(1)、基态N原子的核外电子排布的轨道表示式为。(2)、B的第一电离能低于Be,可能的原因是。(3)、分子结构示意图如图1,其中为键(填序号,下同),为键。
a.配位键 b.非极性键 c.键 d.键
(4)、在某种催化剂表面与反应的释氢机理如图2。
①若用和做反应物,生成的氢气是(填序号)。
a. b. c.HD
②写出理论上与完全反应的总反应的离子方程式:。
(5)、研究发现,在低温高压条件下为正交晶系结构。的2×2×2超晶胞结构如图3所示(超晶胞内含有16个氨硼烷分子,)。氨硼烷晶体的密度为(已知:;表示阿伏加德罗常数)。
-
19、化学小组研究的性质,完成如下实验:
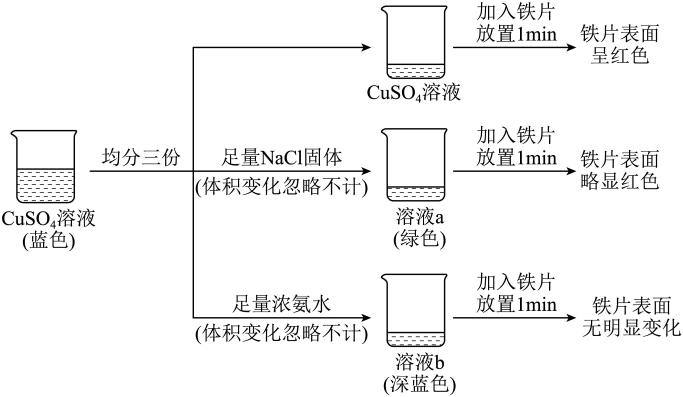
已知:;;
下列说法不正确的是( )
A、溶液中加入NaCl固体: B、溶液a中加入浓氨水时不可能出现蓝色沉淀 C、溶液a、b中铁片的颜色不同证明 D、溶液b中加入足量乙醇时可以析出深蓝色晶体 -
20、中国自行研制、具有自主知识产权的C919大型客机机舱内部首次使用芳砜纶纤维制作椅罩、门帘。芳砜纶纤维是有机耐高温纤维,由三种单体
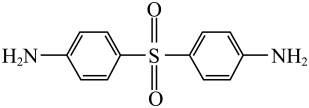 、
、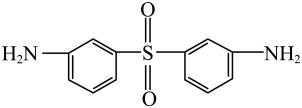 、
、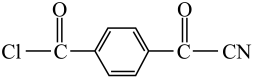 缩合共聚制成。芳砜纶纤维结构简式如图所示:
缩合共聚制成。芳砜纶纤维结构简式如图所示: 。下列说法不正确的是( ) A、芳砜纶纤维中不含手性碳原子 B、
。下列说法不正确的是( ) A、芳砜纶纤维中不含手性碳原子 B、 的名称为4,4'-DDS,推测
的名称为4,4'-DDS,推测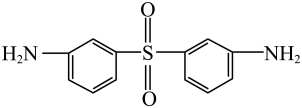 的名称为3,3'-DDS
C、参加反应的三种单体的物质的量之比为3:1:8
D、及时移除HCl,有利于提高产率并得到具有较高聚合度的缩聚物
的名称为3,3'-DDS
C、参加反应的三种单体的物质的量之比为3:1:8
D、及时移除HCl,有利于提高产率并得到具有较高聚合度的缩聚物