相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、有机物分子中基团间的相互影响会导致化学性质的不同。下列叙述错误的是( )A、苯酚能与NaOH溶液反应而乙醇不能,说明苯环活化了轻基 B、甲苯能使酸性高锰酸钾溶液褪色而甲烷不能,说明甲基活化了苯环 C、苯酚能与浓溴水反应而苯不能,说明经基活化了苯环 D、甲苯比苯更容易发生硝化反应,说明甲基活化了苯环
-
2、下列实验不能达到预期目的是( )
①乙醇和30%的硫酸共热到170℃制乙烯
②用漠水除去混在苯中的乙烯,分液得到纯净的苯
③将溴乙烧加入NaOH溶液中共热,冷却后滴入AgNO3溶液,以此检验溴乙烧中的溴元素
④将电石与水反应产生的乙快通入溴水中,溴水褪色,证明乙快和Br2发生了加成反应
⑤将2%的NaOH溶液4~6滴,滴入2mL10%的CuSO4溶液中制得Cu(OH)2悬浊液,用作检验醛基的试剂
A、①②③④⑤ B、②④ C、①③⑤ D、①②③⑤ -
3、NA为阿伏加德罗常数的值。下列说法正确的是( )A、28g晶体硅中Si-Si键的数目为4NA B、12g石墨中C-Cσ键的数目为NA C、31g白磷(P4)中P-P键的数目为1.5NA D、60gSiO2晶体中含Si-O键的数目为2NA
-
4、微粒间的相互作用是影响物质性质的重要因素。下列说法正确的是( )A、稳定性:H2O>H2S,是由于水分子间存在氢键 B、沸点:HBr>HCl,是由于HBr的相对分子质量较大,分子间作用力较大 C、酸性:CH2ClCOOH>CH3COOH,是由于-Cl是吸电子基,CH2ClCOOH羧基中羟基的极性更小 D、沸点:对羟基苯甲酸>邻羟基苯甲酸,是由于前者形成分子内氢键,后者形成分子间氢键
-
5、下列有关物质溶解度的说法错误的是( )A、戊醇在水中溶解度小于乙醇,主要是由于戊醇的烃基较大 B、日常生活中用有机溶剂溶解油漆,利用了“相似相溶”规律 C、乙醇与水互溶,主要是由于乙醇能与水形成分子间氢键 D、硫难溶于水,微溶于酒精,易溶于CS2 , 说明分子极性:H2O<C2H5OH<CS2
-
6、下列粒子的价层电子对互异模型为四面体形且其空间结构为V形的是( )A、SO2 B、NO C、OF2 D、ClO
-
7、下列说法正确的是( )A、
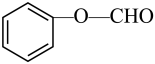 中含有醛基,所以该物质属于醛
B、间二氯苯只有1种结构能证明苯分子中6个碳原子之间的键完全相同
C、
中含有醛基,所以该物质属于醛
B、间二氯苯只有1种结构能证明苯分子中6个碳原子之间的键完全相同
C、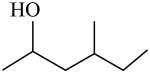 的名称为2-羟基-4-甲基己烷
D、
的名称为2-羟基-4-甲基己烷
D、 存在属于芳香族化合物的同分异构体
存在属于芳香族化合物的同分异构体
-
8、利用有机物的性质可对其进行鉴别、分离与提纯。下列说法错误的是( )A、可用碳酸氢钠溶液鉴别乙酸、乙醇与苯 B、可用溴的四氯化碳溶液鉴别环己烷与甲苯 C、可用乙醚萃取植物中的青蒿素 D、可用蒸馏的方法分离二氯甲烷、三氯甲烷和四氯化碳
-
9、VSEPR模型和杂化轨道理论常用于预测和解释分子的空间结构。下列说法正确的是( )A、凡是AB3型的共价化合物,其中心原子A均采用sp2杂化轨道成键 B、凡是中心原子采取sp3杂化的分子,其空间结构都是正四面体形 C、杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 D、凡是分子中形成π键的原子,均采用sp2杂化
-
10、下列有关同分异构体和同系物的说法正确的是( )A、2-甲基丁烷与新戊烷互为同分异构体 B、乙醚和乙醇互为同分异构体 C、淀粉、纤维素的分子式均为(C6H10O5)n , 两者互为同分异构体 D、
 和
和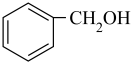 分子组成相差一个“CH2”,两者互为同系物
分子组成相差一个“CH2”,两者互为同系物
-
11、物质的聚集状态与其性能之间关系密切。下列说法错误的是( )A、等离子体由电子、阳离子和电中性粒子组成,具有良好的导电性和流动性 B、大多数离子液体含有体积很大的阴、阳离子,呈液态,难挥发 C、液晶既具有液体的流动性,又具有类似晶体的各向异性 D、圆形容器中结出的冰是圆形的,体现了晶体的自范性
-
12、下列有关共价键的说法错误的是( )A、H2O2中只有σ键没有π键 B、所有σ键的强度都比π键的大 C、卤化氢中H-F键的键能最大 D、键长和键角的数值可通过晶体的X射线衍射实验获得
-
13、生活中处处都有化学。下列说法错误的是( )A、苯甲酸及其钠盐可用作食品防腐剂 B、新冠疫苗一般采用冷藏存放,以避免蛋白质变性 C、人体内核苷酸聚合生成多聚核苷酸的过程中,发生了酯化反应 D、变质的油脂有难闻的哈喇味是因为油脂发生了加成反应
-
14、葡萄糖酸锌用于治疗缺锌引起的营养不良、厌食症、儿童生长发育迟缓等,可用葡萄糖酸钙和硫酸锌反应制得。(1)、位于周期表的(填“s”“p”“d”“f”或“ds”)区;元素氮和氧在周期表中相邻,第一电离能NO(填“>”或者“<”)。(2)、葡萄糖酸分子中所含元素的电负性由大到小的顺序为(填元素符号),该分子中碳原子杂化类型为。(3)、中的空间结构为(用文字描述)。(4)、晶体中部分O原子被N原子替代后可以改善半导体性能,键与键相比,键离子键成分的百分数较大,原因是。(5)、的立方晶胞如图所示,原子填充于O原子形成的(填多面体名称)空隙中,若晶胞的密度为阿伏加德罗常数的值用表示,则晶胞的棱长为(用代数式表示)。
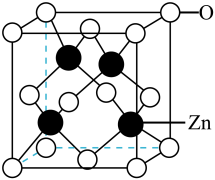
-
15、龙葵醛W是一种珍贵的香料,在自然界中未发现其存在,属于合成香料,可按下列路线合成。

已知:

回答下列问题:
(1)、化合物A的结构简式为;F中含有的官能团名称为。(2)、B→C反应的试剂和条件为。(3)、D→E的反应类型是。(4)、写出G→W反应的化学方程式。(5)、G有多种同分异构体,写出满足下列条件的有机物G的同分异构体的结构简式。①其水溶液遇溶液显紫色。
②核磁共振氢谱为四组峰,峰面积比为1∶2∶3∶6。
(6)、参照上述合成路线和信息,以乙醇为基本原料(无机试剂任选)设计制备正丁醇()的合成路线:。 -
16、2-呋喃甲酸乙酯(
 )常用于合成香料,是一种透明液体,不溶于水。实验室可用2-呋喃甲酸(
)常用于合成香料,是一种透明液体,不溶于水。实验室可用2-呋喃甲酸( )和乙醇在浓硫酸催化下反应制得2-呋喃甲酸乙酯,反应原理及部分制备装置如下:
)和乙醇在浓硫酸催化下反应制得2-呋喃甲酸乙酯,反应原理及部分制备装置如下:

Ⅰ.制备
步骤1:按图1装置,在三颈瓶中加入苯、浓硫酸、(约)无水乙醇,用仪器B加入2-呋喃甲酸,控制反应液温度保持在68℃,回流。
Ⅱ.提纯
步骤2:将反应后的混合物倒入水中,加入无水固体(20℃时,水中最多能溶解无水固体),搅拌、静置、过滤,向滤液中加入活性炭(用于吸附反应后混合物中的固体小颗粒),再次搅拌、静置、过滤。
步骤3:将滤液静置,待分层后分离水相和有机相,并用苯对水层少量多次萃取,合并有机相(仍残留少量水),再利用图2装置进行蒸馏,保留少量浓缩液,待浓缩液冷却后,在乙醇中重结晶,得无色针状晶体。
几种物质的沸点和相对分子质量如表:
物质
2-呋喃甲酸乙酯
2-呋喃甲酸
乙醇
苯和水恒沸物
沸点/℃
196
230
78
69
相对分子质量
140
112
46
-
回答下列问题:
(1)、仪器A的名称是。(2)、步骤1装置的加热方式是 , 其优点是。(3)、步骤2中的作用是。(4)、步骤3中用苯多次萃取的目的是;锥形瓶中收集的主要物质是。(5)、本实验中2-呋喃甲酸乙酯的产率为(精确到小数点后一位)。 -
17、A、B、C、D、E是原子序数依次增大的前四周期元素,其相关信息如下:
元素
相关信息
A
基态原子轨道上只有1个电子
B
基态原子核外s能级上的电子总数与p能级上的电子总数相等
C
短周期主族元素中原子半径最大
D
单质为良好的半导体材料
E
基态有5个未成对电子
请回答下列问题:
(1)、E的元素符号 , E基态原子的电子排布式。(2)、和半径较大的是(填元素离子符号)。(3)、C的基态原子含有种空间运动状态不同的电子,A与C形成的二元化合物的晶体类型为。(4)、D的氧化物熔点高于干冰的原因是;写出C的最高价氧化物的水化物与D的最高价氧化物反应的离子方程式。 -
18、已知:Diels-Alder反应
 ,则
,则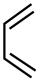 与
与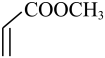 反应得到的产物是( ) A、
反应得到的产物是( ) A、 B、
B、 C、
C、 D、
D、
-
19、材料在国民经济发展中发挥着重要作用,下列有关说法不正确的是( )
A
防弹衣的主要材料:

聚合物分子内含有酰胺基
B
隐形飞机的微波吸收材料:
单体能使溴水褪色
C
隐形眼镜的材料:

该物质具有良好的亲水性,可经加聚反应制备
D
尼龙66:

由己胺和己酸经缩聚反应制备
A、A B、B C、C D、D -
20、下列有关晶体结构和性质的判断错误的是( )
A
B
C
D




金刚石晶体中,每个碳原子被12个六元环共用
晶体中,每个晶胞平均含有4个
干冰熔化或升华时,分子内的共价键被破坏
晶体中,距最近且等距的有6个
A、A B、B C、C D、D