相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列反应属于氧化还原反应且能量变化符合图像的是( )
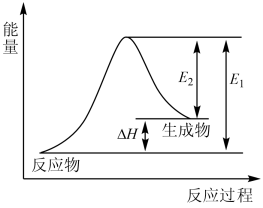 A、C(s)+CO2(g) = 2CO(g) B、CH4(g)+2O2(g) = CO2(g)+2H2O(l) C、NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l) D、Ba(OH)2·8H2O(s)+2NH4Cl(s) = BaCl2(aq)+2NH3(g)+10H2O(l)
A、C(s)+CO2(g) = 2CO(g) B、CH4(g)+2O2(g) = CO2(g)+2H2O(l) C、NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l) D、Ba(OH)2·8H2O(s)+2NH4Cl(s) = BaCl2(aq)+2NH3(g)+10H2O(l) -
2、病毒核酸采样管中的红色液体是一种样本保护液,其中含有胍盐,作用于病毒核酸保存。已知胍是有机一元碱,碱性与氢氧化钠相近;胍盐易水解为氨和尿素。以下说法错误的是( )A、核酸和蛋白质都是生物大分子 B、核酸水解最终产物中含有磷酸、六碳糖和碱基 C、胍保存不当时易吸收空气中的CO2而变质 D、合理使用尿素可以促进农作物的生长,提高粮食产量
-
3、青霉胺可以用于医学上误食铜盐的解毒,解毒原理:Cu2+形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法错误的是( )
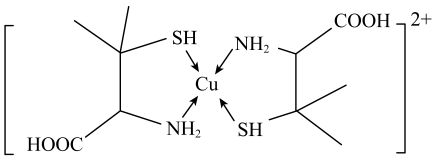 A、共价键键角的大小关系为H2O<NH3 B、电负性大小关系为O>N>H>Cu C、该配合物易溶于水的主要原因是其与水可形成分子间氢键 D、与铜离子形成配位键强弱的大小关系为H2S>NH3
A、共价键键角的大小关系为H2O<NH3 B、电负性大小关系为O>N>H>Cu C、该配合物易溶于水的主要原因是其与水可形成分子间氢键 D、与铜离子形成配位键强弱的大小关系为H2S>NH3 -
4、短周期主族元素a、b、c、d的原子序数依次增大,a为第二周期且原子核外p能级上的电子总数与s能级上的电子总数相等,b为第三周期且原子核外没有未成对电子,c的单质晶体是芯片的主要材料,d与a位于同一主族。下列说法正确的是( )A、简单离子半径a的比b的小 B、b的第一电离能大于同周期相邻的两种元素 C、c的常见氧化物是一种离子晶体 D、d的简单氢化物的空间结构为直线形
-
5、下列有关离子方程式的书写正确的是( )A、用纯铜电板电解CuCl2溶液:Cu2++2Cl-Cu+Cl2↑ B、用FeCl3溶液腐蚀铜板:2Fe3++3Cu=2Fe2++3Cu2+ C、向草酸钠溶液中加入酸性高锰酸钾溶液:2+5+16H+=2Mn2++10CO2↑+8H2O D、向H2O中投入Na2O2固体:H2O+Na2O2=2Na++2OH-+O2↑
-
6、下列事实与相应的物质的化学键键能大小无关的是( )A、熔点:H2O>HF B、活泼性:N2<P4 C、热稳定性:CH4>SiH4 D、硬度:金刚石>晶体硅
-
7、下列化学用语表示正确的是( )A、N2分子内σ键和π键个数之比为1:3 B、中子数为9的氮原子: C、邻羟基苯甲醛分子内氢键
 D、氨基苯甲酸的结构简式
D、氨基苯甲酸的结构简式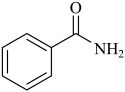
-
8、如图所示为双液锌铜原电池。下列有关叙述正确的是( )
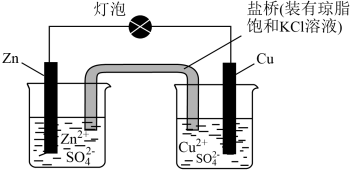 A、盐桥的作用是传导电子 B、在该电池的外电路中,电流由铜片流向锌片 C、锌片上发生还原反应:Zn-2e-=Zn2+ D、铜片做正极,电极反应是:Cu=Cu2++2e-
A、盐桥的作用是传导电子 B、在该电池的外电路中,电流由铜片流向锌片 C、锌片上发生还原反应:Zn-2e-=Zn2+ D、铜片做正极,电极反应是:Cu=Cu2++2e- -
9、设NA为阿伏加德罗常数的数值,下列说法中正确的是( )A、46g乙醇分子中所含C-H键的数目为6NA B、将标准状况下NA个H2O的体积约为22.4L C、23gNa与足量的Cl2反应转移的电子数目为NA D、60g二氧化硅晶体中含有的Si-O键数目为2NA
-
10、下列化合物属于强电解质的是( )A、CH3COOH B、NH3 C、H2O D、NaOH
-
11、3-氯靛红酸酐(
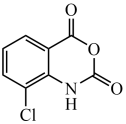 )是重要的材料中间体,其制备流程图如下:
)是重要的材料中间体,其制备流程图如下: 
已知:
 (1)、3-氯靛红酸酐的分子式为 , 苯环上碳原子的杂化方式为;(2)、有机物B的名称为 , 写出符合下列条件有机物B的所有同分异构体的结构简式;
(1)、3-氯靛红酸酐的分子式为 , 苯环上碳原子的杂化方式为;(2)、有机物B的名称为 , 写出符合下列条件有机物B的所有同分异构体的结构简式;a.苯环上只有两个取代基且互为邻位 b.既能发生银镜反应又能发生水解反应
(3)、该流程未采用甲苯直接硝化的方法制备有机物B,而是经由①、②、③三步反应进行制取,其目的是;(4)、⑥的反应类型是 , ⑥的主要目的是;(5)、⑧的反应试剂和条件为;F中含氧官能团的名称为;(6)、以有机物C为原料,在一定条件下制备含酰胺基聚合物的化学方程式。 -
12、乙酰基二茂铁是橘红色固体,熔点为81℃,沸点为163℃,常用作火箭燃料的添加剂。由二茂铁合成乙酰基二茂铁的原理如下图所示。已知乙酸酐
 易水解。
易水解。
实验步骤如下:
步骤①:称取0.1g(0.00054mol)二茂铁,放入仪器A中,加入2mL(0.02mol)新蒸的乙酸酐,放入磁子,并装上空气冷凝管和干燥管,在60~75℃水浴中用磁力搅拌器搅拌溶解(见制备装置图,部分仪器已略去)后,迅速加入6~8滴浓磷酸,使反应液呈深红色,在室温下再搅拌60min。
步骤②:将反应液转入盛有约5g冰的烧杯中,用冷水刷洗反应瓶并将刷洗液并入烧杯中。滴加氢氧化钠水溶液至pH为7~8.此时有大量橘红色固体析出。冷却后抽滤,并用少量冷水洗涤2次。在小于60℃红外灯下烘干后,刮下粗产物。
(1)、仪器A的名称为;(2)、装有无水氯化钙干燥管的作用是;(3)、步骤②中用pH试纸测定溶液的pH的操作是;用碳酸氢钠替换氢氧化钠中和产物时不需测定溶液的pH,观察到 , 可作为中和反应完成的判断标准;固体碳酸氢钠需分批加入,原因是;(4)、红外灯的温度不宜过高的原因是 , 提纯乙酰基二茂铁粗品的方法是 , 提纯后得到乙酰基二茂铁0.037g,本实验的产率是(保留两位有效数字);(5)、二茂铁由两个环戊二烯负离子与亚铁离子结合而成,已知分子中的大键可用符号表示,其中m代表参与形成大键的原子数,n代表参与形成大键的电子数(如苯分子中的大键可表示为),则中的大键应表示为 , 已知二乙酰基二茂铁 只有一种结构(由于乙酰基的致钝作用,使两个乙酰基不在一个环上),能否绕着与金属键合的轴转动?(填“能”或“否”)。
只有一种结构(由于乙酰基的致钝作用,使两个乙酰基不在一个环上),能否绕着与金属键合的轴转动?(填“能”或“否”)。 -
13、党的二十大报告指出“深入推进能源革命”“加快规划建设新型能源体系”,天然气是一种较为清洁的燃料,具有重大发展潜力。回答下列问题:(1)、天然气的主要成分是甲烷,甲烷的空间构型为;(2)、可经过如下步骤催化加氢转化为甲烷:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
反应Ⅲ的 , 已知其正反应活化能为 , 则其逆反应活化能;
(3)、我国科研人员通过控制光沉积的方法构建型复合材料光催化剂,其中和离子渗透Nafion膜可协同、分别反应,构建了一个人工光合作用体系,其反应机理如下:
总反应的化学方程式为;
(4)、动力学研究:在多个1L恒容密闭装置中,分别充入和发生反应Ⅲ,在不同温度下反应至10min时,测得转化率随温度的关系如图1所示。已知该反应的速率方程为 , , 其中、为速率常数,受温度影响,lgk与1/T的关系图如图2所示。
①图1中,反应至a点的二氧化碳平均反应速率为;
②图1中,反应至c点 (填“大于”“小于”或“等于”),原因是 , c点的对应的是图2中的点。(已知 , k为速率常数,AR为常数,Ea为活化能,T为温度)
-
14、某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略):

已知:①NaClO溶液与Ag反应的产物为AgCl、NaOH和
②NaClO溶液在受热或酸性条件下易分解:
③铜和银是同族相邻元素
请回答下列问题:
(1)、“氧化”阶段需在80℃条件下进行,适宜的加热方式为;(2)、银元素位于元素周期表的第周期第族,属于区;(3)、“溶解”阶段中发生的反应的离子方程式为;(4)、为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并将洗涤液合并入;(5)、若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,则需要增加氨水的用量,除因过量NaClO与反应外(该条件下与不反应),还因为。 -
15、科学家发现对LiTFSI(一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。LiTFSI的结构如图,X、Y、Z、M为同一短周期元素,Z与W位于同一主族。下列叙述正确的是( )
 A、元素电负性: B、第一电离能: C、、的VSEPR模型均为直线形 D、M的简单氢化物的沸点一定高于X的氢化物
A、元素电负性: B、第一电离能: C、、的VSEPR模型均为直线形 D、M的简单氢化物的沸点一定高于X的氢化物 -
16、根据下列实验操作和实验现象所得出的结论正确的是( )
选项
实验操作
实验现象
实验结论
A.
将苯、液溴与铁粉充分混合,将生成的气体先后导入、溶液
溶液中产生淡黄色沉淀
苯与液溴发生了取代反应
B.
加热与浓的混合液至170℃,将生成的气体导入溴水中
溴水褪色
发生了消去反应
C.
向电石中滴加饱和食盐水,将生成的气体导入酸性溶液中
酸性溶液褪色
被氧化
D.
向固体中滴加乙酸溶液,将生成的气体导入苯酚钠溶液中
苯酚钠溶液变浑浊
酸性强弱:乙酸>碳酸>苯酚
A、A B、B C、C D、D -
17、冠醚是一类皇冠状的分子,其中18-冠-6可以与形成超分子。制备18-冠-6的方法如图所示。下列说法正确的是( )
 A、18-冠-6分子中碳原子都采用sp杂化 B、18-冠-6与之间通过离子键形成超分子 C、18-冠-6分子中所有原子一定共平面 D、该制备18-冠-6的反应类型为取代反应
A、18-冠-6分子中碳原子都采用sp杂化 B、18-冠-6与之间通过离子键形成超分子 C、18-冠-6分子中所有原子一定共平面 D、该制备18-冠-6的反应类型为取代反应 -
18、下列事实不能用有机化合物分子中基团间的相互作用解释的是( )A、乙烯能发生加成反应而乙烷不能 B、苯在50~60 ℃时发生硝化反应而甲苯在30 ℃时即可发生 C、甲苯能使酸性KMnO4溶液褪色而甲烷不能 D、苯酚能与NaOH溶液反应而乙醇不能
-
19、咖啡酸是中药杜仲的活性成分之一,具有保肝利胆、促进肝细胞再生的作用,其结构简式如图所示。下列关于咖啡酸的叙述正确的是( )
 A、咖啡酸分子中含有4种官能团 B、咖啡酸分子中含手性碳原子 C、咖啡酸能使酸性溶液褪色 D、咖啡酸不存在顺反异构
A、咖啡酸分子中含有4种官能团 B、咖啡酸分子中含手性碳原子 C、咖啡酸能使酸性溶液褪色 D、咖啡酸不存在顺反异构 -
20、2-丙醇在铜作催化剂并加热的条件下,可被氧化为Q。下列物质与Q互为同分异构体的是( )A、 B、 C、 D、