相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、关于生活中的有机物,下列说法不正确的是( )A、皮肤接触浓硝酸变黄是蛋白质的颜色反应 B、工业上利用油脂在碱性条件下的水解反应制取肥皂和甘油 C、食用植物油的主要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质 D、纤维素、油脂、蛋白质均是天然高分子化合物
-
2、如图是一些常见有机物的转化关系,以下有关反应的说法不正确的是( )
 A、反应①是加成反应 B、以反应②是加聚反应 C、反应③是消去反应 D、反应⑧是氧化反应
A、反应①是加成反应 B、以反应②是加聚反应 C、反应③是消去反应 D、反应⑧是氧化反应 -
3、2018年俄罗斯世界杯比赛中当运动员肌肉挫伤或扭伤时,队医随即对准运动员的受伤部位喷射药剂一氯乙烷(沸点为12.27℃,进行局部冷冻麻醉应急处理。那么制取一氯乙烷的最好方法是( )A、乙烷与氯气发生取代反应 B、乙烯与氯气发生加成反应 C、乙烷与氯化氢反应 D、乙烯与氯化氢发生加成反应
-
4、下列化学方程式书写不正确的是( )A、苯与液溴反应:
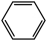 +Br2
+Br2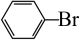 +HBr
B、实验室制备乙烯:CH3CH2OH CH2=CH2↑+H2O
C、溴乙烷与NaOH的乙醇溶液共热:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
D、向苯酚钠溶液中通入CO2:2
+HBr
B、实验室制备乙烯:CH3CH2OH CH2=CH2↑+H2O
C、溴乙烷与NaOH的乙醇溶液共热:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
D、向苯酚钠溶液中通入CO2:2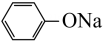 +CO2+H2O→2
+CO2+H2O→2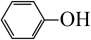 +Na2CO3
+Na2CO3
-
5、某有机物的结构简式如图所示,关于该有机物,下列叙述不正确的是( )
 A、一定条件下,能发生加聚反应 B、1mol该有机物与溴水发生反应,消耗Br2的物质的量为1mol C、该有机物有三种官能团 D、该有机物苯环上的一个H被Cl取代,有3种产物
A、一定条件下,能发生加聚反应 B、1mol该有机物与溴水发生反应,消耗Br2的物质的量为1mol C、该有机物有三种官能团 D、该有机物苯环上的一个H被Cl取代,有3种产物 -
6、下列分子的所有原子肯定不在同一平面内的是( )A、ClCH=CHCl B、CO2 C、CH≡CH D、CH3C≡CCH3
-
7、下列实验中,能达到相应实验目的的是( )
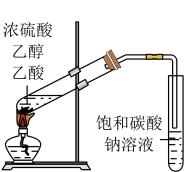



A.制备并收集乙酸乙酯
B.除去甲烷中的乙烯
C.验证溴乙烷的消去产物是乙烯
D.分离乙醇和乙酸
A、A B、B C、C D、D -
8、下列有关芳香烃的叙述中,不正确的是( )A、苯与浓硝酸、浓硫酸共热可反应生成硝基苯
 B、甲苯与氯气在光照下发生一元取代反应,主要生成
B、甲苯与氯气在光照下发生一元取代反应,主要生成 C、乙苯可被酸性高锰酸钾溶液氧化为
C、乙苯可被酸性高锰酸钾溶液氧化为 (苯甲酸)
D、苯乙烯在合适条件下催化加氢可生成
(苯甲酸)
D、苯乙烯在合适条件下催化加氢可生成
-
9、关于正丁烷(CH3﹣CH2﹣CH2﹣CH3)、异丁烷(
 )的下列说法错误的是( ) A、它们互称同分异构体 B、它们的一氯代物都各有2种 C、它们互称同系物 D、正丁烷和异丁烷化学性质相似
)的下列说法错误的是( ) A、它们互称同分异构体 B、它们的一氯代物都各有2种 C、它们互称同系物 D、正丁烷和异丁烷化学性质相似 -
10、下列各组混合物能用分液漏斗分离的是( )A、苯和甲苯 B、己烯和己烷 C、乙酸乙酯和水 D、丙酮和乙醇
-
11、下列有机物的命名正确的是( )A、
 苯甲酸
B、CH2=CH-CH=CH2 1,3-二丁烯
C、
苯甲酸
B、CH2=CH-CH=CH2 1,3-二丁烯
C、 1,3-苯二酚
D、
1,3-苯二酚
D、 2-羟基丙烷
2-羟基丙烷
-
12、由A(C2H2)和E(C7H6O)制备聚乙烯醇缩苯丙醛(M)的合成路线如图所示:

已知:
 (R、R′代表氢原子或烃基)。
(R、R′代表氢原子或烃基)。回答下列问题:
(1)、反应①②的反应类型分别是、。(2)、E的化学名称是 , F中官能团名称是。(3)、H的结构简式是;反应③的化学方程式是。(4)、写出一种满足下列条件的B的同分异构体的结构简式:。①有3种氢原子;②能发生银镜反应与水解反应。
(5)、参照上述合成路线和信息,写出以乙醇为原料合成 的合成路线:(无机试剂任选)。 -
13、某校兴趣小组采用类似制乙酸乙酯的装置(如图),由环己醇制备环己烯,其反应原理为
 。环己醇和环己烯的部分性质见下表:
。环己醇和环己烯的部分性质见下表: 有机物
密度/(g·cm-3)
熔点/℃
沸点/℃
溶解性
环己醇
096
25
161
能溶于水
环己烯
0.81
-103
83
难溶于水

回答下列问题:
(1)、制备粗品将12.5L环己醇加入试管A中,再加入1mL浓硫酸,摇匀后加入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品(含有环己醇和少量酸性杂质)。
①导管B的作用是。
②加入碎瓷片的目的是。
(2)、制备精品
①向环己烯粗品中加入Na2CO3溶液,振荡、静置、分层,环己烯在分液漏斗的层,放出下层液体后,将。
②将所得的环己烯按如图装置蒸馏,蒸馏时要加入生石灰,其目的是。
③收集产品时,应控制温度在左右,实验制得的环己烯精品产量低于理论产量,其原因可能是(填字母)。
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时部分环己醇随产品一起蒸出
④区分环己烯精品和粗品的试剂是(填“酸性高锰酸钾溶液”或“金属钠”)。
-
14、丙酸苯甲酯为无色液体,有鲜花的甜香气味,常用于配制食品、香烟、香皂、日用化妆香精,其合成路线如图所示。

回答下列问题:
(1)、D的结构简式为 , 其名称为。(2)、反应①的化学方程式为 , 反应②的反应类型为。(3)、E中含有种不同化学环境的氢,其与NaOH溶液反应的化学方程式为。(4)、能与FeCl3溶液发生显色反应的D的同分异构体有种,其中核磁共振氢谱有4组峰的同分异构体的结构简式为。 -
15、二乙酸-1,4-环己二醇酯可通过下列路线合成:
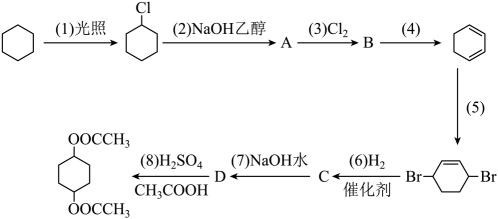
请你写出各步反应的化学方程式,并指出其反应类型。(提示:路线中(5)的反应可利用1,3-环己二烯与Br2的1,4-加成反应)
(1)、(2)、(3)、(4)、(5)、(6)、(7)、(8)、 -
16、保幼酮是保幼激素的一种,其可以保持昆虫的幼虫特征而阻止幼虫转变为成虫,从而达到阻止繁殖的作用,其结构简式如图所示。下列有关保幼酮的说法正确的是( )
 A、分子式为C16H28O3 B、不能发生加聚反应 C、环上的一氯代物有5种(不包括立体异构) D、一定条件下1mol保幼酮最多与3molH2发生反应
A、分子式为C16H28O3 B、不能发生加聚反应 C、环上的一氯代物有5种(不包括立体异构) D、一定条件下1mol保幼酮最多与3molH2发生反应 -
17、有机化合物分子中基团间的相互影响会导致其化学性质的改变。下列叙述不能说明上述观点的是( )A、苯酚易与NaOH溶液反应,而乙醇不能 B、甲酸乙酯能够发生银镜反应,而乙酸乙酯不能 C、甲苯可使酸性溶液褪色,而乙烷不能 D、苯酚与浓溴水反应而苯与液溴在催化下反应
-
18、Y是合成药物查尔酮类抑制剂的中间体,可由X在一定条件下与Z反应制得。下列叙述正确的是( )
 A、Y含有2种官能团 B、Y、Z均含有顺反异构体 C、一定条件下,X、Y均能与新制氢氧化铜反应 D、Z与AgNO3溶液反应,生成浅黄色沉淀
A、Y含有2种官能团 B、Y、Z均含有顺反异构体 C、一定条件下,X、Y均能与新制氢氧化铜反应 D、Z与AgNO3溶液反应,生成浅黄色沉淀 -
19、从水杨酸(
 )到阿司匹林(
)到阿司匹林( )、入长效缓释阿司匹林,水杨酸的结构改造经历了数百年。下列有关说法正确的是( ) A、阿司匹林的水溶性小于水杨酸 B、可用碳酸氢钠溶液区分水杨酸和阿司匹林 C、阿司匹林能与氯化铁溶液发生显色反应 D、1 mol
)、入长效缓释阿司匹林,水杨酸的结构改造经历了数百年。下列有关说法正确的是( ) A、阿司匹林的水溶性小于水杨酸 B、可用碳酸氢钠溶液区分水杨酸和阿司匹林 C、阿司匹林能与氯化铁溶液发生显色反应 D、1 mol 与足量NaOH溶液反应,最多消耗2 mol NaOH
与足量NaOH溶液反应,最多消耗2 mol NaOH
-
20、异松油烯可以用于制作香精,防腐剂和工业溶剂等,其结构简式如图。下列有关异松油烯的说法不正确的是( )
 A、分子式是 B、能发生加成、氧化、取代反应 C、存在属于芳香烃的同分异构体 D、核磁共振氢谱有6个吸收峰
A、分子式是 B、能发生加成、氧化、取代反应 C、存在属于芳香烃的同分异构体 D、核磁共振氢谱有6个吸收峰