相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列关于元素及其化合物的性质说法不正确的是( )A、浓硫酸与蔗糖反应,观察到蔗糖变黑,体现了浓硫酸的脱水性 B、硝酸见光受热易分解,一般保存在棕色试剂瓶中,放置在阴凉处 C、燃油发动机产生的、与反应能生成和 , 因此可直接排放 D、铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物
-
2、2022年11月29日,神舟十五号载人飞船成功发射,我国6名航天员首次实现太空会师。下列说法错误的是( )A、活性炭可用于吸附航天舱中异味 B、可用作宇航乘组的供氧剂 C、镁铝合金可用作飞船零部件材料 D、可用作航天器的太阳能电池板
-
3、为抑制新冠疫情的传播,除做好个人防护外,也要做好环境物品等的消毒。下列物质不能用于消毒杀菌的是( )A、酒精 B、明矾 C、次氯酸钠 D、过氧乙酸(
 )
)
-
4、如图是制备漂白粉的实验装置,下列说法正确的是( )
 A、将MnO2和浓盐酸置于锥形瓶中反应制备Cl2 B、三颈烧瓶中发生反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O C、冰水浴的作用是降低反应温度,防止发生副反应 D、锥形瓶和三颈烧瓶之间应加装一个盛有饱和碳酸氢钠溶液的洗气瓶
A、将MnO2和浓盐酸置于锥形瓶中反应制备Cl2 B、三颈烧瓶中发生反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O C、冰水浴的作用是降低反应温度,防止发生副反应 D、锥形瓶和三颈烧瓶之间应加装一个盛有饱和碳酸氢钠溶液的洗气瓶 -
5、下列关于乙烯的说法正确的是( )A、与溴单质或酸性高锰酸钾反应都与碳碳双键有关,但是两者原理不相同 B、CH3CH2Br不可能是乙烯的加成产物,只能是CH3CH3的一卤取代产物 C、乙烯和聚乙烯二者都能使溴水褪色,性质相似 D、乙烯与氢气发生加成反应生成乙烷,所以除去乙烷中混有少量乙烯,可以在一定条件下通入过量氢气
-
6、下列有关物质的分离提纯操作的说法正确的是( )A、蒸馏时,温度计应插入液面以下 B、分液时,下层液体从分液漏斗的下口流出,上层液体从上口倒出 C、可用酒精萃取溴水中的溴 D、东晋葛洪《肘后备急方》中称“青蒿一握,以水二升渍,绞取汁”,以此法提取青蒿素属于过滤
-
7、不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3以防止腐蚀。(1)、基态碳原子的电子排布图为。(2)、铬和镍元素都易形成配位化合物:
①[Cr(H2O)4Cl2]Cl•2H2O中Cr3+的配位数为。
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是 , 在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为。
③氨是分子(填“极性”或“非极性”),中心原子的轨道杂化类型为 , 氨的沸点高于PH3 , 原因是。
(3)、镍元素基态原子的价电子排布式为 , 3d能级上的未成对电子数为。(4)、单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是。(5)、某镍白铜合金的立方晶胞结构如图所示。若合金的密度为dg/cm3 , 晶胞参数a=cm。
-
8、中国早在周朝已能冶炼铸铁了。目前,铁及其化合物广泛地应用到各个领域。请回答下列问题:(1)、基态铁原子的电子排布式为。(2)、我国菱铁矿FeCO3储量较为丰富,其中CO的空间结构为 , 与CO互为等电子体的一种分子的化学式为。(3)、草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如图,碳原子的杂化方式是。
 (4)、Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20℃、103.6℃左右。因此可知Fe(CO)5属于晶体;从电子对给予情况来看,CO与Fe之间形成键。(5)、铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是。若该晶体的密度是dg•cm-3 , 则两个最近的Fe间的距离为pm(设NA为阿伏加德罗常数的值)。
(4)、Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20℃、103.6℃左右。因此可知Fe(CO)5属于晶体;从电子对给予情况来看,CO与Fe之间形成键。(5)、铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是。若该晶体的密度是dg•cm-3 , 则两个最近的Fe间的距离为pm(设NA为阿伏加德罗常数的值)。
-
9、某化合物Ⅰ可通过如图合成路线合成:

已知:
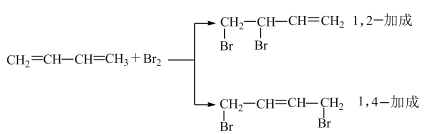
回答下列问题:
(1)、中,属于烃的是(填标号)。(2)、的反应类型属于(填“加成”或“加成”)。(3)、F在氢氧化钠的水溶液中加热,发生反应的化学方程式为。(4)、完全燃烧消耗。(5)、最多可与反应,所得产物为。(6)、中浓硫酸的作用是。 -
10、某化学兴趣小组用甲、乙两套装置(如图所示)进行丙烯酸(H2C=CHCOOH)与乙醇(CH3CH2OH)酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:
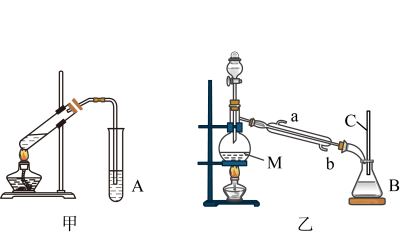 (1)、仪器M的名称为 , 仪器A、B中的溶液均为。(2)、甲、乙两套装置中效果比较好的装置是 , 原因是。(3)、乙装置中冷凝水应该从(填“a”或“b”)口进入。(4)、按甲图安装好仪器后,在反应管中加入配制的体积比为3∶2的乙醇和丙烯酸,加热至沸腾,很久也没有果香味液体生成,原因是。(5)、乙醇需要过量一些的原因是。(6)、某同学选用了CH3CH218OH、CH2=CH-COOH两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:。(7)、下列有关有机知识表述正确的是____(填字母)。A、乙烯可以通过加成反应制得CH3CHCl2 B、等物质的量的甲烷和乙酸完全燃烧时所需O2的质量相同 C、乙酸乙酯中含有乙酸杂质,可加入一定量的乙醇和浓硫酸通过酯化反应除去 D、葡萄糖、麦芽糖均能与银氨溶液发生银镜反应
(1)、仪器M的名称为 , 仪器A、B中的溶液均为。(2)、甲、乙两套装置中效果比较好的装置是 , 原因是。(3)、乙装置中冷凝水应该从(填“a”或“b”)口进入。(4)、按甲图安装好仪器后,在反应管中加入配制的体积比为3∶2的乙醇和丙烯酸,加热至沸腾,很久也没有果香味液体生成,原因是。(5)、乙醇需要过量一些的原因是。(6)、某同学选用了CH3CH218OH、CH2=CH-COOH两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:。(7)、下列有关有机知识表述正确的是____(填字母)。A、乙烯可以通过加成反应制得CH3CHCl2 B、等物质的量的甲烷和乙酸完全燃烧时所需O2的质量相同 C、乙酸乙酯中含有乙酸杂质,可加入一定量的乙醇和浓硫酸通过酯化反应除去 D、葡萄糖、麦芽糖均能与银氨溶液发生银镜反应 -
11、布洛芬具有抗炎、镇痛、解热作用,其结构简式如图所示,下列关于布洛芬的说法错误的是( )
 A、苯环上的一氯代物有2种 B、1mol布洛芬最多能消耗1molNaOH C、布洛芬可以与乙醇发生酯化反应 D、布洛芬中的所有原子可能共平面
A、苯环上的一氯代物有2种 B、1mol布洛芬最多能消耗1molNaOH C、布洛芬可以与乙醇发生酯化反应 D、布洛芬中的所有原子可能共平面 -
12、在有机合成中,常会将官能团消除或增加,下列相关过程中反应类型及相关产物不合理的是( )A、乙烯→乙二醇:CH2=CH2

 B、溴乙烷→乙醇:CH3CH2BrCH2=CH2CH3CH2OH
C、1-溴丁烷→1-丁炔:CH3CH2CH2CH2BrCH3CH2CH=CH2
B、溴乙烷→乙醇:CH3CH2BrCH2=CH2CH3CH2OH
C、1-溴丁烷→1-丁炔:CH3CH2CH2CH2BrCH3CH2CH=CH2 CH3CH2C≡CH
D、乙烯→乙炔:CH2=CH2
CH3CH2C≡CH
D、乙烯→乙炔:CH2=CH2 CH≡CH
CH≡CH
-
13、以2-溴丙烷为原料制取1,2-丙二醇,需要经过的反应是( )A、加成-消去-取代 B、消去-加成-取代 C、消去-取代-加成 D、取代-消去-加成
-
14、苹果酸分子的结构简式为
 。下列说法正确的是( ) A、1mol苹果酸与足量金属Na反应生成1mol H2 B、1mol苹果酸可与3mol NaOH发生反应 C、苹果酸分子中的官能团有羟基和羧基 D、
。下列说法正确的是( ) A、1mol苹果酸与足量金属Na反应生成1mol H2 B、1mol苹果酸可与3mol NaOH发生反应 C、苹果酸分子中的官能团有羟基和羧基 D、 与苹果酸互为同分异构体
与苹果酸互为同分异构体
-
15、分子式为C5H12O的饱和一元醇有机物有( )A、4种 B、6种 C、8种 D、9种
-
16、下列转化中的“X溶液”可以是( )
 A、NaOH B、Na2CO3 C、NaHCO3 D、Na
A、NaOH B、Na2CO3 C、NaHCO3 D、Na -
17、下列醇中既能发生消去反应,又能被氧化为酮的是( )
①
 ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥ A、①⑤ B、②③ C、②④ D、②⑥
A、①⑤ B、②③ C、②④ D、②⑥ -
18、2020年以来新冠病毒疫情在全国出现,一次性医用口罩对于全国人民至关重要,口罩的主要原料为聚丙烯树脂。下列说法错误的是( )A、聚丙烯结构简式为
 B、由丙烯合成聚丙烯的反应类型为加聚反应
C、聚丙烯不能使酸性高锰酸钾溶液褪色
D、聚丙烯在自然环境中容易降解
B、由丙烯合成聚丙烯的反应类型为加聚反应
C、聚丙烯不能使酸性高锰酸钾溶液褪色
D、聚丙烯在自然环境中容易降解
-
19、核糖是合成核酸的重要原料,结构简式为:CH2OH-CHOH-CHOH-CHOH-CHO,下列关于核糖的叙述正确的是( )A、可以与新制氢氧化铜悬浊液反应 B、与葡萄糖互为同系物 C、可以跟氯化铁溶液显色 D、可以使紫色石蕊试液变红
-
20、用分子式C7H8O所表示的某化合物含有苯环,并且和FeCl3溶液不发生显色反应,这种化合物的同分异构体有 ( )A、2种 B、3种 C、4种 D、5种