相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、等物质的量的下列有机化合物完全燃烧,消耗氧气的量最多的是( )A、己烷 B、苯 C、甲苯 D、苯甲醇
-
2、可以用分液漏斗分离的一组混合物是( )A、苯和甲苯 B、乙醇和水 C、苯和水 D、溴和四氯化碳
-
3、鉴别下列各组有机物所选试剂或方法可行的是( )A、乙烯和乙炔:溴的四氯化碳溶液 B、甲苯和二甲苯:酸性溶液 C、淀粉和蛋白质:碘水 D、乙酸和丙酸:碳酸钠溶液
-
4、下列有机物中,沸点最高的是( )A、乙烷 B、甲醇 C、乙醇 D、乙二醇
-
5、某烯烃经催化加氢后可得到2-甲基丁烷,则该烯烃的名称不可能是( )A、甲基丁烯 B、甲基丁烯 C、甲基丁烯 D、甲基丁烯
-
6、由的转化过程中,经过的反应类型依次为( )A、氧化、取代、加成、消去 B、消去、取代、加成、水解 C、还原、消去、加成、取代 D、加成、取代、消去、取代
-
7、下列化学用语书写正确的是( )A、四氯化碳的电子式为:
 B、分子的球棍模型:
B、分子的球棍模型: C、乙醛的结构简式为:
D、甲苯的分子式:
C、乙醛的结构简式为:
D、甲苯的分子式:
-
8、化学与生活密切相关,下列有关说法错误的是( )A、油脂没有固定的熔沸点 B、酚醛树脂是用酚类与醛类在酸性或碱性的催化下相互缩合而成的高分子化合物 C、一定条件下蔗糖和麦芽糖均能水解 D、纤维素和聚氯乙烯均为天然的高分子化合物
-
9、下列有机物类别划分正确的是( )A、
 属于苯的同系物
B、含有碳碳双键,属于烯烃
C、
属于苯的同系物
B、含有碳碳双键,属于烯烃
C、 属于链状化合物
D、
属于链状化合物
D、 属于脂环化合物
属于脂环化合物
-
10、汽车工业的发展得益于化工等行业的支撑。(1)、三种可燃物在空气中发生燃烧反应的能量变化示意图如图,你认为可燃物(填“A”、“B”或“C”)更适合用作车用燃料。(已知:燃点是指在规定的条件下,应用外部热源使物质表面起火并持续燃烧一定时间所需的最低温度,燃点较低时存在安全隐患。)
 (2)、燃油汽车尾气有污染,尾气中生成过程中的能量变化如图所示。
(2)、燃油汽车尾气有污染,尾气中生成过程中的能量变化如图所示。
生成(填“吸收”或“放出”)的热量。
(3)、利用催化技术可将汽车尾气中的和转化为和 , 化学方程式为:①某温度下,在容积的密闭容器中通入和 , 测得不同时间如下表:
时间/s
0
1
2
3
……
……
用的浓度变化表示的平均反应速率为。
②下列可以表明上述反应已达到平衡状态的是。
a.容器中的气体压强保持不变 b.的浓度之比为
c.的浓度不再改变 d.相同时间内,反应消耗同时消耗
(4)、国家电投氢能公司全自主研发的“氢腾”燃料电池系统广泛应用于氢能大巴。某种氢燃料电池的内部结构如图,下列说法正确的是( ) A、电池工作时,电解质溶液中的向b极移动 B、a极发生的电极反应为 C、b极为正极,发生氧化反应 D、当外电路有电子转移时,b极消耗
A、电池工作时,电解质溶液中的向b极移动 B、a极发生的电极反应为 C、b极为正极,发生氧化反应 D、当外电路有电子转移时,b极消耗 -
11、某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取 , 并完成相关性质探究(不考虑水蒸气)。(1)、I.实验验证气体成分:兴趣小组同学设计了如图所示装置进行了实验探究。
为验证并吸收 , 装置B中加入的试剂为;装置C中品红溶液的作用是。 (2)、装置D中加入的试剂为。(3)、装置H的作用为。(4)、Ⅱ.实验探究的还原性:将分别通入无氧、有氧且浓度均为的溶液和2溶液中,探究和哪种微粒起到了主要氧化作用,实验记录如下:
(2)、装置D中加入的试剂为。(3)、装置H的作用为。(4)、Ⅱ.实验探究的还原性:将分别通入无氧、有氧且浓度均为的溶液和2溶液中,探究和哪种微粒起到了主要氧化作用,实验记录如下:
曲线a所示溶液降低,说明能与水反应生成(填化学式);pH变化 溶液中是否产生沉淀 
溶液(无氧)中无白色沉淀 溶液(有氧)中有白色沉淀 溶液(无氧)中有白色沉淀 溶液(有氧)中有白色沉淀 (5)、曲线b所示溶液中的反应可按如下方式进行,请完成并配平该离子方程式:(6)、结合上述实验,可以推测,溶液(有氧)中,氧化的主要微粒是 , 其理由是。 -
12、我国空间站“天和”核心舱太阳翼电池采用自主研发的砷化镓器件,能量转化效率大大提高。已知:砷()与镓()同位于第四周期;与同主族,与P同主族。(1)、P在元素周期表中的位置是 , 镓的原子结构示意图为。(2)、非金属性强弱SP(填“大于”或“小于”),下列表述中能证明这一事实的是(填字母)。
a.S的简单氢化物的水溶液比P的简单氢化物的水溶液酸性强
b.S最高价氧化物对应的水化物的酸性强于P最高价氧化物对应的水化物的酸性
c.在反应中,P原子得电子数比S原子得电子数多
d.S的简单阴离子的还原性比P的简单阴离子的还原性弱
(3)、下列关于的推断正确的是(填序号)。①的最高正价为②原子半径: , ③元素的金属性:
(4)、 , 的酸性由强到弱的关系是。(5)、与在一定条件下化合为 , 用电子式表示的形成过程:。 -
13、(1)、I.分子模型可以帮助同学们认识有机物的微观结构,几种烃的分子模型如下图。
写出③的属于链状烷烃的同分异构体的结构简式:。 (2)、等质量的②、③、④完全燃烧时,消耗氧气的质量从大到小的顺序为(填序号)。(3)、Ⅱ.G是石油化工的重要产品,某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如图:
(2)、等质量的②、③、④完全燃烧时,消耗氧气的质量从大到小的顺序为(填序号)。(3)、Ⅱ.G是石油化工的重要产品,某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如图:
B中的官能团的名称为 , G→C的反应类型为。(4)、C→D的化学反应方程式为。(5)、实验室中制备F的反应装置如图所示:
①与教材中采用的实验装置不同,此装置中采用了球形干燥管,其作用是。试管a中加入的化学试剂是。
②若实验中用含的C与E反应则E→F的化学方程式为。
-
14、硝酸工业尾气中的、进入大气后,会形成光化学烟雾、破坏臭氧层等。可用溶液对含氨氧化物的废气进行处理,反应的化学方程式如下:① , ② , 将一定量和的混合气体通入溶液中,恰好被完全吸收。下列说法不正确的是( )A、原混合气体中在标准状况下的体积可能为 B、通入的混合气体在标况下的体积可能为 C、原混合气体中与的体积之比可能是 D、所得溶液中和的物质的量之比可能为1:2
-
15、某反应在体积为的密闭容器中进行,从各物质的量的变化情况如图所示(A、B、C均为气体)。下列说法正确的是( )
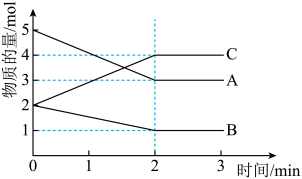 A、该反应的化学方程式为 B、说明该反应已达到平衡状态 C、由图求得A的平衡时的转化率为 D、反应开始至时,A的平均反应速率为
A、该反应的化学方程式为 B、说明该反应已达到平衡状态 C、由图求得A的平衡时的转化率为 D、反应开始至时,A的平均反应速率为 -
16、短周期主族元素W、X、Y、Z、Q的原子序数依次增大,形成的化合物是一种重要的食品添加剂,结构如图。Z核外最外层电子数与X核外电子总数相等。W的原子半径在周期表中最小。下列有关叙述正确的是( )
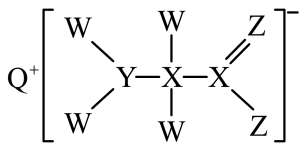 A、简单离子半径大小: B、氢化物的沸点: C、化合物中所有原子均满足8电子稳定结构 D、Y元素对应的单质与Z元素对应的单质在常温下能反应
A、简单离子半径大小: B、氢化物的沸点: C、化合物中所有原子均满足8电子稳定结构 D、Y元素对应的单质与Z元素对应的单质在常温下能反应 -
17、近年来电池研究领域涌现出纸电池,它像纸一样轻薄柔软,其结构如下图所示。某同学据此利用质量相同的铜片和镁片,电解液(溶液)和隔离膜制作简易电池。下列关于其放电过程说法正确的是( )
 A、铜片为负极 B、电子由镁片经隔离膜流向铜片 C、导线中转移时,两极质量差为 D、将铜片换为铝片,电解液换为溶液,负极为镁片
A、铜片为负极 B、电子由镁片经隔离膜流向铜片 C、导线中转移时,两极质量差为 D、将铜片换为铝片,电解液换为溶液,负极为镁片 -
18、有机物R是金银花的一种成分,具有广谱抗病毒功效,键线式为
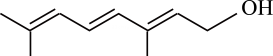 (已知的键线式为
(已知的键线式为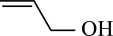 )。下列说法错误的是( ) A、R的分子式为 B、用酸性高锰酸钾溶液可以确认R含碳碳双键 C、R分子中所有碳原子可能共平面 D、R能发生加成、氧化、取代反应
)。下列说法错误的是( ) A、R的分子式为 B、用酸性高锰酸钾溶液可以确认R含碳碳双键 C、R分子中所有碳原子可能共平面 D、R能发生加成、氧化、取代反应 -
19、下列有关“实验操作”“现象”及“实验结论”都正确的是( )
选项
实验操作
现象
实验结论
A
取少量涂改液,向其中加入硝酸酸化的硝酸银溶液
无白色沉淀
涂改液中不存在氯元素
B
取溶液于试管中,加入溶液,充分反应后滴入几滴溶液
溶液变血红色
与的反应有一定限度
C
向蔗糖溶液中加入少量稀 , 加热,再加入银氨溶液
无银镜产生
蔗糖没有发生水解
D
向某溶液中加入溶液并加热,用湿润的红色石蕊试纸靠近试管口
试纸变蓝
该溶液中存在
A、A B、B C、C D、D -
20、某同学设计了下图所示两个实验装置(图I、图Ⅱ中除连接的铜棒不同外,其他均相同),下列有关说法正确的是( )
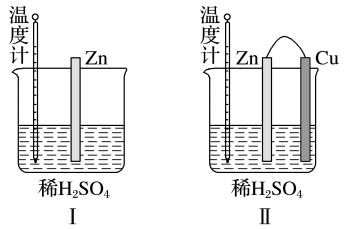 A、图I中锌棒溶解的速率比图Ⅱ的快 B、图I中温度计的示数高于图Ⅱ的示数 C、图I和图Ⅱ中温度计示数相等,且均高于室温 D、图I和图Ⅱ的气泡均产生于锌棒表面
A、图I中锌棒溶解的速率比图Ⅱ的快 B、图I中温度计的示数高于图Ⅱ的示数 C、图I和图Ⅱ中温度计示数相等,且均高于室温 D、图I和图Ⅱ的气泡均产生于锌棒表面