相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列陈述I与陈述Ⅱ均正确,且具有因果关系的是( )
选项
陈述I
陈述Ⅱ
A
常温下,向铝片表面滴加浓硫酸,没有明显现象
铝不和浓硫酸发生化学反应
B
在酸性KMnO4溶液中通入乙烯,溶液褪色
乙烯有漂白性
C
将盛满Cl2和CH4(体积比为4:1)的量筒倒置盛饱和食盐水的水槽中,光照下观察到液面缓慢上升
产物中含有易溶于水的HCl
D
将光洁的铜丝灼烧后,铜丝变黑,趁热将其插入2mL乙醇中,铜丝变红
乙醇具有氧化性
A、A B、B C、C D、D -
2、“宏观辨识与微观探析”是化学学科素养之一。下列离子方程式符合题意且正确的是( )A、向稀盐酸中加入少量钠块剧烈反应: B、在磁性氧化铁粉末中加入含淀粉的HI溶液,溶液变蓝色: C、向苛性钠溶液中通入NO2 , 红棕色气体消失,生成两种盐: D、向Na2SiO3溶液中通入过量CO2 , 产生白色沉淀:
-
3、工业上,常用氨气脱硝。一定温度下,向2L恒容密闭容器中充人6molNO和4 mol NH3 , 发生反应:。测得各物质的物质的量与时间关系如图所示。下列叙述错误的是( )
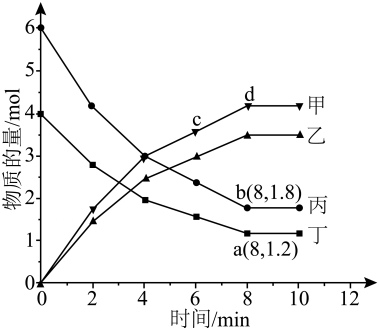 A、乙代表N2 B、逆反应速率:c<d C、b点正反应速率与逆反应速率之差等于0 D、0~8min内丁的平均反应速率为0.35mol·L-1·min-1
A、乙代表N2 B、逆反应速率:c<d C、b点正反应速率与逆反应速率之差等于0 D、0~8min内丁的平均反应速率为0.35mol·L-1·min-1 -
4、下列各组物质反应没有明显现象且属于氧化还原反应的是( )A、新制饱和氯水和SO2 B、SO2和品红溶液 C、NaClO溶液和Na2SO3溶液 D、NaHSO4溶液和NaHSO3溶液
-
5、近日,一款激素类药物“醋酸氢化可的松片”上热搜。它的键线式如图所示。已知:与四个互不相同的原子或基团相连接的碳原子叫手性碳原子。下列叙述错误的是( )
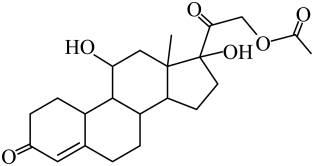 A、该物质中含有3个甲基 B、该物质分子含有手性碳原子 C、该物质能与Na、NaOH、NaHCO3溶液反应 D、该物质能发生氧化、加成、取代反应
A、该物质中含有3个甲基 B、该物质分子含有手性碳原子 C、该物质能与Na、NaOH、NaHCO3溶液反应 D、该物质能发生氧化、加成、取代反应 -
6、近日,华中科技大学武汉光电国家研究中心王鸣魁/申燕课题组等人利用分子筛的“限域效应”将SnCuxO2+x纳米团簇封装在MFI沸石通道中,允许*CO中间体在沸石通道中形成(*代表吸附在固体表面),实现了CO2的高效还原与转化,装置如图所示。下列叙述正确的是( )
 A、放电时,电子流向:b极→a极→膜X→b极 B、放电时,正极反应式为 C、放电时,转移2mol电子时理论上a极质量增重14g D、放电时,CO2被还原生成的*CO通过膜X向a极迁移
A、放电时,电子流向:b极→a极→膜X→b极 B、放电时,正极反应式为 C、放电时,转移2mol电子时理论上a极质量增重14g D、放电时,CO2被还原生成的*CO通过膜X向a极迁移 -
7、硅被誉为信息革命的“催化剂”。高纯硅的制备简易流程如下:

下列叙述正确的是( )
A、反应①的生成物有CO2、SiC B、反应②发生置换反应生成SiHCl3和H2 C、已知SiHCl3中H显-1价,则反应③中氧化剂是SiHCl3 , 还原剂是H2 D、制得的高纯硅可用于制造光导纤维 -
8、劳动有利于“知行合一”,创造幸福生活。下列劳动项目与所述的化学知识没有关联的是( )
选项
劳动项目
化学知识
A
帮厨活动:帮家长炒菜,菜起锅前添加加碘食盐
碘酸钾是强电解质
B
环保行动:宣传使用聚碳酸酯制造的包装材料
聚碳酸酯在自然界可生物降解
C
家务劳动:用热纯碱溶液清除餐具和餐桌的油污
油脂在纯碱溶液中生成可溶物
D
学农活动:对作物施碳酸氢铵肥料时要深施覆盖
碳酸氢铵见光、受热都易分解
A、A B、B C、C D、D -
9、18世纪70年代瑞典化学家舍勒将软锰矿(主要成分为MnO2)和浓盐酸混合加热得到一种黄绿色气体——氯气。受此启发,某小组设计如下实验,能达到实验目的的是( )A、制备氯气
 B、证明氯气有漂白性
B、证明氯气有漂白性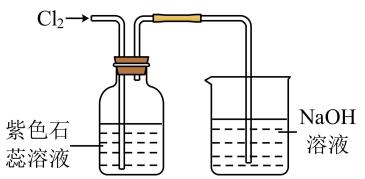 C、纯化氯气
C、纯化氯气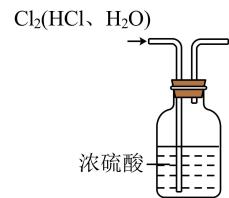 D、铁丝在氯气中燃烧
D、铁丝在氯气中燃烧
-
10、建设美丽乡村,守护中华家园,衣食住行皆化学。下列说法正确的是( )A、粉刷墙壁使用的生石灰主要成分是Ca(OH)2 B、整修乡村公路大量使用的水泥属于新型无机非金属材料 C、合理使用添加剂有助于身体健康,维生素C因难与氧气反应而做抗氧化剂 D、公园增设健身器材表面涂一层防锈漆有利于延长使用时间
-
11、“挖掘文物价值,讲好中国故事”。下列有关广东博物馆的镇馆之宝的叙述错误的是( )A、“信宜铜蚕”的材质主要是青铜,它属于合金材料 B、“千金猴王砚”具有耐强酸、强碱腐蚀性 C、“金漆木雕大神龛”中木雕的主要成分是天然高分子材料 D、制作“元青花人物纹玉壶春瓶”的主要原料是黏土
-
12、美好生活离不开化学知识的运用。下列有关叙述错误的是( )A、糖类、蛋白质都是人体必需的基本营养物质 B、石油经过分馏可得到乙烯、丙烯等化工原料 C、灾后重建时常用明矾净化饮用水 D、生活中可定期用84消毒液对居住环境消毒
-
13、化合物是一种合成药物中间体,一种合成化合物的人工合成路线如图:
 (1)、中不含原子的官能团名称 ,的分子式 。(2)、反应类型 。(3)、物质能发生消去反应,反应所需试剂和条件 ,消去后的有机产物有 种,试写出其中一种产物的结构简式 。(4)、的化学方程式为 。
(1)、中不含原子的官能团名称 ,的分子式 。(2)、反应类型 。(3)、物质能发生消去反应,反应所需试剂和条件 ,消去后的有机产物有 种,试写出其中一种产物的结构简式 。(4)、的化学方程式为 。 -
14、在实验室用乙醇制取乙烯时,常会看到烧瓶中的液体变黑,并在制得的乙烯中混有、等杂质。某课外小组的同学设计了如图所示的装置,用来制取乙烯并验证乙烯的性质。回答下列问题:
 (1)、实验室制取乙烯的反应原理: 。(2)、装置中一处明显的错误是 ,玻璃仪器的名称为 ,其中加入碎瓷片的作用是 。(3)、为证明实验过程中有产生,并验证乙烯的性质,正确的装置连接顺序 ,装置中应添加的试剂 ,装置中的现象 。
(1)、实验室制取乙烯的反应原理: 。(2)、装置中一处明显的错误是 ,玻璃仪器的名称为 ,其中加入碎瓷片的作用是 。(3)、为证明实验过程中有产生,并验证乙烯的性质,正确的装置连接顺序 ,装置中应添加的试剂 ,装置中的现象 。 -
15、(1)、有下列几组物质,请将序号填入下列空格内:
A.和
B.和石墨
C.
 和
和
D.和
E.乙醇和乙二醇
互为同位素的是;
互为同系物的是;
互为同素异形体的是 。
(2)、同分异构现象在有机化学中普遍存在,中学阶段常见的同分异构体有三类:官能团异构,位置异构,碳架异构写出符合相应条件的有机化合物的结构简式:与互为官能团异构的是 ;
与互为位置异构的是 ;
与互为碳架异构的是 ;
与
 苯甲醇互为同分异构且遇到溶液发显色反应的是 。
苯甲醇互为同分异构且遇到溶液发显色反应的是 。 -
16、写出下列有机物的系统命名或结构简式。(1)、
 。 (2)、
。 (2)、 。 (3)、2,二甲基 , 丁二烯 。(4)、2, , 三甲基戊烷 。(5)、苯甲酸甲酯 。(6)、邻氯甲苯 。(7)、 。(8)、2, , 三硝基甲苯 。
。 (3)、2,二甲基 , 丁二烯 。(4)、2, , 三甲基戊烷 。(5)、苯甲酸甲酯 。(6)、邻氯甲苯 。(7)、 。(8)、2, , 三硝基甲苯 。 -
17、某有机物的结构简式如图所示,下列有关该物质的说法正确的是 ( )
 A、该有机化合物最多能与的发生加成反应 B、它可与碳酸钠溶液反应生成 C、该有机化合物最多能与的 D、该有机化合物最多能与的发生反应
A、该有机化合物最多能与的发生加成反应 B、它可与碳酸钠溶液反应生成 C、该有机化合物最多能与的 D、该有机化合物最多能与的发生反应 -
18、某有机物的结构简式如图所示,下列有关该物质的说法正确的是( )
 A、它的分子式为 B、可使高锰酸钾酸性溶液褪色 C、含有羧基、羟基、酮基种含氧官能团 D、能与银氨溶液发生银镜反应
A、它的分子式为 B、可使高锰酸钾酸性溶液褪色 C、含有羧基、羟基、酮基种含氧官能团 D、能与银氨溶液发生银镜反应 -
19、下列化合物的分子中,所有原子都处于同一平面的有 ( )
甲烷
乙烷
苯
乙烯
A、 B、 C、 D、 -
20、分子式为的有机物共有不含立体异构( )A、种 B、种 C、种 D、种