相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、根据下列实验操作、实验现象和得出的结论均正确的是( )
选项
实验操作
现象
结论
A
在乙醇试样中加入少量CuSO4•5H2O并搅拌
试管底部有蓝色晶体
乙醇试样中含有水
B
在试管中加0.5g淀粉和4mL2mol/LH2SO4溶液,再加少量新制Cu(OH)2 , 加热
有黑色固体产生
淀粉未发生水解
C
向某溶液中加入足量的BaCl2溶液
产生白色沉淀
原溶液中一定含有SO
D
向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀,再加少许浓硫酸,迅速搅拌
蔗糖变黑
浓硫酸有脱水性
A、A B、B C、C D、D -
2、碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。的一种制备方法如图所示。

已知:
下列说法正确的是( )
A、“富集”过程中发生氧化还原反应 B、“悬浊液”静置后得到白色沉淀 C、“沉淀”的组成主要是银和铁 D、“氧化”过程通入足量提高碘单质产量 -
3、某实验小组用溶液和溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
已知:
实验序号
温度
溶液
溶液
出现沉淀所需的时间
Ⅰ
0℃
Ⅱ
0℃
Ⅲ
0℃
Ⅳ
30℃
下列说法不正确的是( )
A、实验Ⅱ中 B、实验Ⅲ中 C、对比实验Ⅰ、Ⅱ、Ⅲ可得:温度相同时,增大反应物浓度,化学反应速率增大 D、对比实验Ⅰ、Ⅳ可得:浓度保持不变时,升高温度,化学反应速率增大 -
4、下列关于酯化反应说法正确的是( )A、用CH3CH218OH与CH3COOH发生酯化反应,生成H218O B、反应液混合时,将浓硫酸倒入乙醇和乙酸的混合液中 C、可用分液漏斗分离饱和Na2CO3溶液和乙酸乙酯的混合溶液 D、在制备乙酸乙酯的实验中,为了防止乙酸和乙醇挥发,小火加热,避免液体沸腾
-
5、银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,总反应式为Ag2O+Zn+H2O=2Ag+Zn(OH)2。下列说法中不正确的是( )A、原电池放电时,负极上发生反应的物质是Zn B、工作时,负极区溶液c(OH-)减小 C、正极发生的反应是Ag2O+2e-+H2O=2Ag+2OH- D、外电路中电流由Zn流向Ag2O
-
6、丙烯醇的结构简式为CH2=CHCH2OH,结合乙烯和乙醇的结构与性质,推测不能与丙烯醇发生的反应的物质有( )A、金属钠 B、溴水 C、NaHCO3溶液 D、氢气
-
7、已知:2SO2(g)+O2(g)2SO3(g)△H , 不同条件下反应过程能量变化如图所示。一定条件下向密闭容器中充入SO2和18O2 , 下列说法中不正确的是( )
 A、反应的△H<0 B、过程b使用了催化剂 C、断裂2molSO2+1molO2中的共价键的能量小于断裂2molSO3中的共价键的能量 D、反应一段时间后,核素18O存在于SO2、O2、SO3中,说明反应已达到化学平衡状态
A、反应的△H<0 B、过程b使用了催化剂 C、断裂2molSO2+1molO2中的共价键的能量小于断裂2molSO3中的共价键的能量 D、反应一段时间后,核素18O存在于SO2、O2、SO3中,说明反应已达到化学平衡状态 -
8、足量的铜与一定量的浓硝酸充分反应,得到4.48L(标准状况)NO2与NO的混合气体,这些气体与一定体积的O2混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入100mL4mol·L-1NaOH溶液,Cu2+恰好沉淀完全。下列说法正确的是( )A、此反应过程中转移了0.5mol的电子 B、消耗氧气的体积为1.12L(标准状况) C、参加反应的HNO3是0.45mol D、混合气体中含2.24L(标准状况)NO
-
9、可逆反应:2NO22NO+O2在恒容密闭容器中反应,下列叙述表示反应达到化学平衡状态的是( )
①单位时间内消耗2molNO2的同时生成2molNO
②混合气体的颜色不再改变
③混合气体的密度不再改变
④混合气体的平均相对分子质量不再改变
A、①②④ B、②③ C、②④ D、③④ -
10、下列方程式与所给事实不相符的是( )A、用FeCl3溶液腐蚀印刷电路板:2Fe3++Cu=2Fe2++Cu2+ B、红棕色的NO2溶于水变为无色:3NO2+H2O=2HNO3+NO C、用小苏打治疗胃酸过多:HCO+H+=CO2↑+H2O D、红热的Fe粉和水蒸气反应生成黑色固体:2Fe+3H2OFe2O3+3H2
-
11、某链状烷烃的相对密度为 H2 的 43 倍,其有多种同分异构体,其中含 4 个甲基的该烷烃的一溴取代物的数目可能是( )A、1 种 B、2 种 C、4 种 D、5 种
-
12、如图是研究 SO2性质的微型实验装置,该装置具有实验现象明显,不易污染空气的特点。实验时向 Na2SO3固体上滴几滴浓硫酸,立即用另一培养皿扣在上面。下列对实验现象的描述或所做的解释正确的是( )
 A、BaCl2溶液变浑浊,产生了 BaSO3沉淀 B、反应中所用硫酸的浓度越大越有利于 SO2的生成 C、Na2S 溶液变浑浊,静置后产生黄色沉淀 D、酸性 KMnO4溶液、品红溶液均褪色,表现了 SO2漂白性
A、BaCl2溶液变浑浊,产生了 BaSO3沉淀 B、反应中所用硫酸的浓度越大越有利于 SO2的生成 C、Na2S 溶液变浑浊,静置后产生黄色沉淀 D、酸性 KMnO4溶液、品红溶液均褪色,表现了 SO2漂白性 -
13、下列有关有机物的说法正确的是( )A、油脂都不能使酸性高锰酸钾溶液褪色 B、蛋白质遇盐溶液都会发生变性 C、纤维素和淀粉分子式相同,结构不同,所以两者互为同分异构体 D、塑料、合成纤维、合成橡胶都属于合成有机高分子材料
-
14、下列说法正确的是( )A、需要加热才能进行的反应一定是吸热反应 B、对于吸热反应,反应物所具有的总能量一定低于生成物所具有的总能量 C、等质量的硫蒸气和硫固体分别完全燃烧生成气态二氧化硫,两者放出的热量相同 D、对于放热反应,形成生成物化学键吸收的能量大于破坏反应物化学键所放出的能量
-
15、科学的假设是实验探究的先导与价值所在。下列在假设引导下的探究肯定没有意义的是( )A、探究与反应可能生成 B、探究Na与乙醇反应可能有生成 C、探究与反应可能有生成 D、探究Mg与溶液反应产生的气体中可能含有
-
16、用NA代表阿伏加德罗常数的值,下列说法正确的是( )A、46g乙醇中存在的共价键总数为7NA B、1molNa2O2固体中含阴、阳离子总数为4NA C、2.3gNa和足量氧气反应转移电子数为0.1NA D、标准状况下,11.2LCCl4中含有C—Cl键的数目为2NA
-
17、金属的冶炼体现了人类文明的发展水平。下列有关金属冶炼的说法正确的是( )A、金属被人类开发利用的时间先后顺序主要取决于金属在地壳中的含量 B、工业上金属Mg、Al都是用电解熔融氯化物的方法冶炼 C、纯铁的硬度比生铁高 D、高炉炼铁的还原剂是CO
-
18、合理利用自然资源关系到人类社会、经济和环境的可持续发展。下列说法错误的是( )A、煤干馏生成的焦炉气能使溴的CCl4溶液褪色 B、石油的分馏、煤的气化和煤的液化都是物理变化 C、化石燃料的燃烧产物在一定的天气条件下会形成次生污染物 D、石油裂化和裂解的目的是获得轻质油和多种重要的化工原料
-
19、下列设备工作时,将化学能主要转化为热能的是( )
 A、图甲燃气灶 B、图乙锂离子电池 C、图丙风力发电 D、图丁太阳能热水器
A、图甲燃气灶 B、图乙锂离子电池 C、图丙风力发电 D、图丁太阳能热水器 -
20、是锂离子电池中广泛应用的电解质。某工厂用LiF和为原料,低温条件下反应制备 , 其流程如下:
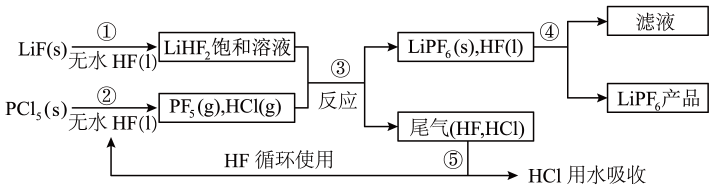
已知:HCl的沸点是−85.0℃,HF的沸点是19.5℃。
请回答下列问题:
(1)、第①步反应中无水HF的作用是、。反应设备不能用玻璃材质的原因是(用化学方程式表示)。(2)、该流程需在无水条件下进行,第③步反应中极易水解,其产物为两种酸,水解的化学方程式是。(3)、第④步分离采用的方法是。(4)、产品中通常混有少量LiF.取样品ng,测得Li的物质的量为wmol,则该样品中的物质的量是mol(用含w、n的代数式表示)。