相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下表是元素周期表的一部分,①~⑦代表对应的元素,回答下列问题:
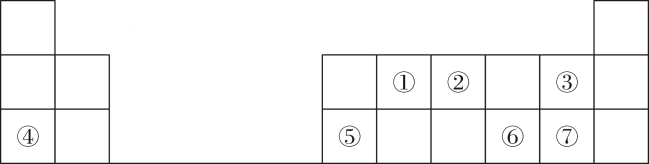 (1)、①的一种核素常用于文物考古,该核素的符号为(以形式表示)。(2)、⑥在元素周期表中的位置是第周期第族。(3)、③④⑦的简单离子半径由大到小的顺序为(填离子符号)。(4)、①②的最高价氧化物对应水化物酸性较强的是(填化学式,下同);③⑦的氢化物稳定性更高的是。(5)、⑤的单质与④的最高价氧化物对应水化物的溶液反应的离子方程式为。(6)、⑥的简单氢化物与⑦的单质反应的化学方程式为。
(1)、①的一种核素常用于文物考古,该核素的符号为(以形式表示)。(2)、⑥在元素周期表中的位置是第周期第族。(3)、③④⑦的简单离子半径由大到小的顺序为(填离子符号)。(4)、①②的最高价氧化物对应水化物酸性较强的是(填化学式,下同);③⑦的氢化物稳定性更高的是。(5)、⑤的单质与④的最高价氧化物对应水化物的溶液反应的离子方程式为。(6)、⑥的简单氢化物与⑦的单质反应的化学方程式为。 -
2、利用原电池原理设计下图装置减缓水体中钢铁设施的腐蚀。下列有关说法不正确的是( )
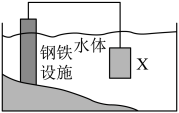 A、材料X可看作原电池的负极 B、材料X应选样金属性比Fe弱的金属 C、钢铁设施上的电极反应式为O2+4e-+2H2O=4OH- D、装置中电流从钢铁设施经导线流向材料X
A、材料X可看作原电池的负极 B、材料X应选样金属性比Fe弱的金属 C、钢铁设施上的电极反应式为O2+4e-+2H2O=4OH- D、装置中电流从钢铁设施经导线流向材料X -
3、在恒温、恒容条件下发生反应:N2(g)+3H2(g)⇌2NH3(g)。下列情况中能说明该反应达到化学平衡的是( )A、氨气的百分含量不再变化 B、混合气体的密度不再变化 C、c(N2):c(H2):c(NH3)=1:3:2 D、生成1molN2的同时生成3molH2
-
4、“液态阳光”能有效助力我国实现“碳达峰”和“碳中和”,其主要反应之一是CO2(g)+3H2(g)=CH3OH(g)+H2O(g)(放热反应)。下列有关说法正确的是( )A、升高温度能加快反应速率 B、减小H2浓度能加快反应速率 C、反应物的总能量低于生成物的总能量 D、使用催化剂不影响反应速率,能影响反应限度
-
5、下列过程中有共价键断裂的是( )A、蔗糖固体溶于水 B、硫酸氢钠固体溶于水 C、干冰升华制冷 D、氢氧化钾固体加热熔融
-
6、NA为阿伏加德罗常数的值,下列说法正确的是( )A、58.5gNaCl晶体中含有的分子数为NA B、标准状况下,22.4LC6H6中含有的分子数为NA C、标准状况下,18g18O2含有的质子数为8NA D、1L2mol/LK2SO4溶液中含有的K+数目为2NA
-
7、W、X、Y、Z是原子序数依次增大的短周期主族元素,W与Y位于同一主族,W、X、Z形成的一种化合物是漂白液的有效成分,该化合物灼烧时,火焰为黄色。下列说法正确的是( )A、原子半径:X<W B、简单氢化物的稳定性:W<Y C、Z的单质不能使品红溶液褪色 D、X、Y组成的化合物是离子化合物
-
8、淀粉在乳酸杆菌作用下可发酵转化成乳酸(
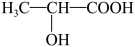 )。下列说法正确的是( ) A、淀粉与纤维素互为同分异构体 B、淀粉能发生水解,最终生成果糖 C、乳酸可通过加聚反应制得聚乳酸 D、乳酸能与NaHCO3溶液反应生成CO2
)。下列说法正确的是( ) A、淀粉与纤维素互为同分异构体 B、淀粉能发生水解,最终生成果糖 C、乳酸可通过加聚反应制得聚乳酸 D、乳酸能与NaHCO3溶液反应生成CO2 -
9、甲、乙、丙、丁是中学常见物质,存在如下转化关系。下列说法不正确的是( )
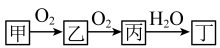 A、若甲为硫单质,则乙具有氧化性 B、若甲为CH4 , 则丙会引起酸雨 C、若丙与水反应生成丁和乙,则甲可能是NH3 D、若丙为淡黄色固体,则甲可保存在煤油中
A、若甲为硫单质,则乙具有氧化性 B、若甲为CH4 , 则丙会引起酸雨 C、若丙与水反应生成丁和乙,则甲可能是NH3 D、若丙为淡黄色固体,则甲可保存在煤油中 -
10、下列各组离子能在无色澄清的溶液中大量共存的是( )A、K+、Na+、、OH- B、Cu2+、K+、Cl-、 C、Na+、Mg2+、、 D、Al3+、Ba2+、、OH-
-
11、下列离子方程式书写正确的是( )A、硫酸铵与氢氧化钡溶液反应:Ba2++=BaSO4↓ B、金属Na与水反应:Na+H2O=Na++OH-+H2↑ C、加热MnO2与浓盐酸:MnO2+4HClMn2++2Cl-+Cl2↑+2H2O D、NaOH溶液中通入少量CO2:CO2+2OH-=+H2O
-
12、配制一定物质的量浓度的溶液,下列仪器中不需要使用的是( )A、
 B、
B、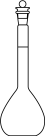 C、
C、 D、
D、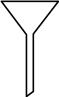
-
13、下列化学用语表达正确的是( )A、乙醛的结构简式:CH3COH B、镁离子的结构示意图:
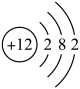 C、CH4的球棍模型:
C、CH4的球棍模型: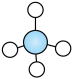 D、NH3的电子式:
D、NH3的电子式: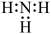
-
14、化学与生产、生活密切相关。下列说法不正确的是( )A、蒸馏可实现海水淡化 B、石油的分馏是化学变化 C、不合理使用化肥会影响土壤的酸碱性 D、维生素C具有还原性,可用作食品的抗氧化剂
-
15、材料是工业化生产的重要支撑。下列说法不正确的是( )A、光导纤维的主要成分是单质硅 B、钢是用量最大、用途最广的合金 C、新型陶瓷碳化硅硬度大,可用作砂轮的磨料 D、铝合金表面覆盖着致密的氧化膜,具有较强的抗腐蚀能力
-
16、下列分类不正确的是( )A、碳酸氢钾——盐 B、涤纶——有机高分子材料 C、医用酒精——混合物 D、冰水混合物——胶体
-
17、CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在某一容积为5L的密闭容器内,加入0.3molCO和0.3molH2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:
 (1)、根据图上数据,该温度(800℃)下的反应的平衡常数K=。(2)、在体积不变的条件下,改变下列条件能使平衡常数K增大的有____(填字母)。A、升高温度 B、降低温度 C、增大压强 D、减小压强 E、加入催化剂 F、移出一氧化碳气体(3)、若保持温度和容器的体积不变,在(1)中的平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后,H2O的转化率(填“升高”“降低”或“不变”)。(4)、在催化剂存在和800℃的条件下,在某容器中某一时刻测得c(CO)=c(H2O)=0.09mol·L-1;c(CO2)=c(H2)=0.13mol·L-1 , 则此时正、逆反应速率的大小:v正(填“>”“<”或“=”)v逆。
(1)、根据图上数据,该温度(800℃)下的反应的平衡常数K=。(2)、在体积不变的条件下,改变下列条件能使平衡常数K增大的有____(填字母)。A、升高温度 B、降低温度 C、增大压强 D、减小压强 E、加入催化剂 F、移出一氧化碳气体(3)、若保持温度和容器的体积不变,在(1)中的平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后,H2O的转化率(填“升高”“降低”或“不变”)。(4)、在催化剂存在和800℃的条件下,在某容器中某一时刻测得c(CO)=c(H2O)=0.09mol·L-1;c(CO2)=c(H2)=0.13mol·L-1 , 则此时正、逆反应速率的大小:v正(填“>”“<”或“=”)v逆。Ⅱ.还原法炼铅,发生反应:PbO(s)+CO(g)⇌Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
温度/℃
300
727
1227
lgK
6.17
2.87
1.24
(5)、某温度下,lgK=1,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为(保留两位有效数字);若向容器中充入一定量的CO气体后,平衡发生移动,再次达到平衡时,CO的百分含量(填“增大”“减小”或“不变”)。 -
18、氮化铬(CrN)是一种耐磨性良好的新型材料,难溶于水。探究小组同学用下图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。

已知:实验室中常用溶液与溶液反应制取N2;CrCl3能溶于水和乙醇。
回答下列问题:
(1)、实验准备就绪后,打开K1 , 关闭K2、K,此时应先加热(填装置代号)装置。(2)、实验中制取N2的化学反应方程式为 , 在该反应中,氧化产物与还原产物的物质的量之比为。(3)、改变K1、K2、K3的状态,加热E装置。试剂a的名称是 , 写出装置E中发生反应的化学方程式。(4)、实验过程中需间歇性微热b处导管的目的是。(5)、向7.0g所得CrN中加入足量NaOH溶液,然后通入水蒸气将NH3全部蒸出,将NH3用60mL1mol·L-1H2SO4溶液完全吸收,剩余的H2SO4用10mL2mol·L-1NaOH溶液恰好中和,则所得产品中CrN的质量分数为(保留三位有效数字)。 -
19、很多重要的工业原料来源于石油化工,结合下图回答有关问题:
 (1)、物质A的结构简式为。(2)、丙烯酸中含氧官能团的名称为。(3)、反应②的反应类型为。(4)、写出下列反应的化学方程式:
(1)、物质A的结构简式为。(2)、丙烯酸中含氧官能团的名称为。(3)、反应②的反应类型为。(4)、写出下列反应的化学方程式:丙烯酸+B→丙烯酸乙酯:;
反应④:。
(5)、28gA和丙烯的混合物在足量的氧气中燃烧,消耗的氧气在标准状况下的体积为。 -
20、蛇纹石是一种天然富镁矿物,主要成分为Mg3Si2O5(OH)4 , 还含有少量Al2O3、Fe2O3、FeO等杂质。现用蛇纹石来制取碱式碳酸镁[Mg2(OH)2CO3],其工艺流程如下:

回答下列问题:
(1)、硅元素在元素周期表中的位置是。(2)、加入的H2O2可将溶液中的Fe2+氧化成Fe3+ , 反应的离子方程式为 , 该步骤操作时应严格控制反应在较低温度下进行,其目的是。(3)、通入NH3调节pH,得到的滤渣主要充分是Fe(OH)3和(填化学式)。(4)、沉镁时先加入氨水进行预氨化处理,但氨水的加入量不宜过多,原因是。(5)、写出加热MgCO3·3H2O生成碱式碳酸镁的化学方程式。