相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。(1)、Ⅰ.如图是元素周期表的一部分,回答下列问题:
①~⑦号元素中原子半径最大的是(填元素符号),其最高价氧化物对应的水化物中含有的化学键是。该元素的单质与氧气在加热条件下反应生成R,用电子式表示R的形成过程。 (2)、①~⑦号元素的最高价氧化物对应的水化物中,酸性最强的是(填化学式,下同),碱性最强的是。(3)、将锌片、铜片用导线连接后浸入⑥的最高价氧化物对应水化物的稀溶液中,构成了原电池,则负极的电极反应式是。一段时间后,若锌片的质量减少了 , 则导线中通过电子。(4)、Ⅱ.某小组为探究的氧化性强弱,设计实验如下:
(2)、①~⑦号元素的最高价氧化物对应的水化物中,酸性最强的是(填化学式,下同),碱性最强的是。(3)、将锌片、铜片用导线连接后浸入⑥的最高价氧化物对应水化物的稀溶液中,构成了原电池,则负极的电极反应式是。一段时间后,若锌片的质量减少了 , 则导线中通过电子。(4)、Ⅱ.某小组为探究的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
序号
实验①
实验②
实验操作


现象
溶液变为黄色
实验①可得出氧化性强弱:。
(5)、实验②观察到的现象是 , 甲同学根据此现象得出结论:氧化性。乙同学认为实验②不能充分证明氧化性 , 他补做了实验③。实验③
另取实验①反应后的黄色溶液少许,先加入足量的固体,充分振荡,然后加入溶液和淀粉溶液。
补做实验③的目的是。
-
2、氨是一种重要的化工原料,在工农业生产中有广泛的应用(1)、Ⅰ.工业合成氨的反应为:。
合成氨的微观历程示意图如下,过程需要(填“吸收”或“放出”)能量。 、
、 、分别表示、催化剂)
、分别表示、催化剂) (2)、工业上可用天然气来制取合成氨的原料气氢气,发生的反应为:。在一定温度下,体积为的恒容密闭容器中测得如表所示数据。
(2)、工业上可用天然气来制取合成氨的原料气氢气,发生的反应为:。在一定温度下,体积为的恒容密闭容器中测得如表所示数据。时间
0
0.40
1.00
0
0
5
0.80
0.60
7
0.20
0.80
0.20
0.60
分析表中数据,判断时反应是否处于平衡状态?(填“是”或“否”)。内,用的浓度变化表示的平均反应速率为。
(3)、Ⅱ.实验小组为探究氮与二氧化氮的反应,设计如图实验装罪:
装置A中生石灰的作用是实验室也常用氯化铵和氢氧化钙混合固体制取氨气,写出发生反应的化学方程式。
(4)、装置B和D的作用都是干燥气体,其中盛装的干燥剂选择合理的是(填字母)。a.甲、乙都是碱石灰 b.甲、乙都是无水氯化钙
c.甲是碱石灰,乙是五氧化二磷 d.甲是浓硫酸,乙是碱石灰
(5)、若氨气与二氧化氮反应生成的产物为水和氮气,则C中发生反应的化学方程式为。(6)、该实验设计中存在着一个很严重的缺陷是。(7)、取铜于装置的锥形瓶中,再加入一定浓度的浓硝酸,充分反应后铜全部溶解,收集到和的混合气体(标准状况),则。 -
3、现有几种有机物,其球棍模型如图所示,
 代表H原子,
代表H原子, 代表C原子,
代表C原子, 代表O原子,请回答下列问题:
代表O原子,请回答下列问题: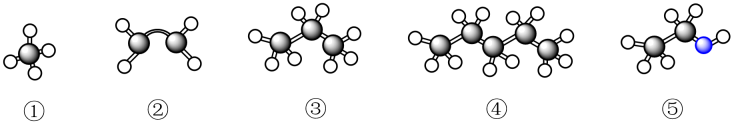 (1)、上述有机物中与①互为同系物的是(填序号)。(2)、鉴别①和②可选用下列试剂中的____(填字母)。A、稀盐酸 B、溴水 C、氢氧化钠溶液 D、四氯化碳(3)、写出④的两种同分异构体的结构简式、。(4)、从成键特点和分子结构两方面分析②、③的差异:a.;b.。(5)、⑤中所含官能团的名称为。(6)、工业上用②与水反应制取⑤,该反应的化学方程式为 , 反应类型为。(7)、写出⑤在有催化剂和加热的条件下制取乙醛的化学反应方程式。如图操作(填“能”或“不能”)制得乙醛。
(1)、上述有机物中与①互为同系物的是(填序号)。(2)、鉴别①和②可选用下列试剂中的____(填字母)。A、稀盐酸 B、溴水 C、氢氧化钠溶液 D、四氯化碳(3)、写出④的两种同分异构体的结构简式、。(4)、从成键特点和分子结构两方面分析②、③的差异:a.;b.。(5)、⑤中所含官能团的名称为。(6)、工业上用②与水反应制取⑤,该反应的化学方程式为 , 反应类型为。(7)、写出⑤在有催化剂和加热的条件下制取乙醛的化学反应方程式。如图操作(填“能”或“不能”)制得乙醛。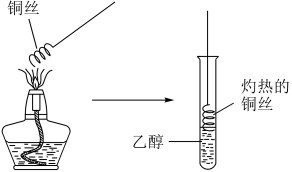
-
4、钛铁矿( , 其中为价)在高温下经氯化得到四氯化钛,氯化过程发生的化学方程式为。制取金属钛的流程如图所示:
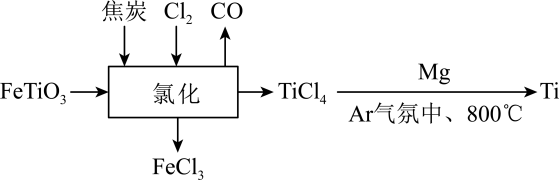
下列说法不正确的是( )
A、制取金属钛时通气的目的是隔绝空气 B、氯化过程中焦炭和都是还原剂 C、根据制取金属钛的反应可推测还原性: D、标准状况下,消耗的氯气可转移电子 -
5、下列实验过程不能达到实验目的的是( )
选项
实验目的
实验过程
A
探究浓硫酸的脱水性和强氧化性
把浓硫酸滴入蔗糖中,并将产生的气体通入澄清石灰水中,观察实验现象
B
探究反应物浓度对反应速率的影响
向分别盛有和溶液的两支试管中同时加入溶液,振荡,记录出现浑浊的时间
C
检验乙醇中是否含有水
向乙醇中加入一小粒金属钠,观察是否有无色气体产生
D
确认二氯甲烷分子不存在同分异构体
先搭建甲烷分子球棍模型,后用2个氯原子取代任意2个氢原子,重复数次,观察所得球棍模型的结构
A、A B、B C、C D、D -
6、实验室制备乙酸乙酯的装置如图所示,下列叙述不正确的是( )
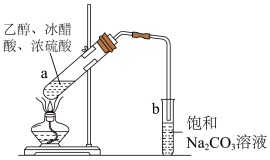 A、浓硫酸能加快酯化反应的速率 B、反应结束后试管中生成无色、有香味的油状液体 C、向试管a中先加入浓硫酸,然后边振荡试管边慢慢加入乙醇,再加入冰醋酸 D、试管中的饱和溶液可降低乙酸乙酯的溶解度,便于分层
A、浓硫酸能加快酯化反应的速率 B、反应结束后试管中生成无色、有香味的油状液体 C、向试管a中先加入浓硫酸,然后边振荡试管边慢慢加入乙醇,再加入冰醋酸 D、试管中的饱和溶液可降低乙酸乙酯的溶解度,便于分层 -
7、部分含硫物质的分类与相应化合价的关系如图,下列说法不正确的是( )
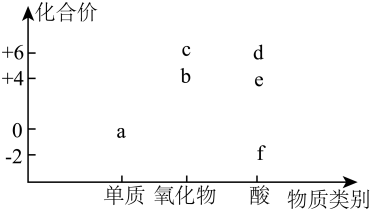 A、与在加热条件下反应生成 B、将通入溶液中,有白色沉淀产生 C、的水溶液久置在空气中酸性会变强 D、将通入的溶液中可以得到
A、与在加热条件下反应生成 B、将通入溶液中,有白色沉淀产生 C、的水溶液久置在空气中酸性会变强 D、将通入的溶液中可以得到 -
8、翡翠是由四种短周期主族元素组成的矿物,可表示为的简单离子的电子层结构相同,的原子半径比的大,的单质是常见的半导体材料,是地壳中含量最多的元素。下列说法不正确的是( )A、Y在化合物中显价 B、原子序数: C、W的简单氢化物稳定性比的强 D、的单质常温下均为气体
-
9、下列离子方程式书写正确的是( )A、金属钠与水的反应: B、将通入溶液中: C、向溶液中加入稀: D、用小苏打治疗胃酸过多:
-
10、文物是人类宝贵的历史文化遗产。下列描述不正确的是( )




A.西汉彩绘陶钟的主要成分是碳酸钙()
B.泥土属于混合物
C.酸雨对莲花纹石柱有严重的破坏作用
D.常温下铁在浓硫酸中会钝化
A、A B、B C、C D、D -
11、在指定条件下,下列物质或离子间的转化能实现的是( )A、胶体 B、 C、 D、
-
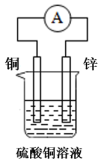
12、下列装置中能组成原电池的是( )A、
 B、
B、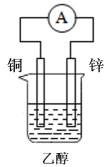 C、
C、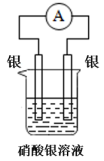 D、
D、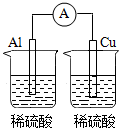
-
13、日常生活中的下列做法,与调控反应速率无关的是( )A、食品罐头抽真空包装 B、在铁制品表面镀铜 C、在奶粉中添加硫酸锌 D、将食物冷藏
-
14、实验室欲配制溶液 , 下列操作正确的是( )
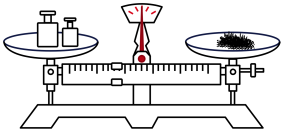
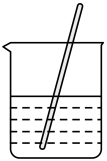
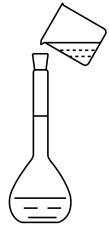

A.称取固体
B.溶解固体
C.向容量瓶内转移液体
D.用胶头滴管定容
A、A B、B C、C D、D -
15、下列物质的用途中,不涉及氧化还原反应的是( )A、用“84”消毒液杀菌消毒 B、用熟石灰改良酸性土壤 C、用铝和氧化铁的混合物焊接铁轨 D、用过氧化钠做呼吸面具的供氧剂
-
16、下列物质能使紫色石蕊试液先变红后褪色的是( )A、Cl2 B、敞口瓶中的久置氯水 C、盐酸 D、活性炭
-
17、“摇摇冰”是一种即用即冷的饮料,吸食时将饮料罐隔离层中的化学物质和水混合后摇动即能制冷,该化学物质可能是( )A、酒精 B、浓硫酸 C、固体 D、固体
-
18、聚醋酸乙烯酯(
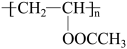 )广泛应用于黏合剂、涂料等领域,其一种合成路线如下(部分反应条件略去):
)广泛应用于黏合剂、涂料等领域,其一种合成路线如下(部分反应条件略去): 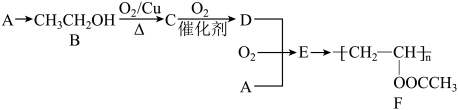
已知:烃A是石油裂解气的主要成分之一,相同状况下,烃A相对于H2的密度为14。
回答下列问题:
(1)、写出A的结构简式 , D中官能团的名称是。(2)、A→B的反应类型为。(3)、E→F的化学方程式为。(4)、符合下列条件的有机物共有种结构(不考虑立体异构)。①与B互为同系物
②相对分子质量比B大28
其中一种的结构简式为。
(5)、下列说法不正确的是(填标号)。a.F为纯净物
b.A、B都能使酸性KMnO4溶液褪色
c.可用大理石鉴别B、D两种物质的水溶液
d.向装有B的试管中投入一小粒钠,钠浮于液面上
-
19、Mg3N2是一种黄绿色粉末,能溶于酸,微溶于乙醇,易与水反应。某实验小组设计如下装置利用Mg和N2反应制备Mg3N2:
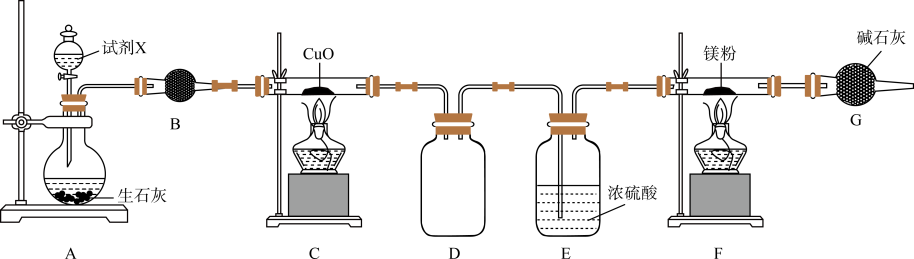
已知:NH3具有还原性,在加热时可将CuO还原成Cu。回答下列问题:
(1)、试剂X的化学名称为 , 装置B中所装试剂可选择(填标号)。a.五氧化二磷 b.无水氯化钙 c.碱石灰 d.活性炭
(2)、写出装置C中发生反应的化学方程式。(3)、实验开始时应先点燃处酒精灯(填“C”或“F"),目的是。(4)、装置G的作用是 , 其中盛装石灰的仪器的名称为。(5)、将制得的Mg3N2放入水中,产生刺激性气味的气体和一种白色沉淀,发生反应的化学方程式为。 -
20、从刻蚀印刷电路板的废液(主要成分为FeCl2、FeCl3、CuCl2)中回收铜并制备氯化铁晶体的一种工业流程如图:
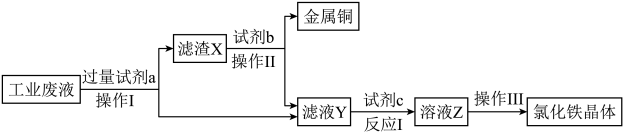
回答下列问题:
(1)、操作I的名称是 , 试剂a的化学式为。(2)、用FeCl3溶液刻蚀铜电路板的化学方程式为。(3)、试剂c可选用(填标号)。若选择上述试剂,反应I中氧化剂与还原剂的物质的量之比为。A.Zn B.H2O2 C.NaOH D.稀H2SO4
(4)、为检验氯化铁晶体中是否混有FeCl2 , 某同学设计方案为:取少许样品于试管中,滴加稀硝酸。若观察到产生气泡,试管口附近有色气体产生,则混有FeCl2.从环保角度考虑,该实验方案存在的不足之处是。(5)、取1.000g产物溶于水中,加入足量NaOH溶液,经过滤、洗涤、灼烧后,所得红棕色固体的质量为0.320g,则该产物中铁元素的质量分数为%。