相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、氮是粮食作物生长必需的元素,将空气中游离态的氮转化成氮的化合物的过程叫作氮的固定。最近科学家研究了一种在酸性介质中利用电解原理进行电化学固氮的方法,反应机理如图所示,氨气在催化剂电极表面产生。下列说法错误的是( )
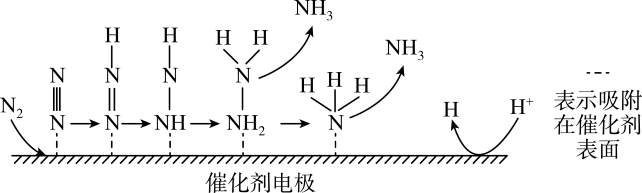 A、该过程中,氮气分子中N≡N键断裂产生N原子 B、电化学固氮法所得的氨气中可能含有少量的 C、催化剂能加快产生氨气的速率 D、该过程中有极性键的形成
A、该过程中,氮气分子中N≡N键断裂产生N原子 B、电化学固氮法所得的氨气中可能含有少量的 C、催化剂能加快产生氨气的速率 D、该过程中有极性键的形成 -
2、化学反应在硫酸工业中有重要应用。关于该反应的叙述正确的是( )A、无限延长化学反应的时间能改变化学反应的限度 B、、、的物质的量比1:2:2时达到平衡状态 C、该反应达到化学平衡状态时,正反应速率和逆反应速率相等且等于零 D、若开始加入和 , 达到化学平衡时核素存在于三种物质中
-
3、从铝土矿(主要成分为)中提取铝的工艺流程如图。下列说法错误的是( )
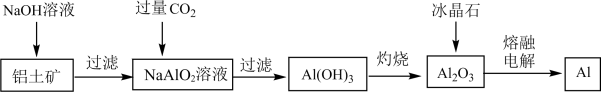 A、对于一些非常活泼的金属,工业上常用电解法冶炼 B、“熔融电解”时发生反应的化学方程式为 C、地壳中的铝元素含量丰富,大部分以游离态的形式存在 D、铝合金表面覆盖着致密的氧化铝薄膜导致其具有较强的耐腐蚀性能
A、对于一些非常活泼的金属,工业上常用电解法冶炼 B、“熔融电解”时发生反应的化学方程式为 C、地壳中的铝元素含量丰富,大部分以游离态的形式存在 D、铝合金表面覆盖着致密的氧化铝薄膜导致其具有较强的耐腐蚀性能 -
4、设表示阿伏加德罗常数的值,下列说法中正确的是( )A、0.1 mol苯中含有的碳碳双键数目为 B、16 g甲烷中含有的极性共价键数目为 C、11.2 L氧气中含有的氧原子数为 D、0.1 mol·L-1盐酸中含有的氢原子数为
-
5、化学反应的能量变化如图所示,下列说法正确的是( )
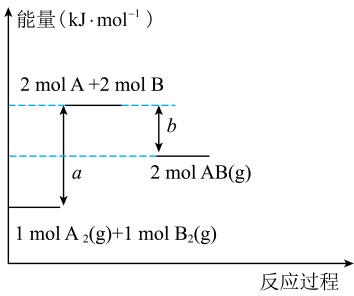 A、三种物质中的能量最高 B、该反应为放热反应 C、生成1 mol 需要吸收 kJ的能量 D、断开1 mol A-A键和1 mol B-B键时要放出a kJ能量
A、三种物质中的能量最高 B、该反应为放热反应 C、生成1 mol 需要吸收 kJ的能量 D、断开1 mol A-A键和1 mol B-B键时要放出a kJ能量 -
6、某有机物(M)的结构简式如图所示,下列有关M的说法正确的是( )
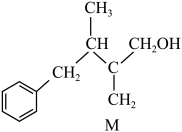 A、不能与金属钠发生反应 B、含有3种官能团 C、可自身发生加聚反应 D、分子式为
A、不能与金属钠发生反应 B、含有3种官能团 C、可自身发生加聚反应 D、分子式为 -
7、已知密闭容器中发生反应 , 在四种不同条件下测得的反应速率分别如下:① ② ③ ④。
则四种条件下反度速率快慢的比较正确的是( )
A、②=③>④>① B、④>②=③>① C、③>②=④>① D、②>①>③>④ -
8、劳动创造幸福,实干成就伟业,下列劳动项目所涉及的化学知识叙述正确的是( )
选项
劳动项目
化学知识
A
电池研发人员研发用于汽车的氢气燃料电池
电动汽车中的能量转化是将化学能直接转化为动能
B
营养师进行膳食指导:是否需要多补充
纤维素与蔗糖互为同分异构体
C
食品采用真空包装
减慢食品氧化速率
D
面包师用奶油给糕点裱花
奶油是高分子化合物
A、A B、B C、C D、D -
9、煤、石油、天然气是人类使用的主要能源,同时也是重要的化工原料。下列关于它们的综合利用的叙述错误的是( )A、以煤、石油和天然气为原料,可以合成高分子材料 B、煤的气化是工业上获得芳香烃的一种重要来源 C、石油的裂解和裂化都是化学变化 D、天然气是一种清洁燃料,属于不可再生资源
-
10、下列化学用语表示正确的是( )A、的空间填充模型:
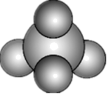 B、氯化铵的电子式:
B、氯化铵的电子式: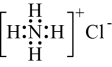 C、甲基的电子式:
C、甲基的电子式: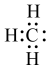 D、HClO的结构式:
D、HClO的结构式:
-
11、化学学科在材料、健康等领域发挥越来越重要的作用,下列说法中错误的是( )A、石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 B、利用氢氟酸刻蚀玻璃制作艺术品 C、高纯硅广泛应用于太阳能电池和计算机芯片 D、高温结构陶瓷具有耐高温、抗氧化等优良性能,可用于火箭发动机
-
12、文物见证了中华文明。下列文物中主要材料为有机物的是( )




A.元青花四爱图梅瓶
B.石家河玉人像
C.越王勾践剑
D.云梦睡虎地秦墓竹简
A、A B、B C、C D、D -
13、如图是中学化学中常见的有机物转化关系(部分相关物质和反应条件已略去)。已知A为一种植物激素,可催熟水果,回答下列问题:
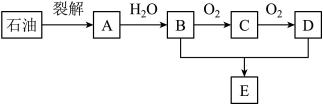 (1)、A的名称是 , A→B的反应类型为。(2)、C中官能团的名称为。(3)、写出B+D→E的化学方程式:。(4)、写出B→C的化学方程式:。(5)、符合下列条件的有机物共有种。
(1)、A的名称是 , A→B的反应类型为。(2)、C中官能团的名称为。(3)、写出B+D→E的化学方程式:。(4)、写出B→C的化学方程式:。(5)、符合下列条件的有机物共有种。①相对分子质量比D大28;②属于D的同系物。
-
14、“液态阳光”即“绿色甲醇”,是指生产过程中碳排放极低或为零时制得的甲醇。我国科学家李灿院士将这一设想变成了现实,在我国实现了工业化验证。一定温度下,在体积恒为2L的密闭容器中,充入2.0 mol CO2(g)和6.0 mol H2(g),发生“液态阳光”的反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g),测得CO2(g)的物质的量如下所示:
时间/min
0
2
4
6
8
n(CO2)/mol
2.0
1.5
1.2
1.0
1.0
(1)、2~4 min内,用CO2表示的化学反应速率v(CO2)=。(2)、0~2 min内与2~4 min内相比,0~2 min H2O(g)的生成速率更快,原因是。从表格数据看,min后,反应到达化学反应限度。(3)、反应达到平衡时,混合气体中H2(g)的体积分数为%。(4)、CH3OH可作燃料电池。某甲醇燃料电池以稀硫酸为电解质溶液,其正极发生反应的电极方程式为;电池工作时,每有1 mol CH3OH参加反应,转移电子的数目为(用NA表示阿伏加德罗常数)。 -
15、习近平总书记指出“要把粮食安全主动权牢牢握在手里”。氨气在农业生产中有广泛的应用。某实验小组设计如图所示装置,制备氨气并验证其性质,回答下列问题:
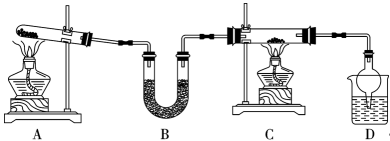 (1)、装置A是氨气发生装置,发生反应的化学方程式为。氨气的水溶液显(填“酸”或“碱”)性。(2)、装置B的名称是 , 下列盛放在B中的药品可以是(填序号)。
(1)、装置A是氨气发生装置,发生反应的化学方程式为。氨气的水溶液显(填“酸”或“碱”)性。(2)、装置B的名称是 , 下列盛放在B中的药品可以是(填序号)。a.P2O5 b.CaCl2 c.碱石灰 d.AlCl3
(3)、装置C中装有氧化铜,通入气体加热后出现光亮的红色固体同时产生的气体是空气的主要成分之一,该反应的方程式是 , 该反应体现氨气的(填“氧化”或“还原”)性。(4)、装置D中,球形管的作用是。利用如图装置完成NH3的喷泉实验,引发喷泉的操作是。
-
16、下表是元素周期表的一部分,①~⑧代表对应的元素,回答下列问题:
 (1)、①的一种核素的质量数为3,该核素的符号为。(2)、⑦在元素周期表中的位置是;⑧的原子结构示意图为。(3)、②③⑧的最高价氧化物对应水化物酸性最强的是(填化学式),②⑥的最高价氧化物对应水化物碱性更强的是(填化学式)。(4)、④⑤⑧的简单离子,半径最小的是(填离子),④和⑧的简单氢化物沸点更高的是(填化学式)。(5)、写出⑥的单质与⑤最高价氧化物对应水化物反应的离子方程式:。(6)、设计实验比较⑤和⑥的金属性强弱:。
(1)、①的一种核素的质量数为3,该核素的符号为。(2)、⑦在元素周期表中的位置是;⑧的原子结构示意图为。(3)、②③⑧的最高价氧化物对应水化物酸性最强的是(填化学式),②⑥的最高价氧化物对应水化物碱性更强的是(填化学式)。(4)、④⑤⑧的简单离子,半径最小的是(填离子),④和⑧的简单氢化物沸点更高的是(填化学式)。(5)、写出⑥的单质与⑤最高价氧化物对应水化物反应的离子方程式:。(6)、设计实验比较⑤和⑥的金属性强弱:。 -
17、如图表示中学化学中常见物质的转化关系(部分条件已略去)。其中A属于正盐,B、C、E是常见的气体,C能使湿润的红色石蕊试纸变蓝,D是一种淡黄色固体。
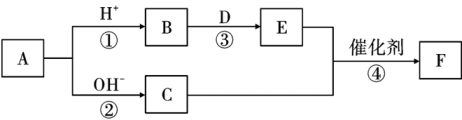
回答下列问题:
(1)、A物质的化学式是 , A中存在的化学键有。(2)、C的电子式是 , 在上述①~④反应中属于氧化还原反应的是(填编号)。(3)、写出B和D反应生成E的化学方程式,并用单线桥法表示电子的转移:。(4)、请写出反应④的化学方程式: , 写出该反应在工业上的用途:。 -
18、某温度下,在恒容密闭容器中发生可逆反应:I2(g)+H2(g)2HI(g)。下列情况中,一定能说明该反应已达到化学平衡状态的是( )A、单位时间内消耗1 mol H2 , 同时消耗2 mol HI B、混合气体的密度不再发生改变 C、H2和HI的物质的量浓度之比为1∶2 D、密闭容器中的压强保持不变
-
19、利用下列装置制备气体,药品、收集方式均正确的是( )
选项
气体
装置
固体药品
液体药品
收集方法
A
SO2
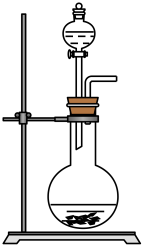
Cu
浓硫酸
排水
B
NH3
氢氧化钙固体
氯化铵固体
向下排空气
C
NO
铜
稀硝酸
向上排空气
D
O2
二氧化锰
双氧水
排水
A、A B、B C、C D、D -
20、ClO2是常见的水处理剂。实验室利用以下反应制备:2KClO3+H2C2O4+H2SO4=2ClO2+K2SO4+2CO2↑+2H2O,下列说法正确的是( )A、还原性:H2C2O4大于ClO2 B、KClO3 在反应中被氧化,失电子 C、ClO2净水利用了ClO2的还原性 D、反应中,每产生22.4 L气体,转移2 mol电子