相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列实验设计能达到实验目的的是( )
选项
实验目的
实验设计
A
除去FeCl2溶液中的FeCl3
向溶液中加入KMnO4溶液
B
鉴别碳酸钠和碳酸氢钠溶液
分别滴入氢氧化钙溶液,观察是否产生沉淀
C
鉴别碳酸钡和硫酸钡固体
取样,分别向样品上滴加稀盐酸,观察固体是否溶解
D
检验溶液中存在I-
滴加淀粉溶液,观察溶液是否变蓝
A、A B、B C、C D、D -
2、垃圾分类回收有利于废物的进一步处理和综合利用。为研究废旧电池的再利用,实验室利用废旧电池的铜帽(主要成分为Zn和Cu)回收Cu,并制备ZnO的部分实验过程如图所示。下列叙述不正确的是( )
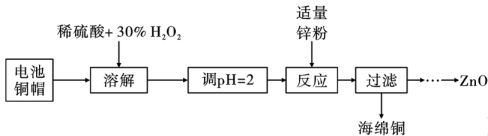 A、溶解操作可用空气替代30%H2O2 B、调节pH时可向溶液中加入Cu(OH)2 C、加入适量的锌粉目的是还原Cu2+ D、过滤后,滤液蒸发结晶、洗涤后,高温灼烧可得的ZnO
A、溶解操作可用空气替代30%H2O2 B、调节pH时可向溶液中加入Cu(OH)2 C、加入适量的锌粉目的是还原Cu2+ D、过滤后,滤液蒸发结晶、洗涤后,高温灼烧可得的ZnO -
3、2023年5月30日,我国神舟十六号宇航员顺利到达空间站。空间站中处理宇航员排泄物的一种方法是:用微生物处理产生氨气,氨气与氧气分别通入燃料电池两极,最终生成常见的无毒物质。示意图如图所示。下列说法正确的是( )
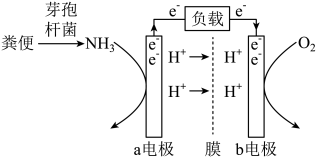 A、a电极是负极,发生还原反应 B、正极区发生的反应是O2+4e-+2H2O=4OH- C、电池工作时电子由a电极经电解质溶液流向b电极 D、每消耗标准状况下2.24L NH3转移电子数为0.3NA
A、a电极是负极,发生还原反应 B、正极区发生的反应是O2+4e-+2H2O=4OH- C、电池工作时电子由a电极经电解质溶液流向b电极 D、每消耗标准状况下2.24L NH3转移电子数为0.3NA -
4、工业上常用碳和水蒸气反应制水煤气。在密闭容器中加入一定量的C(s)和H2O(g),发生反应:C(s)+H2O(g)CO(g)+H2(g),下列说法错误的是( )A、用碳粉代替碳块,CO(g)的生成速率增加 B、保持容器体积不变,充入氦气,反应速率增加 C、保持容器体积不变,将CO(g)抽离出来,反应速率减慢 D、升高温度,反应的正、逆速率均增加
-
5、下列反应属于吸热反应的是( )A、碘化氢分解 B、二氧化碳和氧化钙化合 C、氢气在氧气中燃烧 D、铝条溶于盐酸
-
6、下列物质的转化关系(反应条件略去),一步反应不能实现的是( )A、Fe+Cl2→FeCl3 B、Na+O2→Na2O2 C、H2S+O2→SO3 D、NH3+O2→NO
-
7、下列说法正确的是( )A、分子式C3H6只能表示一种物质 B、CH4与少量Cl2混合光照产物中存在CCl4 C、乙醇和丙三醇互为同系物 D、C6H6与氯气反应生成C6H6Cl6属于取代反应
-
8、短周期主族元素X、Y、Z、W原子序数依次增大,X最高正价和最低负价的代数和为0,Y的简单氢化物常做制冷剂,Z被称为国防金属,W和Y同族。下列说法正确的是( )A、简单氢化物的还原性:W>Y B、最高价氧化物对应水化物的酸性:X>Y C、Z的氧化物可溶于氢氧化钠溶液 D、最简单氢化物的沸点:X>Y
-
9、配制0.1mol/L的NaOH溶液,如图所示装置和描述均正确的是( )
 A、用图①装置称量一定质量的NaOH固体 B、用图②溶解NaOH固体 C、转移洗涤后用图③装置定容 D、定容完成后摇匀如图④所示
A、用图①装置称量一定质量的NaOH固体 B、用图②溶解NaOH固体 C、转移洗涤后用图③装置定容 D、定容完成后摇匀如图④所示 -
10、下列说法不正确的是( )A、过度使用化肥,会造成水体富营养化,产生水华等污染 B、味精化学名称是谷氨酸钠,是化学制品,应禁止使用 C、豆腐的制备是利用盐卤等物质能使豆浆中的蛋白质聚沉 D、根据金属活泼性不同,可以采用加热分解、高温还原等不同的冶炼方法
-
11、能正确表示下列反应的离子方程式为( )A、过量SO2溶解在NaOH溶液中:SO2+2OH-=HSO+H2O B、NaHCO3和盐酸反应:HCO+H+=H2O+CO2↑ C、Fe2O3溶于氢碘酸:4Fe3++6HI=4Fe2++3I2+3H2O D、硫酸铜溶液中滴加氨水:Cu2++2OH-=Cu(OH)2↓
-
12、NA为阿伏加德罗常数的值,下列说法正确的是( )A、常温下,18 g D2O中含质子数为10NA B、标准状况下,22.4 L SO3中含有的分子数为NA C、标准状况下,22.4 L C2H6含有的共价键数目为7NA D、1 L 0.1 mol·L-1NaCl溶液中含有的NaCl分子数目为2NA
-
13、下列各组离子,在无色澄清溶液中能大量共存的是( )A、Fe2+、H+、ClO-、Cl- B、NH、Ca2+、Cl-、OH- C、K+、Ca2+、MnO、NO D、NH、Mg2+、Cl-、SO
-
14、巴豆酸的结构简式为CH3CH=CHCOOH,下列有关该物质的说法正确的是( )A、属于乙酸的同系物 B、所有原子均处于同一平面 C、可发生加成反应不能发生取代反应 D、能使溴水和酸性高锰酸钾溶液褪色
-
15、下列仪器和用途对应错误的是( )
选项
A
B
C
D
仪器
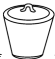

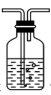
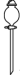
用途
蒸发溶液
过滤
除去气体中杂质
滴加溶液
A、A B、B C、C D、D -
16、下列化学用语表达正确的是( )A、O2与O3互为同系物 B、丙烷的球棍模型为
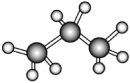 C、乙烯的结构简式是CH2CH2
D、用电子式表示氯化氢分子的形成过程:
C、乙烯的结构简式是CH2CH2
D、用电子式表示氯化氢分子的形成过程:
-
17、当光束通过下列物质时,会出现丁达尔效应的是( )A、云、雾 B、Fe(OH)3晶体 C、FeSO4溶液 D、饱和食盐水
-
18、化学与生产生活密切相关,下列说法正确的是( )A、在我国最早使用的合金是钢 B、石油的分馏属于化学变化 C、从海水中提取物质都要通过化学反应才能实现 D、高纯硅可用于制作光感电池
-
19、下列关于常见物质的分类正确的是( )A、汽油——化合物 B、纯碱——盐 C、硫酸氢钠——酸 D、碘酒——电解质
-
20、海水是巨大的资源宝库,利用海水为原料可获得许多化工产品。回答下列问题:(1)、从海水提取的粗盐中含有等杂质离子,精制时一般步骤如下:
加入的试剂1、2分别是、。
(2)、海水中溴元素主要以形式存在,工业上从海水中提取溴的流程如下:
①写出“氧化”过程中发生反应的离子方程式。
②将吹出后的含空气按一定速率通入吸收塔,用和水进行吸收,吸收后的空气进行循环利用。写出吸收过程中发生反应的离子方程式;吹出时的吹出率与吸收塔中流量的关系如图所示。流量过大,吹出率反而下降的原因是。
 (3)、工业上也可用溶液代替二氧化硫水溶液吸收最终转化为和则发生反应的化学方程式为;当有个电子发生转移时理论上吸收的质量为g。(4)、第一次“氧化”后已获得游离态的溴,“吹出”又将之转变成化合态的溴,其目的是。
(3)、工业上也可用溶液代替二氧化硫水溶液吸收最终转化为和则发生反应的化学方程式为;当有个电子发生转移时理论上吸收的质量为g。(4)、第一次“氧化”后已获得游离态的溴,“吹出”又将之转变成化合态的溴,其目的是。