相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、甲醇脱氢法制HCOOCH3工艺过程涉及如下反应:
反应Ⅰ:2CH3OH(g)=HCOOCH3(g)+2H2(g) ΔH1=+135.4 kJ·mol-1
反应Ⅱ:CH3OH(g)=CO(g)+2H2(g) ΔH2=+106.0 kJ·mol-1
向容积为10 L的恒容密闭容器中通入1.0 mol CH3OH气体发生上述反应,反应相同时间,测得CH3OH的转化率和HCOOCH3的选择性随温度变化如下图所示。

(已知:HCOOCH3的选择性=×100%)
下列说法正确的是( )
A、2CO(g)+2H2(g)=HCOOCH3(g)的ΔH=+76.6 kJ·mol-1 B、虚线代表的是CH3OH的转化率 C、553K时,HCOOCH3的产量为 0.1mol D、低于553K时,温度越高,生成的HCOOCH3越多。高于553K时,温度越高,生成的CO越多 -
2、一定温度下,把2.5 mol A和2.5 mol B混合盛入容积为2 L的密闭容器里,发生如下反应: , 经5 s反应达平衡,在此5 s内C的平均反应速率为 , 同时生成1 mol D,下列叙述中错误的是( )A、 B、反应达到平衡状态时A转化了1.5 mol C、若D的浓度不再变化,则该可逆反应达到化学平衡状态 D、反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为6:5
-
3、在2 L密闭容器中进行反应:mX(g)+nY(g)
 pZ(g)+qQ(g),2 s内X表示的平均反应速率为 mol/(L·s),则2 s内,物质Q增大的物质的量为( ) A、 mol B、 mol C、 mol D、mol
pZ(g)+qQ(g),2 s内X表示的平均反应速率为 mol/(L·s),则2 s内,物质Q增大的物质的量为( ) A、 mol B、 mol C、 mol D、mol -
4、下列关于化学反应速率的说法正确的是( )
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高,化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④3 mol•L﹣1•s﹣1的反应速率一定比1 mol•L﹣1•s﹣1的反应速率大
⑤升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数
⑥有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
⑦增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
⑧催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率
A、②⑤ B、②⑥⑧ C、②③⑤⑦⑧ D、①②④⑤⑧ -
5、下列说法正确的是( )A、已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol B、已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4 kJ/mol,则含0.5 mol NaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.7 kJ C、可燃物的系数为1的燃烧反应的焓变即为该可燃物的燃烧热 D、已知2C(s)+2O2(g)=2CO2(g) △H=a kJ/mol,2C(s)+O2(g)=2CO(g) △H=b kJ/mol,则a>b
-
6、有机物A的分子式为 , 可发生以下转化,已知B、D是生活中的两种常见的有机物,下列说法错误的是( )
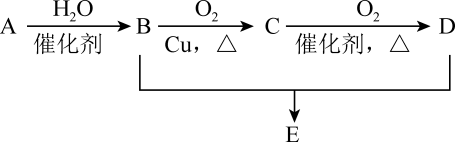 A、75%的B溶液常用于医疗消毒 B、上述流程中D、E都能与NaOH溶液反应 C、上述流程中B、D、E三种物质可以用饱和溶液鉴别 D、由B、D制备E常用浓硫酸作脱水剂
A、75%的B溶液常用于医疗消毒 B、上述流程中D、E都能与NaOH溶液反应 C、上述流程中B、D、E三种物质可以用饱和溶液鉴别 D、由B、D制备E常用浓硫酸作脱水剂 -
7、柠檬烯是一种食用香料,其结构简式如图所示。下列有关柠檬烯的分析正确的是( )
 A、它的分子中所有原子一定在同一平面上 B、1mol柠檬烯可以和3molH2发生加成反应 C、它和丁基苯(
A、它的分子中所有原子一定在同一平面上 B、1mol柠檬烯可以和3molH2发生加成反应 C、它和丁基苯( )互为同分异构体
D、一定条件下,它分别可以发生加成、取代、氧化、加聚等反应
)互为同分异构体
D、一定条件下,它分别可以发生加成、取代、氧化、加聚等反应
-
8、下列说法不正确的是( )A、甲烷分子空间填充模型是:
 B、乙烯分子的球棍模型为
B、乙烯分子的球棍模型为 C、甲烷和乙烯的混合物可通过溴的四氯化碳溶液分离
D、乙烯和环丙烷(
C、甲烷和乙烯的混合物可通过溴的四氯化碳溶液分离
D、乙烯和环丙烷( )不属于同系物
)不属于同系物
-
9、从海带中提取碘单质,可经以下实验流程完成。下列有关说法正确的是( )
 A、“氧化”过程中发生反应的离子方程式为 B、从碘水中萃取碘单质,可用酒精作萃取剂 C、以上流程在萃取、分液之后,还要经过反萃取、蒸馏等步骤才能获得碘单质 D、分液时,先打开活塞放出下层液体,再关闭活塞从上口倒出上层液体
A、“氧化”过程中发生反应的离子方程式为 B、从碘水中萃取碘单质,可用酒精作萃取剂 C、以上流程在萃取、分液之后,还要经过反萃取、蒸馏等步骤才能获得碘单质 D、分液时,先打开活塞放出下层液体,再关闭活塞从上口倒出上层液体 -
10、黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) △H=xkJ·mol-l
已知:①C(s)+O2(g)=CO2(g) △H=akJ·mol-l
②K2S(s)=S(s)+2K(s) △H=bkJ·mol-l
③2K(s)+N2(g)+3O2(g)=2KNO3(s) △H=ckJ·mol-l
下列说法正确的是( )
A、x>0 a<0 B、b<0 c<0 C、x=3a-b-c D、1mol 碳(s)在空气中不完全燃烧生成CO的焓变小于akJ·mol-1 -
11、已知乙醇、石墨和氢气的燃烧热分别为a、b、c(均为正值,单位均为kJ/mol)。则反应2C(石墨,s)+2H2(g)+H2O(l)=C2H5OH(l)的焓变为( )A、(2b+2c-a)kJ/mol B、(a-2b-2c)kJ/mol C、(b+c-a)kJ/mol D、(a-2b-c)kJ/mol
-
12、下列说法错误的是( )A、利用盖斯定律可计算某些难以直接测量的反应焓变 B、在指定状态下各物质的焓值都是确定且是唯一的 C、如果一个化学方程式通过其他几个化学方程式相加减而得到,那么该反应的焓变可由相关化学方程式的焓变相加减而得到 D、当同一个化学反应以不同的过程完成时,反应的焓变是不同的
-
13、空间探测器发射时常用肼(N2H4)作燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知:①N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol;②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ/mol。则N2H4(g)和NO2(g)反应的热化学方程式为( )A、2N2H4+2NO2=3N2+4H2O △H=-1135.7kJ/mol B、N2H4(g)+NO2(g)=N2(g)+2H2O(g) △H=-567.85kJ/mol C、2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H=+1135.7kJ/mol D、N2H4(l)+NO2(g)=N2(g)+2H2O(g) △H=-567.85kJ/mol
-
14、人体的营养物质包括糖类、油脂、蛋白质、维生素、无机盐和水,下列关于某些营养物质的说法不正确的是( )A、医用酒精能使鸡蛋清从其水溶液中析出而又不改变它的化学性质 B、油脂都可以看作是脂肪酸与甘油通过酯化反应形成的酯 C、糖类是绿色植物光合作用的产物,也是人类最重要的能量来源 D、人类体内没有水解纤维素的酶,无法吸收和利用纤维素,但食物中的纤维素有助于消化和排泄。
-
15、下列说法不正确的是( )A、非处方药不需要凭医生处方,消费者可自行购买和使用,其包装上有“OTC”标识 B、亚硝酸钠是一种防腐剂和护色剂,可用于一些肉制品如腊肉、香肠等的生产,但使用量和残留量都有规定 C、用反应:
 生产环氧乙烷,原子利用率和产率都是100%,符合绿色化学原子经济性要求
D、抗坏血酸(即维生素C)能氧化为脱氢抗坏血酸而发挥抗氧化作用,是水果罐头中常用的抗氧化剂
生产环氧乙烷,原子利用率和产率都是100%,符合绿色化学原子经济性要求
D、抗坏血酸(即维生素C)能氧化为脱氢抗坏血酸而发挥抗氧化作用,是水果罐头中常用的抗氧化剂
-
16、化学与生活密切相关。下列说法错误的是( )A、苯甲酸钠和山梨酸钾均可作食品防腐剂 B、维生素C和细铁粉均可作食品脱氧剂 C、双氧水和碘酒均可用于皮肤外用消毒 D、生石灰和五氧化二磷均可作食品干燥剂
-
17、A~H是常见有机物,、均为有香味的油状物质且互为同系物,E可用于催熟果实。
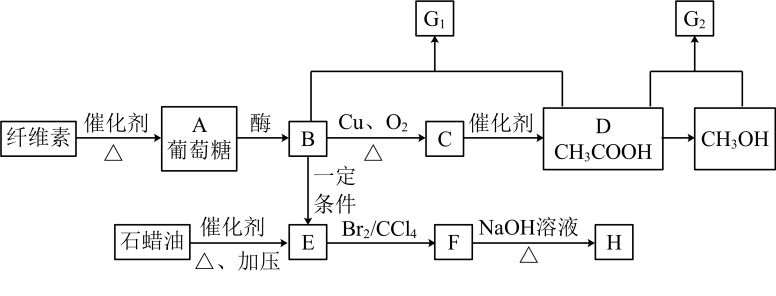
已知:(R代表烃基或H)
请回答下列问题:
(1)、纤维素的分子式是。(2)、A分子所含官能团的名称是 , 它与新制反应生成的砖红色固体是(填化学式),该反应在生活中的应用是。(3)、的同类别的同分异构体的结构简式是。(4)、有多种方法可合成G₁,请写出E与D在一定条件下通过加成反应合成的化学方程式:。(5)、H的分子式为 , 1 mol H与过量的Na反应放出1 mol , 写出1 mol H与2 mol D反应的化学方程式:。(6)、以有机物H为原料合成 的路线图(反应条件省略)如图:
的路线图(反应条件省略)如图:

则Y的结构简式是。
-
18、科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。
Ⅰ.活性炭纤维吸附法是工业提取碘单质的方法之一,其流程如图1所示:
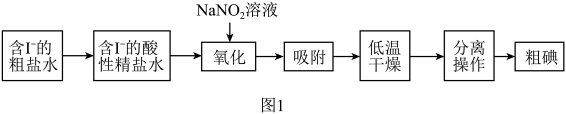
已知:a.溶液只能将氧化成 , 同时生成NO气体。
b.酸性条件下,会与反应生成和。
(1)、粗盐水中还含有、、 , 制成精盐水时所加试剂的顺序是____(填标号)。A、溶液、NaOH溶液、溶液、稀盐酸 B、NaOH溶液、溶液、溶液、稀盐酸 C、NaOH溶液、溶液、溶液、稀盐酸 D、溶液、溶液、NaOH溶液、稀盐酸(2)、“氧化”过程中发生反应的离子方程式是。(3)、酸性溶液是常用的氧化剂,但此过程中选择价格更贵的的原因是。(4)、根据碘单质的特性,分离操作是 , 冷凝得粗碘。(5)、Ⅱ.以金红石(主要成分为TiO₂)为原料制取海绵钛的工艺流程如图2所示:
高温条件下,反应1可生成一种可燃性气体,反应1的化学方程式是。
(6)、上述流程中可循环利用的物质是(填化学式),电解熔融的化学方程式是。(7)、反应2中钛的提取率在不同温度下随时间变化的曲线如图3,则反应最适宜的条件是。
-
19、某化学兴趣小组设计了如下实验装置验证浓硫酸的性质,并检验其与蔗糖反应的产物。
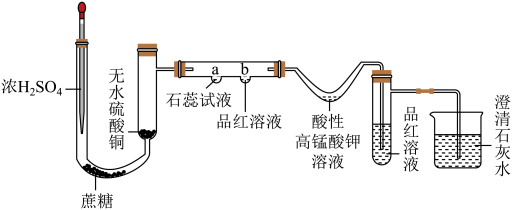
实验步骤:I.按如图所示组装好实验装置,( )。
II.在U形管内装入0.3g蔗糖 , U形管的内套管中加入无水硫酸铜,胶头滴管里盛放浓硫酸,直形玻璃管的凹槽a、b处分别加入2滴石蕊试液和品红溶液,V形管处加入适量酸性高锰酸钾溶液,具支小试管中加入1 mL品红溶液,小烧杯中加入澄清石灰水。
III.挤压胶头滴管,注入5滴浓硫酸于蔗糖中,微热U形管,开始反应时停止加热。
请根据所学知识回答问题:
(1)、步骤1的括号上应填入的内容是。(2)、微热时可以看到,蔗糖先变黄后变黑,然后膨胀并有气体产生。变黑体现了浓硫酸的性,蔗糖变黑过程中发生反应的化学方程式为。(3)、无水硫酸铜处出现的现象是。(4)、a处的现象是石蕊试液(填“褪色”或“由紫色变成红色”),可得到的结论是。(5)、酸性高锰酸钾溶液中发生反应的离子方程式为。(6)、能证明有生成的现象是。(7)、该实验设计的优点是(填一条)。 -
20、将一定量铁粉和铜粉混合均匀后分为四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成的体积和剩余金属的质量如表所示(设的还原产物只有):
实验序号
Ⅰ
Ⅱ
Ⅲ
Ⅳ
稀硝酸的体积/
50
100
150
175
剩余金属的质量/g
9.0
4.8
0
0
的体积(标准状况)/
1120
2240
3360
V
下列说法错误的是( )
A、 B、每等份混合物的质量为 C、稀硝酸的物质的量的浓度为 D、实验Ⅰ中发生反应的化学方程式为