相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、生命活动需要一系列的复杂的化学过程来维持,食物中的营养物质是这些过程的能量基础。下列关于糖类、油脂、蛋白质的说法正确的是( )A、糖类、油脂、蛋白质是人体必需的基本营养物质,在人体内都可以发生水解 B、向蔗糖溶液中加入稀硫酸并加热,再加入新制悬浊液,加热,未见砖红色沉淀,则蔗糖不发生水解 C、油脂在酸性条件下水解的反应叫皂化反应 D、农业上用波尔多液(由硫酸铜溶液和石灰乳制成)来防治植物病毒的原理是重金属阳离子和强碱能使蛋白质发生变性
-
2、下列实验操作能达到实验目的的是( )
选项
实验操作
实验目的
A
将海带灰溶于水,过滤,向滤液中滴加淀粉溶液
检测海带中含有碘元素
B
将SO2通入滴有酚酞的NaOH溶液中,溶液红色褪去
证明SO2的漂白性
C
向硅酸钠溶液中通入CO2气体,有白色沉淀产生
验证H2CO3的酸性强于H2SiO3
D
向市售乙醇中加入一小粒钠,有气泡产生
检测市售乙醇中存在水
A、A B、B C、C D、D -
3、部分含铁物质的分类与相应化合价关系如图所示。下列推断合理的是( )
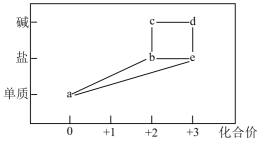 A、a可与e反应生成b B、b只有还原性,没有氧化性 C、可将溶液e加入浓碱液中制得d的胶体 D、不可能存在b→c→d→e→b的循环转化关系
A、a可与e反应生成b B、b只有还原性,没有氧化性 C、可将溶液e加入浓碱液中制得d的胶体 D、不可能存在b→c→d→e→b的循环转化关系 -
4、下列各组物质互为同分异构体的是( )A、16O2与18O2 B、CH4与CH3CH3 C、正丁烷与异丁烷 D、乙烷与乙烯
-
5、一定量的一氧化氮和足量碳在恒容密闭容器中发生反应: , 下列不能说明反应已达平衡状态的是( )A、NO的转化率不再发生变化 B、容器内压强不再发生变化 C、容器内混合气体的平均相对分子质量不再发生变化 D、容器内混合气体的密度不再发生变化
-
6、煤、石油和天然气的综合利用能够提高利用率,减少污染,获得多种化工产品。下列说法错误的是( )A、天然气的主要成分为CH4 B、通过石油裂化和裂解可获得乙烯、丙烯等重要的基本化工原料 C、煤的干馏和石油的分馏均属于化学变化 D、石油分馏后得到的汽油、煤油、柴油均是混合物
-
7、设为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,1 mol苯的体积为22.4 L B、1 mol S在足量氧气中燃烧生成SO3的数目为 C、1 mol铁和过量稀硝酸反应,转移的电子数目为 D、30 g乙烷中含有C—H键的数目为
-
8、乙醇和乙酸是人们生活和生产中常用的有机物。下列有关说法错误的是( )A、乙醇的催化氧化可以得到乙酸 B、1 mol乙醇可以和足量的金属钠反应产生0.5 mol H2 C、可用酸性高锰酸钾溶液鉴别乙醇和乙酸 D、可用饱和的碳酸钠溶液除去乙酸乙酯中的乙酸
-
9、“绿色化学”也称作环境友好化学,其核心思想就是改变“先污染后治理”的观念和做法。下列实验或叙述中不符合“绿色化学”理念的是( )A、用乙醇汽油代替普通汽油作汽车燃料 B、工业合成氨时,氨分离后剩余的气体再利用 C、制CuSO4时先将Cu氧化成CuO后再与稀硫酸反应 D、通过化学方法去治理排放到环境中的废气、废渣、废液
-
10、已知化学反应的能量变化如图所示,则有关说法错误的是( )
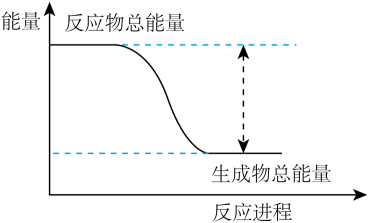 A、随着反应的进行,该反应向环境放出热量 B、A2的稳定性大于物质AB C、该反应中,化学键断裂吸收的总能量小于化学键形成放出的总能量 D、铝片与盐酸反应的能量变化趋势与图示相似
A、随着反应的进行,该反应向环境放出热量 B、A2的稳定性大于物质AB C、该反应中,化学键断裂吸收的总能量小于化学键形成放出的总能量 D、铝片与盐酸反应的能量变化趋势与图示相似 -
11、从微观角度认识物质是掌握物质性质的途径之一。下列有关说法不正确的是( )A、乙烷的分子式:C2H6 B、的结构示意图:
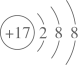 C、甲烷分子的空间填充模型:
C、甲烷分子的空间填充模型: D、氨气的电子式:
D、氨气的电子式:
-
12、化学与科技、生产、生活密切相关,下列说法错误的是( )A、卡塔尔AIJanoub体育场屋顶采用聚四氟乙烯板材,该板材属于有机高分子材料 B、大飞机C919用到了铝锂合金,铝锂合金属于金属材料 C、光导纤维在信息技术发展中应用广泛,制造光导纤维的主要材料是单质硅 D、葡萄酒中通常含有微量的SO2 , 既可以杀菌又可以防止营养成分被氧化
-
13、下列关于氮及其化合物的说法中不正确的是( )A、氮的固定过程中一定发生了氧化还原反应 B、氮氧化物大量排放到空气中会造成酸雨 C、NO和N2都可稳定存在于空气中 D、N2既可作氧化剂又可作还原剂
-
14、高分子F是一种皮革处理剂,一种合成F的流程如下:
 (1)、有机物C的名称是 有机物E中所含官能团名称(2)、A和C互为(填“同系物”或“同分异构体”,下同);C和
(1)、有机物C的名称是 有机物E中所含官能团名称(2)、A和C互为(填“同系物”或“同分异构体”,下同);C和 互为 (3)、有机物D的结构简式(4)、A和无机物X生成有机物B的反应类型(5)、写出E生成F的化学方程式:(6)、E可能具有下列性质的是。
互为 (3)、有机物D的结构简式(4)、A和无机物X生成有机物B的反应类型(5)、写出E生成F的化学方程式:(6)、E可能具有下列性质的是。a.能使溴水褪色
b.易溶于水
c.能在热烧碱溶液中发生水解反应
d.在常温下能与H2反应
-
15、CO是重要化工原料和清洁能源。(1)、I.CO(g)+NO2(g) ⇌ CO2(g)+NO(g)改变下列条件,反应速率增大的是____A、降温 B、缩小体积 C、加入催化剂 D、减压(2)、一定温度下,在2L恒容密闭容器中投入x mol CO(g)和x mol NO2(g),发生上述反应,经过t min达到平衡,CO的转化率为a。
①下列情况表明上述反应达到平衡状态的是
A.混合气体的密度保持不变 B.混合气体的摩尔质量保持不变
C.气体总压强保持不变 D.NO的消耗速率等于CO的消耗速率
②0-t min间CO的平均速率v(CO)=
(3)、Ⅱ.CO是一种清洁能源。CO空气碱性燃料电池能量转化率高,电池反应为2CO+O2+4KOH=2K2CO3+2H2O。在(填“正”或“负”)极区通入空气,写出负极反应式:。
(4)、Ⅲ.CO 是一种常用的化工原料。工业上利用CO和H2制备甲醇:
已知该反应为放热反应。下列图像符合上述反应中能量变化的是(填“甲”或“乙”)

-
16、治理氮氧化物(NOx)的污染是化学研究的重要课题之一。NO能被灼热的铁粉还原为N2 , 同时生成FeO,利用下列装置模拟该反应。

已知:①浓硝酸可将NO氧化为NO2;②NaOH溶液能与NO2反应,不与NO反应。
(1)、打开A装置分液漏斗活塞,烧瓶中观察到的实验现象有:铜片表面出现无色气泡,铜片逐渐变小、 、烧瓶中溶液由无色变为蓝色。(2)、A装置溶液由无色变为蓝色的离子方程式。(3)、上述装置接口的连接顺序为:a→→→→→g→h→b→c→d→(按气流方向,用小写字母表示)。(4)、①装置B的作用是 ②装置D的作用(5)、装置E中反应的化学方程式为 -
17、某兴趣小组用铬铁矿(FeCr2O4 , 含Al、Si氧化物等杂质)为主要原料制备K2Cr2O7晶体,流程如下:
 (1)、焙烧时向矿料中加入碳酸钠和氧气,发生如下反应FeCr2O4转化为Na2CrO4 , Na2CO3+SiO2Na2SiO3+CO2↑,Na2CO3+Al2O32NaAlO2+CO2↑
(1)、焙烧时向矿料中加入碳酸钠和氧气,发生如下反应FeCr2O4转化为Na2CrO4 , Na2CO3+SiO2Na2SiO3+CO2↑,Na2CO3+Al2O32NaAlO2+CO2↑写出FeCr2O4转化为Na2CrO4的化学方程式。
(2)、滤渣1的主要成分是。(3)、滤渣2的成分是和。(4)、流程中调pH:已知2CrO+2H+⇌Cr2O+H2O,蒸发结晶所产生的副产品是。(5)、结晶步骤Na2Cr2O7+2KCl= K2Cr2O7+2NaCl该反应是类型(四种基本反应类型)。(6)、该小组用m1 kg铬铁矿(FeCr2O4 50%)制备K2Cr2O7 , 最终得到m2 kg,产率为。 -
18、学生在实验室制取乙酸乙酯的装置如图:下列说法错误的是 ( )
 A、若用含示踪原子的乙醇和乙酸反应,则A中反应方程式:CH3COOH+C2H518OHCH3CO18 OC2H5+H2O B、长导管不伸入饱和碳酸钠液面以下目的是防倒吸 C、分离出乙酸乙酯层用的方法是分液 D、如果用4.6 g的C2H5OH和9.0 g的乙酸反应制得乙酸乙酯6.6 g,则本实验的产率是50%(产率指的是某种生成物的实际产量与理论产量的比值)
A、若用含示踪原子的乙醇和乙酸反应,则A中反应方程式:CH3COOH+C2H518OHCH3CO18 OC2H5+H2O B、长导管不伸入饱和碳酸钠液面以下目的是防倒吸 C、分离出乙酸乙酯层用的方法是分液 D、如果用4.6 g的C2H5OH和9.0 g的乙酸反应制得乙酸乙酯6.6 g,则本实验的产率是50%(产率指的是某种生成物的实际产量与理论产量的比值) -
19、海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是( )
 A、海水起电解质溶液作用 B、N极仅发生的电极反应: C、玻璃陶瓷具有传导离子和防水的功能 D、该锂-海水电池属于一次电池
A、海水起电解质溶液作用 B、N极仅发生的电极反应: C、玻璃陶瓷具有传导离子和防水的功能 D、该锂-海水电池属于一次电池 -
20、某有机物的结构简式如图所示,有关说法正确的是( )
 A、分子式为C11H11O3 B、1 mol该有机物最多能消耗2mol NaOH反应 C、既能使酸性高锰酸钾溶液褪色,又能使溴水褪色且褪色原理相同 D、能发生取代、加成、酯化、加聚等反应
A、分子式为C11H11O3 B、1 mol该有机物最多能消耗2mol NaOH反应 C、既能使酸性高锰酸钾溶液褪色,又能使溴水褪色且褪色原理相同 D、能发生取代、加成、酯化、加聚等反应