相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、据文献报道:催化某反应的一种反应机理如下图所示。下列叙述正确的是( )
 A、该反应有助于去除温室气体 B、该催化循环中Fe的成键数目未发生变化 C、的使用降低了总反应的焓变 D、参与了该催化循环
A、该反应有助于去除温室气体 B、该催化循环中Fe的成键数目未发生变化 C、的使用降低了总反应的焓变 D、参与了该催化循环 -
2、M(
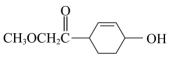 )和N(
)和N(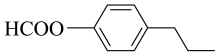 )均为合成药剂。下列说法正确的是( ) A、M中有3个手性碳原子 B、可用溶液鉴别M和N C、都能使酸性溶液褪色 D、1 mol N物质最多消耗1molNa
)均为合成药剂。下列说法正确的是( ) A、M中有3个手性碳原子 B、可用溶液鉴别M和N C、都能使酸性溶液褪色 D、1 mol N物质最多消耗1molNa -
3、活性ZnO是一种面向新世纪的新型高功能精细无机产品,某锌泥[主要含Zn、ZnO和]回收活性ZnO的工业流程如下:
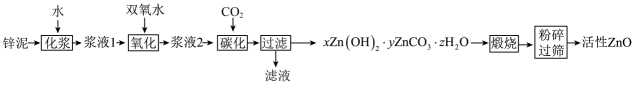
下列说法错误的是( )
A、“化浆”的目的是增大固液接触面积 B、温度越高,“氧化”步骤速率越快 C、增大压强可增大“碳化”过程中的吸收量 D、可通过所得活性ZnO质量和煅烧后产生的质量计算x -
4、下列图示或化学用语表达正确的是( )A、甲醛的电子式为
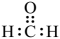 B、1,1-二氯乙烷的键线式:
B、1,1-二氯乙烷的键线式: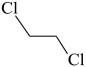 C、NaCl的晶胞:
C、NaCl的晶胞: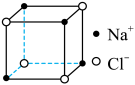 D、乙烯分子中π键的电子云图形:
D、乙烯分子中π键的电子云图形:
-
5、化学与科学、社会、历史密切相关,下列叙述错误的是( )A、敦煌壁画的颜料之一云母为聚硅酸盐,其阴离子以硅氧四面体为结构单元构成 B、用纳米技术催化合成可降解塑料聚碳酸酯,可实现“碳”的循环利用 C、纳米铁粉可以高效地吸咐去除污水中的、、等重金属离子 D、“垃圾分类”将易腐垃圾转化成热值较高的可燃性气体,属于生物质能热化学转换
-
6、安徽省历史文化悠久。下列四种安徽历史文化宝藏主要成分是由有机物构成的是( )
选项
A
B
C
D
文化宝藏




名称
徽派木雕
影青釉莲瓣纹注子注碗
铸客大鼎
金扣玛瑙碗
A、A B、B C、C D、D -
7、新型半导体材料如碳化硅(SiC)、氮化镓(GaN)等在国防技术、航空航天及5G技术等领域扮演着重要的角色。回答下列问题:(1)、基态Si原子中,核外电子占据的最高能层的符号为 , 占据最高能级的电子的电子云轮廓图形状为;基态Ga原子的核外电子排布为[Ar]3d104s24p1 , 其转化为下列激发态时,吸收能量最少的是(填选项字母)。
A.[Ar]
 B.[Ar]
B.[Ar]
C.[Ar]
 D.[Ar]
D.[Ar] (2)、C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结构分析,其原因为。(3)、硼(B)与Ga是同主族元素,硼氢化钠(NaBH4)是有机合成中重要的还原剂,其阴离子BH的立体构型为;另一种含硼阴离子的结构如图所示,其中B原子的杂化方式为。
(2)、C与Si是同主族元素,C原子之间可以形成双键、叁键,但Si原子之间难以形成双键、叁键。从原子结构分析,其原因为。(3)、硼(B)与Ga是同主族元素,硼氢化钠(NaBH4)是有机合成中重要的还原剂,其阴离子BH的立体构型为;另一种含硼阴离子的结构如图所示,其中B原子的杂化方式为。 (4)、GaCl3的熔点为77.9℃,GaF3的熔点为1000℃,试分析GaCl3熔点低于GaF3的原因为;气态GaCl3常以二聚体形式存在,二聚体中各原子均满足8e-结构,据此写出二聚体的结构式为。(5)、B和Mg形成的化合物刷新了金属化合物超导温度的最高记录。该化合物的晶体结构单元如图所示,其中Mg原子间形成正六棱柱,6个B原子分别位于六个三棱柱体心。则该化合物的化学式可表示为;相邻B原子与Mg原子间的最短距离为nm(用含x、y的代数式表示)。
(4)、GaCl3的熔点为77.9℃,GaF3的熔点为1000℃,试分析GaCl3熔点低于GaF3的原因为;气态GaCl3常以二聚体形式存在,二聚体中各原子均满足8e-结构,据此写出二聚体的结构式为。(5)、B和Mg形成的化合物刷新了金属化合物超导温度的最高记录。该化合物的晶体结构单元如图所示,其中Mg原子间形成正六棱柱,6个B原子分别位于六个三棱柱体心。则该化合物的化学式可表示为;相邻B原子与Mg原子间的最短距离为nm(用含x、y的代数式表示)。
-
8、高脂血能引起动脉粥样硬化、冠心病、胰腺炎等疾病,已成为现代人的健康杀手之一。下图是一种治疗高血脂的新药J的合成路线:

已知:
①

②

回答下列问题:
(1)、A是一种芳香烃,其名称为 , B→C的反应条件为 , C→D的反应类型为。(2)、J的结构简式是;(3)、写出G→H反应的化学方程式为;(4)、化合物W的相对分子质量比E大14,则符合下列条件的W的可能结构共有种(不含立体异构);①属于芳香族化合物;②遇FeCl3溶液显紫色;③能发生银镜反应
其中核磁共振氢谱有5组吸收峰,且峰面积比为2∶2∶2∶1∶1的结构简式为。
-
9、苯甲醇与苯甲酸是重要的化工原料,可通过苯甲醛在氢氧化钠水溶液中的歧化反应制得,反应的化学方程式为:

某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:

已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。苯甲酸微溶于水。
请根据以上信息,回答下列问题:
(1)、萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是 , 其理由是。萃取分液后,所得水层用盐酸酸化的目的是(用化学方程式表示)。(2)、苯甲酸在A、B、C三种溶剂中的溶解度(S)随温度变化的曲线如下图所示:
重结晶时,合适的溶剂是。洗涤时采用的合适洗涤剂是(填字母);
A.饱和食盐水 B.Na2CO3溶液 C.乙醇 D.蒸馏水
(3)、重结晶过程:热溶解→活性炭脱色→→ →抽滤→洗涤→干燥。重结晶过程中第一空的作用为。 -
10、按要求完成以下内容(1)、肉桂醛是重要的医药原料,也是重要的香料,其结构简式如图一所示,以肉桂醛为原料合成的肉桂醛二乙缩醛的结构如图二所示:

肉桂醛的的名称为(系统命名法),肉桂醛二乙缩醛的分子式为。
(2)、物质M结构如图, 具有的官能团除碳卤键外还有(填名称)。 (3)、丙三醇催化氧化的化学方程式为。(4)、制备酚醛树脂的化学方程式为。(5)、合成结构简式为
具有的官能团除碳卤键外还有(填名称)。 (3)、丙三醇催化氧化的化学方程式为。(4)、制备酚醛树脂的化学方程式为。(5)、合成结构简式为 的高分子材料的单体为。
的高分子材料的单体为。 -
11、化合物Z具有广谱抗菌活性,可利用X和Y反应获得。下列有关说法正确的是( )
 A、有机物X中含有一个手性碳原子 B、有机物Y可以和乙醇发生缩聚反应 C、有机物Y不存在顺反异构现象 D、1mol有机物Z与足量NaOH溶液反应最多消耗4 mol NaOH
A、有机物X中含有一个手性碳原子 B、有机物Y可以和乙醇发生缩聚反应 C、有机物Y不存在顺反异构现象 D、1mol有机物Z与足量NaOH溶液反应最多消耗4 mol NaOH -
12、乙酸苯乙酯可作为茉莉、白兰、月下香等香精的调和香料,它可以用乙醇、甲苯为原料进行人工合成,合成线路如下图所示。下列说法错误的是( )
 A、有机物A结构中一定有4个原子处于同一平面上 B、发生反应③时加入适量过量的有机物B,可提高的
A、有机物A结构中一定有4个原子处于同一平面上 B、发生反应③时加入适量过量的有机物B,可提高的 的产率
C、有机物C的芳香族化合物类同分异构体的数目为3种
D、合成线路中共涉及2种有机反应类型
的产率
C、有机物C的芳香族化合物类同分异构体的数目为3种
D、合成线路中共涉及2种有机反应类型
-
13、有关晶体的结构如下图所示,下列说法中正确的是( )
 A、在NaCl晶体中,阳离子的配位数为8,阴离子的配位数为6 B、该气态团簇分子的分子式为EF或FE,其晶体不导电 C、在金刚石晶体中,每个碳原子被6个六元环共同占有,每个六元环最多有4个碳原子共面 D、在CaF2晶体中,每个晶胞平均占有4个Ca2+ , F-的配位数是4
A、在NaCl晶体中,阳离子的配位数为8,阴离子的配位数为6 B、该气态团簇分子的分子式为EF或FE,其晶体不导电 C、在金刚石晶体中,每个碳原子被6个六元环共同占有,每个六元环最多有4个碳原子共面 D、在CaF2晶体中,每个晶胞平均占有4个Ca2+ , F-的配位数是4 -
14、聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如下:

下列说法不正确的是( )
A、形成聚维酮的单体是 B、1个聚维酮分子由(m+n)个单体加聚而成
C、聚维酮碘是一种水溶性高分子化合物
D、聚维酮、聚维酮碘在一定条件下均能发生水解反应
B、1个聚维酮分子由(m+n)个单体加聚而成
C、聚维酮碘是一种水溶性高分子化合物
D、聚维酮、聚维酮碘在一定条件下均能发生水解反应
-
15、下列实验操作、现象及结论均正确的是( )
选项
实验操作及实验现象
实验结论
A
向蔗糖溶液中滴加几滴稀H2SO4后,水浴加热,一段时间后再加入少量银氨溶液,继续水浴加热,未在试管内壁上形成银镜
蔗糖未发生水解反应
B
将油脂、乙醇和氢氧化钠溶液混合加热几分钟,用胶头滴管取少量混合物滴入蒸馏水中,液体表层无剩余油滴
油脂已完全水解
C
向溴乙烷中加入NaOH水溶液,水浴加热,一段时间后再加入AgNO3溶液,未生成淡黄色沉淀
溴乙烷未发生取代反应
D
向蛋白质溶液中加入浓HNO3 , 析出白色固体
蛋白质发生了盐析过程
A、A B、B C、C D、D -
16、己二酸是一种重要的化工原料,科学家在现有工业路线基础上,提出了一条“绿色”合成路线;

下列说法正确的是( )
A、环己烷分子的组成元素均位于元素周期表p区 B、工业路线中涉及苯的取代反应,该反应需使用苯、浓溴水混合加热制得溴苯 C、由于环己醇分子之间存在氢键,环己醇的沸点比甲基环己烷( )高
D、己二酸分子中所含σ键个数与π键个数之比为11∶2
)高
D、己二酸分子中所含σ键个数与π键个数之比为11∶2
-
17、亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,烧制青花瓷时可用于绘画。制备方法为:Fe+6HCN+2K2CO3=K4[Fe(CN)6]+H2↑+2CO2↑+2H2O。设NA为阿伏加德罗常数,下列说法正确的是( )A、27gHCN分子含有π键数目为NA B、[Fe(CN)6]4-中,金属离子价层电子排布式为3d6 C、反应过程中,每生成1molCO2 , 转移电子数目为4NA D、K2CO3中阴离子的空间构型为平面三角形,其中碳原子的价层电子对数目为4
-
18、下列各组中的反应,属于同一反应类型的是( )A、由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 B、乙酸乙酯的水解和乙烯制聚乙烯 C、由氯代环己烷消去制环己烯;由丙烯加溴制1,2-二溴丙烷 D、乙烯使酸性高锰酸钾溶液褪色和乙醛使溴水褪色
-
19、化学与科学、技术、社会、环境(STSE)密切联系。下列说法错误的是( )A、新冠病毒可用75%乙醇、次氯酸钠溶液、过氧乙酸进行消毒,其消毒原理相同 B、生产N95口罩的主要原料聚丙烯是一种高分子化合物 C、绿色化学要求从源头上消除或减少生产活动对环境的污染 D、聚乙烯是生产食品保鲜膜、塑料水杯等生活用品的主要材料,不能用聚氯乙烯替代
-
20、某实验小组同学用铜与浓硫酸反应制取SO2 , 验证SO2性质并制备NaHSO3 , 设计如图所示实验装置。
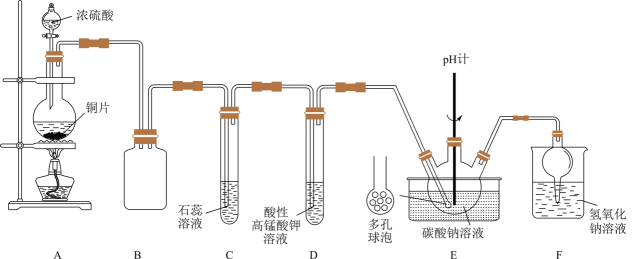
回答下列问题:
(1)、C中的实验现象是 , F的作用是。(2)、A中发生反应的化学方程式是。(3)、试管D中发生反应的离子方程式为。(4)、装置E中设计多孔球泡的目的是。(5)、向装置E中通入SO2可制得NaHSO3.已知:Na2SO3水溶液中H2SO3、HSO、SO随pH的分布如图1所示,Na2SO4的溶解度曲线如图2所示。
①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通入SO2的实验操作为。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,在高于℃条件下趁热过滤,用少量无水乙醇洗涤,干燥,密封包装。