相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列有关营养物质的说法正确的是( )A、蛋白质的水解产物都含有羧基和羟基 B、葡萄糖可用于发生银镜反应 C、天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点 D、蔗糖溶液中滴加3~5滴稀硫酸,煮沸冷却后加入银氨溶液,观察不到银镜产生,说明蔗糖没有水解
-
2、下列有机化学反应方程式及反应类型均正确的是( )
选项
化学方程式
反应类型
A
CH3COOH+CH3CH2OHCH3COOC2H5
取代反应
B
CH4+Cl2CH3Cl+HCl
置换反应
C
CH2=CH2+Cl2→CH3CHCl2
加成反应
D

取代反应
A、A B、B C、C D、D -
3、下列物质的生产流程不合理的是( )A、 B、 C、 D、
-
4、某温度下,浓度都是1 mol·L-1的两种气体X2和Y2 , 在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度分别为:c(X2)=0.4 mol·L-1 , c(X2)=0.8 mol·L-1 , c(Z)=0.4 mol·L-1 。则该反应的反应式可表示为:( )A、X2+2Y22XY2 B、2 X2+Y2 X2Y C、3 X2+Y2 2X3Y D、X2+3 Y22XY3
-
5、甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应(CH3)2C=O+HCN→(CH3)2C(OH)CN
(CH3)2C(OH)CN+CH3OH+H2SO4→CH2=C(CH3)COOCH3+NH4HSO4
新法合成的反应:CH3CCH+CO+CH3OH→CH2=C(CH3)COOCH3下列说法错误的是( )
A、HCN的电子式为 B、新法没有副产物产生,原子利用率高
C、与旧方法比,新方法对设备腐蚀性小
D、与旧方法比,新方法原料无爆炸危险
B、新法没有副产物产生,原子利用率高
C、与旧方法比,新方法对设备腐蚀性小
D、与旧方法比,新方法原料无爆炸危险
-
6、根据实验操作及现象,下列结论中正确的是( )
选项
实验操作及现象
结论
A
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象
稀硝酸的氧化性比浓硝酸强
B
将铜、银和AgNO3溶液组成原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝
Cu的金属性比Ag强
C
向溴水中加入苯,振荡后静置,水层颜色变浅
溴与苯发生了化学反应
D
取一定量Na2SO3样品,溶解后加入BaCl2溶液,产生白色沉淀。加入浓HNO3 , 仍有沉淀
此样品中含有SO
A、A B、B C、C D、D -
7、一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变化的是( )
A
硫化钠溶液出现浑浊
Na2S+2O2=Na2SO4
B
溴水颜色逐渐褪去
4Br2+4H2O=HBrO4+7HBr
C
Na置于空气中颜色变暗
2Na+O2=Na2O2
D
浓硝酸颜色为黄色
4HNO3=4NO2↑+O2 ↑+2H2O
A、A B、B C、C D、D -
8、设 NA为阿伏加德罗常数的值,下列说法正确的是( )A、0.5 mol正丁烷分子中共价键的数目为6.5 NA B、标准状况下,11.2L氯仿的物质的量为0.5mol C、1 mol羟基(-OH)与1 mol氢氧根(OH-)的电子数均为10 NA D、10 mL 18 mol/L 硫酸跟足量锌充分反应,转移的电子数为0.36NA
-
9、化学和生活密切相关。下列说法正确的是( )A、竹简的成分之一纤维素属于天然高分子 B、北京冬奥会的火炬“飞扬”使用的碳纤维属于有机高分子材料 C、维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化 D、苯甲酸钠可以作为食品防腐剂是由于其具有酸性
-
10、二十大报告指出“推动绿色发展,促进人与自然和谐共生”,强调要深入推进环境污染防治。其中碳和氮氧化物的综合处理是环境污染治理的重要内容,一种利用一氧化碳脱硝的方法涉及如下反应:
ⅰ. ;
ⅱ. ;
ⅲ. 。
回答下列问题:
(1)、一氧化碳与一氧化氮反应生成无污染气体的热化学方程式为。(2)、已知反应ⅲ的速率方程为(k为只受温度影响的速率常数)。向某2 L刚性密闭容器中充入0.1 mol 和0.1 mol , 控制一定温度下,只发生反应ⅲ,10 min末达到平衡,此时容器中NO的体积分数为40%。①10 min内该反应的平均反应速率;
②该温度下,反应ⅲ的平衡常数;
③若向平衡后的容器中充入一定量 , 此时会(填“增大”、“减小”或“不变”)。
(3)、某实验小组研究高温下和反应造成污染的程度。一定温度下,向某恒容密闭容器中按体积比4∶1投入和 , 发生反应ⅰ和反应ⅱ。①下列条件能说明上述两反应均达到平衡状态的是(填选项字母)。
a.的消耗速率等于的生成速率时
b.体积分数与体积分数相等时
c.混合气体颜色不再发生变化
d.混合气体密度不再发生变化
②当容器内压强减少5%时,的体积分数为(保留三位有效数字)。
(4)、我国科研工作者提出NO脱除可通过如图所示两种方式完成。实际生产中更适宜选择方式二的原因为。
-
11、吡咯(
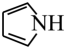 )是一种含氮五元杂环化合物,其衍生物广泛用作有机合成、医药、农药、香料、橡胶硫化促进剂、环氧树脂固化剂等的原料;用作色谱分析标准物质,也用于有机合成及制药工业。Zavy-alov吡咯(N)是其一种重要衍生物,合成路线如下:
)是一种含氮五元杂环化合物,其衍生物广泛用作有机合成、医药、农药、香料、橡胶硫化促进剂、环氧树脂固化剂等的原料;用作色谱分析标准物质,也用于有机合成及制药工业。Zavy-alov吡咯(N)是其一种重要衍生物,合成路线如下: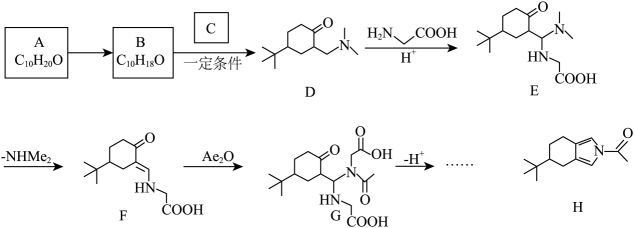
已知:ⅰ.Me-代表 , Ac-代表;
ⅱ.
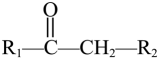
 。
。回答下列问题:
(1)、吡咯的化学式为;A的结构简式为 , A的核磁共振氢谱图中有个吸收峰。(2)、A→B需要的试剂和条件为;G中含氧官能团的名称包括酰胺基和。(3)、D→E和E→F的反应类型分别为 , 。(4)、写出B→D的化学方程式为。(5)、G有多种同分异构体,其中满足下列条件的结构简式为(写出一种即可)。a.遇溶液显紫色;
b.能与溶液反应生成;
c.核磁共振氢谱有4组峰;
d.苯环和
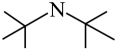 中的氮原子直接相连。
中的氮原子直接相连。 -
12、己二酸[]是重要的有机合成中间体,是重要的化工原料。实验室利用图1装置(夹持、加热装置省略)制备己二酸。
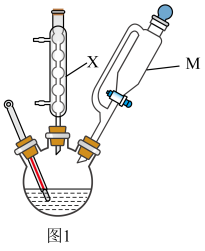
已知:己二酸的物理常数如下表所示。
色态
相对分子质量
熔点/℃
溶解性
己二酸
白色晶体
146
152
g/100 mL水
乙醇
15℃
25℃
100℃
易溶
1.4
2.3
160
Ⅰ.制备:向三颈烧瓶中,先加入一定量的浓 , 再通过仪器M向三颈烧瓶中缓缓加入环己醇,保持80℃持续反应2h。
Ⅱ.提纯:冷却后,抽滤、洗涤、干燥得己二酸粗品。
Ⅲ.测定粗品纯度:精确称取粗品0.0146 g于锥形瓶中,加入适量蒸馏水溶解,加入合适指示剂,用0.01 mol/L的NaOH标准液滴定至终点,重复上述操作三次,平均消耗NaOH标准液的体积为V mL。
实验原理:
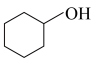 (未配平)。
(未配平)。回答下列问题:
(1)、与分液漏斗相比,仪器M的优点为;仪器X的作用为。(2)、制备时,如图1连接装置后需先进行的操作为;为避免制备过程中尾气污染空气,仪器X后需连接尾气处理装置,其中装置内盛放的试剂为(填化学式)溶液。(3)、洗涤时应选用(填选项字母)。a.热水 b.冰水 c.乙醇
(4)、第一次滴定开始和结束时,滴定管中的液面如图2,则消耗NaOH溶液的体积为mL。
重复上述操作三次,记录另两次数据如表中所示:
滴定次数
初读数/mL
末读数/mL
第二次
1.20
17.60
第三次
5.10
23.40
最终所得己二酸粗品的纯度为。
-
13、据报道纳米晶在生物医学领域有很大需求。我国科研团队以作保护气,油酸等为溶剂,用氧化镉(CdO)和硒、硫前驱体制得纳米晶CdS、CdSe。回答下列问题:(1)、Cd与Zn同族,均位于元素周期表中区;基态N原子电子排布式为。(2)、O、S、Se的最简单氢化物沸点由高到低的顺序为(填分子式)。(3)、比更易分解,由此可知键能N-HC-H(填“>”、“=”或“<”)。(4)、已知油酸结构简式为
 。油酸中各元素电负性由大到小的顺序为 , 其中碳原子的杂化方式为。 (5)、CdS、CdSe的立方晶胞结构相似(如下图,图示不表示原子相对大小)。
。油酸中各元素电负性由大到小的顺序为 , 其中碳原子的杂化方式为。 (5)、CdS、CdSe的立方晶胞结构相似(如下图,图示不表示原子相对大小)。
①CdSe晶胞中,Cd原子位于由Se原子构成的(填“正四面体”、“正六面体”或“正八面体”)空隙中,Se原子配位数为。
②CdS的晶胞参数为a pm,阿伏加德罗常数的值为 , 该晶胞的密度为(列出计算式即可)。
-
14、室温下,用0.100mol/L NaOH溶液滴定20.00 mL 溶液。滴定过程中含A微粒的分布分数()和pH随NaOH溶液体积变化如图所示。下列说法正确的是( )
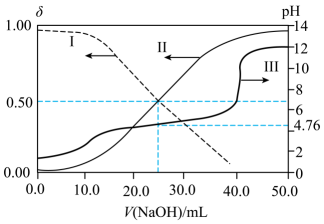 A、原溶液的物质的量浓度为0.125mol/L B、pH=7时, C、加入NaOH溶液越多,越高,水的电离程度越大 D、
A、原溶液的物质的量浓度为0.125mol/L B、pH=7时, C、加入NaOH溶液越多,越高,水的电离程度越大 D、 -
15、有机物M为肿瘤血管阻断剂,对正常血管影响小,可切断肿瘤血管供血,导致大面积肿瘤细胞死亡,具有较好的抗肿瘤活性,其分子结构如图所示。下列关于M的说法错误的是( )
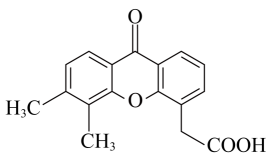 A、分子中碳原子有和两种杂化方式 B、该物质可发生还原反应和酯化反应 C、分子中所有碳原子一定共平面 D、该物质与苯甲酸互为同系物
A、分子中碳原子有和两种杂化方式 B、该物质可发生还原反应和酯化反应 C、分子中所有碳原子一定共平面 D、该物质与苯甲酸互为同系物 -
16、由实验操作和现象能得出相应结论的是( )
选项
实验操作
现象
结论
A
常温下,用pH计测定0.5mol/L溶液的pH
测得pH等于7
不影响水的电离程度
B
向碘水中加入后充分振荡
分层,下层为浅紫色
属于非极性分子,相似相溶,易溶于非极性分子
C
向淀粉溶液中加入稀硫酸,加热,一段时间后,冷却,加入NaOH溶液调至碱性,再加入新制 , 加热
出现砖红色沉淀
淀粉已完全水解
D
液溴和苯在铁粉作用下剧烈放热,将产生的气体直接通入硝酸银溶液中
出现浅黄色沉淀
苯和液溴发生了取代反应
A、A B、B C、C D、D -
17、设为阿伏加德罗常数的值。下列说法错误的是( )A、9 g重水()中含有的质子数为5 B、浓盐酸与氧化剂反应,每制备1 mol 转移电子的数目可能小于2 C、14 g环戊烷和环己烷的混合物中含有σ键的数目为3 D、200 mL 0.1mol/L的NaOH水溶液中含有氧原子数为0.02
-
18、T℃时,向体积为1 L的刚性密闭容器中充入发生反应: 。实验测得与时间变化关系如下表所示:
t/min
0
20
40
60
80
/
1.00
0.80
0.65
0.55
0.50
下列叙述错误的是( )
A、0~20 min内,用M表示的平均反应速率为0.01 B、60 min时,反应达到平衡状态 C、其他条件不变,升高温度,Q的平衡转化率增大 D、其他条件不变,加入催化剂后N的平衡产率不变 -
19、一种在锂电池工业中有重要用途的化合物的结构如图所示,其中短周期元素X、Y、Z、R、Q的原子序数依次增大,R、Q处于不同周期,基态Y原子核外有5种运动状态不同的电子。下列说法错误的是( )
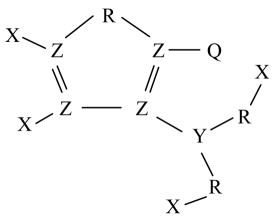 A、原子半径:X<Y<Z<R B、第一电离能:Y<Z<R C、该分子中Y与Z的杂化方式相同 D、最高价含氧酸的酸性:Y<Z<Q
A、原子半径:X<Y<Z<R B、第一电离能:Y<Z<R C、该分子中Y与Z的杂化方式相同 D、最高价含氧酸的酸性:Y<Z<Q -
20、用氢氧燃料电池为电源,以与辛胺为原料实现了甲酸盐和辛腈的高选择性合成,装置工作原理如图。下列说法错误的是( )
 A、气体X为氧气,气体Y为氢气 B、工作过程中燃料电池内溶液的pH保持不变 C、每消耗1 mol 会有4 mol 由M电极区移向N电极区 D、M电极上的电极反应式为
A、气体X为氧气,气体Y为氢气 B、工作过程中燃料电池内溶液的pH保持不变 C、每消耗1 mol 会有4 mol 由M电极区移向N电极区 D、M电极上的电极反应式为