相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列说法正确的是( )A、当生成2mol时放出92.4kJ热量,将0.5mol和足量在此条件下充分反应,放出热量46.2kJ B、反应放热,则白磷比红磷稳定 C、反应放热,则相同条件下,1mol和1mol断键吸收的总能量小于生成2mol成键释放的总能量 D、相同条件下,如果1mol氢原子所具有的能量为 , 1mol氢分子的能量为 , 则
-
2、由下列实验及现象推出的相应结论正确的是( )
实验
现象
结论
A
将样品溶于稀硫酸后,滴加溶液
溶液变红
晶体已氧化变质
B
向溶液X中滴加稀溶液,将湿润的红色石蕊试纸置于试管口
试纸不变蓝
溶液X中无
C
将气体依次通入溶液、品红溶液
品红溶液不褪色
的酸性比弱
D
用铂丝蘸取某溶液进行焰色试验
火焰呈黄色
该溶液中一定含有不含有
A、A B、B C、C D、D -
3、利用海水提取溴和镁的过程如下,下列说法不正确的是( )
 A、试剂可以选用石灰乳 B、工业上常利用电解溶液冶炼金属镁 C、若提取1mol , 至少需要标准状况下44.8L的 D、吸收塔中发生反应的离子方程式为
A、试剂可以选用石灰乳 B、工业上常利用电解溶液冶炼金属镁 C、若提取1mol , 至少需要标准状况下44.8L的 D、吸收塔中发生反应的离子方程式为 -
4、在一容积恒定的绝热密闭容器中,进行可逆反应: , 当下列物理量不变时,能表明该反应已达到该条件下的最大限度的是( )
①容器内气体的压强
②混合气体的密度
③混合气体的平均相对分子质量
④A的物质的量
⑤单位时间内生成2n mol C,同时生成n mol A
A、①②③④⑤ B、②③④⑤ C、①②③④ D、②④⑤ -
5、利用如图所示装置进行下列实验,能得到相应实验结论的是( )
选项
①
②
③
实验结论

A
硝酸
溶液
非金属性:
B
浓硫酸
蔗糖
溴水褪色
浓硫酸具有脱水性和强氧化性
C
硫酸
加有酚酞的溶液褪色
具有漂白性
D
浓盐酸
溶液变为黄色
氧化性:
A、A B、B C、C D、D -
6、王浆酸是从蜂王浆中分离出来的一种有机酸,有关王浆酸的说法不正确的是( )
 A、分子式为 B、能使溴的四氯化碳溶液褪色 C、一定条件下能发生取代反应和氧化反应 D、1mol王浆酸最多能中和2mol
A、分子式为 B、能使溴的四氯化碳溶液褪色 C、一定条件下能发生取代反应和氧化反应 D、1mol王浆酸最多能中和2mol -
7、如图为氟利昂()破坏臭氧层的反应过程示意图,下列说法不正确的是( )
 A、过程Ⅰ需要吸收能量 B、过程Ⅱ可用方程式表示为 C、过程Ⅲ可用方程式表示为 D、上述过程说明氟利昂中氯原子是破坏的催化剂
A、过程Ⅰ需要吸收能量 B、过程Ⅱ可用方程式表示为 C、过程Ⅲ可用方程式表示为 D、上述过程说明氟利昂中氯原子是破坏的催化剂 -
8、下列离子方程式正确的是( )A、次氯酸钠溶液吸收足量二氧化硫气体: B、向溶液中通入少量的: C、足量的铁与稀硝酸反应: D、“84消毒液”和“洁厕灵”(主要成分为盐酸)混合使用会产生有毒气体:
-
9、下列关于试剂的保存和仪器的使用错误的是( )A、氢氟酸应保存在塑料瓶中 B、溶液保存时要加入适量铁粉 C、用陶瓷坩埚加热熔融或 D、浓硝酸保存在棕色试剂瓶中
-
10、代表阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,2.24L含有的原子总数为 B、4.8g中含有的中子数为 C、0.1mol中含有的碳碳单键数为 D、含2mol的浓硫酸与足量铜加热反应,生成的分子数为
-
11、下列判断错误的是( )A、非金属性: B、还原性: C、酸性: D、碱性:
-
12、下列说法正确的是( )A、通过化学变化可以实现与之间的转化 B、的电子式为:
 C、某化合物熔融状态下能导电,该化合物中一定有离子键
D、与互为同素异形体
C、某化合物熔融状态下能导电,该化合物中一定有离子键
D、与互为同素异形体
-
13、化学与生活密切相关,下列说法错误的是( )A、医用消毒酒精中乙醇的体积分数为75% B、用灼烧的方法可以区分蚕丝和人造纤维 C、硫酸钡可用于胃肠X射线造影检查 D、燃煤中加入可以减少酸雨的形成和温室气体的排放
-
14、工业上常以高硫铝土矿(主要成分为Al2O3、Fe2O3 , 还含有少量FeS2等)为原料,生产Fe3O4(Fe3O4中1个Fe呈+2价,2个Fe呈+3价)和铝单质的工艺流程如图所示:
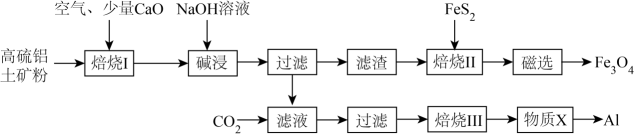
已知:①FeS2在“焙烧Ⅰ”过程中,发生反应的化学方程式为;②“焙烧Ⅱ”在隔绝空气的条件下发生反应的化学方程式为。
(1)、FeS2中硫的化合价为价;碱浸后滤渣的主要成分有(填化学式)。(2)、矿粉经过“焙烧Ⅰ”后,所得的大块烧渣需要进行“碱浸”,为了加快浸取的速率,可采取的措施有、(任写两点)。(3)、写出流程中过量CO2通入滤液中发生反应的离子方程式:。(4)、反应中产生的污染性气体SO2 , 可用下列哪种溶液吸收____(填字母)。A、浓硫酸 B、硝酸 C、NaOH溶液 D、氨水(5)、工业上,常用熔融的氧化铝为原料冶炼金属Al,发生反应的化学方程式为。生成的气体可以在流程的(填“焙烧Ⅰ”“焙烧Ⅱ”或“焙烧Ⅲ”)中循环使用。 -
15、某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。
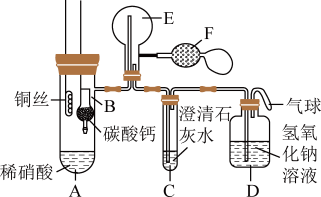
实验步骤与现象如下:
Ⅰ.将B装置下移,使碳酸钙与稀硝酸接触,产生气体;
Ⅱ.当C装置中产生白色沉淀时,立刻将B装置上提;
Ⅲ.将A装置中铜丝放入稀硝酸中,给A装置微微加热,A装置中产生无色气体,E装置中开始时出现浅红棕色气体;
Ⅳ.用F装置向E装置中鼓入空气,E装置中气体颜色逐渐加深;一段时间后,装置C中白色沉淀溶解。
回答下列问题:
(1)、写出操作Ⅰ中的化学方程式:。(2)、C装置中白色沉淀的化学式是。操作Ⅱ中当C装置中产生白色沉淀时立刻将B装置上提的原因是。(3)、写出操作Ⅲ中A装置中产生无色气体的化学方程式:。(4)、E装置内气体颜色逐渐加深的原因是。(5)、若该小组另取30 mL 的硝酸溶液与上述实验剩余的6.4 g铜丝在加热条件下反应,恰好完全反应,产生一定量NO和NO2的混合气体(反应过程中溶液体积变化忽略不计),则反应后的溶液中硝酸铜的物质的量浓度为(保留3位有效数字)。混合气体中NO的物质的量为mol。 -
16、乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。(1)、请写出实验室制取乙酸乙酯的化学方程式:。(2)、实验室制取乙酸乙酯的主要步骤如下:
Ⅰ.在甲试管(如图)中先加入3 mL乙醇,然后边振荡试管边慢慢加入2 mL浓硫酸和2 mL乙酸,再加入几片碎瓷片;
Ⅱ.按图连接好装置(装置气密性良好),小火均匀地加热3~5 min;
Ⅲ.待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。

①加入碎瓷片的目的是。
②与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是。
(3)、为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用如图所示装置进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后,充分振荡乙试管,再测有机层的厚度,实验记录如下:实验编号
甲试管中试剂
乙试管中试剂
有机层的厚度/cm
A
2 mL乙醇、1 mL乙酸、3 mL 浓硫酸
饱和Na2CO3溶液
3.0
B
2 mL乙醇、1 mL乙酸、3 mL H2O
0.1
C
2 mL乙醇、1 mL乙酸、3 mL H2SO4溶液
0.6
D
2 mL乙醇、1 mL乙酸、盐酸
0.6
①实验D的目的是与实验C相对照,证明对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是mL和。
②若加入的乙酸为120 g,乙醇为138 g,发生酯化反应得到132 g乙酸乙酯,试计算该反应的产品的产率为(产率)。
(4)、乙酸乙酯的某种同分异构体分子中含有2个甲基,且能与碳酸氢钠溶液反应,则该物质的结构简式为。 -
17、(1)、Ⅰ.在一定温度下,4 L恒容密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示。回答下列问题:
根据题中数据写出该反应的化学方程式: , 时刻,N的平均速率为。 (2)、、、三个时刻中,处于平衡状态的为(填“”“”或“”),后的某一时刻给体系升高温度,v(正)将(填“增大”或“减小”)。(3)、平衡后容器中气体的压强和反应前气体的压强之比是 , 平衡时N的转化率为。(4)、Ⅱ.某学习小组利用铁与稀硫酸的反应,探究影响化学反应速率的因素,结果如下表:
(2)、、、三个时刻中,处于平衡状态的为(填“”“”或“”),后的某一时刻给体系升高温度,v(正)将(填“增大”或“减小”)。(3)、平衡后容器中气体的压强和反应前气体的压强之比是 , 平衡时N的转化率为。(4)、Ⅱ.某学习小组利用铁与稀硫酸的反应,探究影响化学反应速率的因素,结果如下表:实验序号
铁的质量(g)
铁的形态
V(H2SO4)(mL)
c(H2SO4)()
反应前溶液的温度(℃)
金属完全消失的时间(s)
1
0.10
片状
50
0.8
20
200
2
0.10
粉状
50
0.8
20
25
3
0.10
片状
50
1.0
20
125
4
0.10
片状
50
1.0
35
50
实验1、2表明对反应速率有影响。
(5)、探究温度对反应速率的影响的实验是(填实验序号)。(6)、实验开始后,会出现速率加快,一段时间后速率减慢,分析其原因。 -
18、理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用反应“”设计了一个化学电池(如图所示)。该电池在外电路中,电流从a极流向b极。下列说法正确的是( )
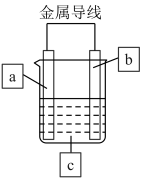 A、电极b的电极材料为铜,电极反应式为 B、电极a的电极材料可以为Ag,也可以是石墨或铁 C、c溶液为AgNO3溶液,放电时向b极移动 D、装置放电时主要将电能转化为化学能
A、电极b的电极材料为铜,电极反应式为 B、电极a的电极材料可以为Ag,也可以是石墨或铁 C、c溶液为AgNO3溶液,放电时向b极移动 D、装置放电时主要将电能转化为化学能 -
19、维生素A常作为保健药物,缓解视觉疲劳,维生素A的结构简式为
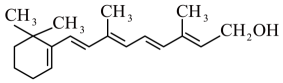 。下列有关维生素A的叙述正确的是( ) A、维生素A含有3种官能团 B、维生素A不能使溴的四氯化碳溶液褪色 C、1 mol维生素A最多可以和5 mol H2加成 D、维生素A不能和氧气发生催化氧化反应
。下列有关维生素A的叙述正确的是( ) A、维生素A含有3种官能团 B、维生素A不能使溴的四氯化碳溶液褪色 C、1 mol维生素A最多可以和5 mol H2加成 D、维生素A不能和氧气发生催化氧化反应 -
20、下列热化学方程式书写正确的是( )A、1 mol CH4(g)完全燃烧生成CO2(g)和H2O(l)时放出890 kJ的热量,其热化学方程式为 B、1 mol H2在氧气中完全燃烧放出热量为285.8 kJ,其热化学方程式为 C、2 mol NO2分解生成1 mol O2和2 mol NO,并吸收116.2 kJ热量,其热化学方程式为 D、1 mol CaCO3吸收178.2 kJ的热量完全分解,则该反应的热化学方程式为