相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
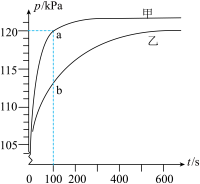
1、某课外实验小组在条件下,利用压强传感器等数字化实验设备,探究镁与不同浓度盐酸的反应速率,两组实验所用试剂和实验结果如下:
序号
镁条的质量/g
盐酸
实验结果
物质的量浓度/
体积/
1
0.01
1.0
2
2
0.01
0.5
2
下列说法错误的是( )
A、理论上两组实验最终生成相同物质的量的气体 B、曲线甲所示内的平均反应速率为 C、曲线乙b点的斜率可表征该反应在时的瞬时速率 D、曲线甲表示使用盐酸时的压强随时间的变化 -
2、化学烫发利用了头发中蛋白质发生化学反应实现对头发的“定型”,其变化过程示意图如下。下列说法不正确的是( )
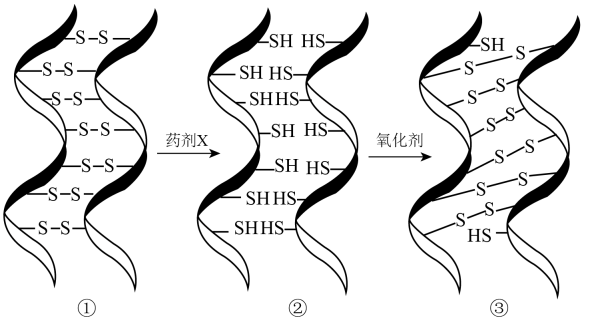 A、药剂X是还原剂 B、头发灼烧时会产生类似烧焦羽毛的特殊气味 C、①→②过程发生了化学键的断裂和形成 D、②→③过程若氧化剂是 , 其还原产物为
A、药剂X是还原剂 B、头发灼烧时会产生类似烧焦羽毛的特殊气味 C、①→②过程发生了化学键的断裂和形成 D、②→③过程若氧化剂是 , 其还原产物为 -
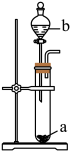
3、常温下利用下列装置进行实验,能得到相应结论的是( )
选项
试剂a、b
现象
结论
装置
A
漂白粉浓盐酸
导管口放置的湿润蓝色石蕊试纸先变红后褪色
漂白粉与浓盐酸反应生成
B
铜、稀硝酸
试管上部气体呈红棕色
铜与稀硝酸反应生成
C
钠、75%酒精溶液
收集的气体移近火焰,发出爆鸣声
钠与乙醇反应生成
D
铁、浓硫酸
无明显现象
铁与浓硫酸未发生反应
A、A B、B C、C D、D -
4、W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与其K层电子数相等,是形成酸雨的物质之一、下列说法正确的是( )A、Y与X可形成离子化合物 B、原子半径: C、Z的最高价氧化物的水化物是弱酸 D、简单氢化物的沸点:
-
5、为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,中电子的数目为 B、丙烷分子中共价键的数目为 C、溶液中的数目为 D、与足量反应转移的电子数目为
-
6、下列流程表示工业制硫酸的原理,有关叙述正确的是( )
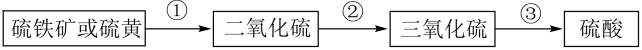 A、①②③都是氧化还原反应 B、硫铁矿主要成分的电子式为
A、①②③都是氧化还原反应 B、硫铁矿主要成分的电子式为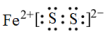 C、③用水做吸收剂
D、二氧化硫实际可产出三氧化硫
C、③用水做吸收剂
D、二氧化硫实际可产出三氧化硫
-
7、下列事实对应离子方程式书写正确的是( )A、工人用白醋除铁锈: B、技术员从海水提溴时用水溶液吸收含溴蒸气: C、药剂师用碳酸氢钠作抗胃酸药: D、环保人员用过量氨水除二氧化硫:
-
8、实验室将粗盐提纯并配制的溶液。本实验必须用到的仪器有( )
①天平 ②酒精灯 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦冷凝管
A、①②④⑥ B、①③⑤⑥ C、①②⑤⑥ D、②③④⑦ -
9、由和组成的混合气体在光照下反应生成四种氯代产物,其沸点如下表所示。利用如图实验装置对液态氯代产物进行分离,下列叙述错误的是( )
氯代产物
沸点/℃
39.8
61.2
76
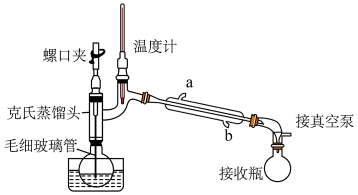 A.毛细玻璃管有平衡气压兼搅拌的作用B.可用热水浴加热,便于控制温度且受热均匀A、分离氯仿控制温度范围: B、冷凝管水流方向为b进a出
A.毛细玻璃管有平衡气压兼搅拌的作用B.可用热水浴加热,便于控制温度且受热均匀A、分离氯仿控制温度范围: B、冷凝管水流方向为b进a出 -
10、一种新型制备氨的方法如图所示。下列说法错误的是( )
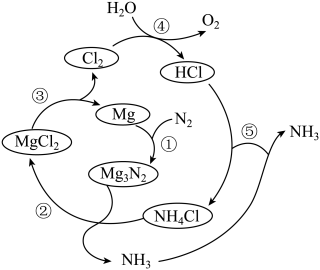 A、反应①属于氮的固定 B、反应③为 C、反应⑤两种气体相遇时,产生白烟 D、该制备总反应为
A、反应①属于氮的固定 B、反应③为 C、反应⑤两种气体相遇时,产生白烟 D、该制备总反应为 -
11、安全至关重要,下列实验室事故处理方法错误的是是( )A、活泼金属燃烧起火,用灭火毯(石棉布)灭火 B、电器起火,先切断电源,再用二氧化碳灭火器灭火 C、皮肤溅上碱液,先用大量水冲洗,再用2%的硼酸溶液冲洗 D、眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗
-
12、近年来,我国在科技领域取得了多项新突破和新发现。下列说法错误的是( )A、利用二氧化碳合成脂肪酸:实现无机小分子转变成有机高分子 B、发现月壤中的“嫦娥石”:其成分属于盐 C、发射太空光伏发电卫星“太阳花”:太阳能转化为电能 D、革新海水原位电解制氢工艺:关键材料聚四氟乙烯耐腐蚀
-
13、下列是某同学搭建的四种分子结构模型,合理的是( )
选项
A
B
C
D
分子
二氧化碳
甲烷
乙烯
乙酸
模型

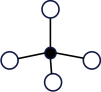
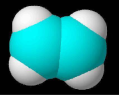
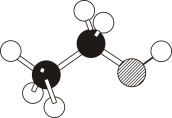 A、A B、B C、C D、D
A、A B、B C、C D、D -
14、化学与人类健康密切相关。下列物质不能用作食品添加剂的是( )A、氯化镁 B、三聚氰胺 C、山梨酸钾 D、二氧化硫
-
15、科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。请回答下列问题:(1)、活性炭吸附法是工业提取碘的方法之一,其流程如下:

已知:pH=2时,I.NaNO2溶液只能将I-氧化为I2 , 同时生成NO
II.
①氧化过程的离子方程式为。
②根据I2的特性,分离操作X应为、冷却结晶。
③酸性KMnO4是常用的强氧化剂,但该方法中却选择了价格较高的NaNO2 , 原因是。
(2)、以金红石(主要成分为TiO2)为原料,制取Ti的工艺流程如图所示:
①I在高温条件下进行,产物中有一种可燃性无色气体。I中反应的化学方程式为。
②II中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为℃。

③II中氩气的作用是。
④海绵钛除杂时得到的MgCl2可以循环使用,在上述工艺流程中可循环使用的物质还有(填化学式)。
-
16、在生活、生产中有重要用途,使用不当会造成环境污染。(1)、某同学利用如图所示装置研究二氧化硫的性质。

①向仪器a中滴加浓硫酸之前,需先通入一段时间 , 此操作的目的是。
②若溶液B为下列溶液,其中通入一定不会产生沉淀的是。
A.B.C.D.
③装置C中产生了浑浊,C中的反应消耗氧化剂与还原剂的物质的量之比为。
(2)、某化工厂用如图所示工艺流程除去燃煤产生的。
①写出在催化剂条件下总反应的化学方程式。
②过程Ⅱ发生反应的离子方程式为。
(3)、电化学法处理是目前研究的热点。利用过氧化氢吸收可消除污染,设计装置如图所示。
①石墨1电极处发生的电极反应式为。
②若11.2L(标准状况)参与反应,则电路中转移电子的物质的量为。
-
17、工业上可用水煤气合成二甲醚: , 恒容密闭容器中充入物质的量之比为1:2的和开始反应。(1)、测得和的浓度随时间变化如图所示,则反应开始至平衡时的平均反应速率。的转化率为。平衡时的容器的压强与起始时压强之比为。
 (2)、若该反应在恒温恒容密闭容器中进行,下列叙述中正确的是____。A、当混合气体的密度不变时说明反应达到最大限度 B、恒容时,充入增大压强,化学反应速率不变 C、容器内压强不再变化,说明该反应已达到最大的限度 D、当时说明该反应已达到平衡状态
(2)、若该反应在恒温恒容密闭容器中进行,下列叙述中正确的是____。A、当混合气体的密度不变时说明反应达到最大限度 B、恒容时,充入增大压强,化学反应速率不变 C、容器内压强不再变化,说明该反应已达到最大的限度 D、当时说明该反应已达到平衡状态 -
18、A的产量可以用来衡量一个国家石油化工发展水平,以A为主要原料合成一种具有果香味的物质E的生产流程如下:
 (1)、D的官能团名称:。(2)、写出反应②的化学方程式。(3)、步骤④的反应类型:。(4)、同学欲用如图装置制备物质E,请回答以下问题:
(1)、D的官能团名称:。(2)、写出反应②的化学方程式。(3)、步骤④的反应类型:。(4)、同学欲用如图装置制备物质E,请回答以下问题:
①试管A发生反应的化学方程式:。
②试管B中的试剂为饱和溶液,其作用除了降低乙酸乙酯的溶解度,便于分层之外,还有。
③试管A中加几块碎瓷片的目的是。
-
19、某污水处理厂利用微生物电池将镀铬废水中的催化还原,其工作原理如下图所示。下列说法错误的是( )
 A、电池工作过程中电子由a极经外电路流向b极 B、b极反应式: C、电池工作过程中a极区附近溶液的pH增大 D、每生成33.6L , 则处理1mol
A、电池工作过程中电子由a极经外电路流向b极 B、b极反应式: C、电池工作过程中a极区附近溶液的pH增大 D、每生成33.6L , 则处理1mol -
20、下列说法错误的是( )A、可用酸性溶液除去甲烷中的杂质乙烯 B、油脂和蛋白质都属于高分子化合物 C、植物油含不饱和脂肪酸,能使的溶液褪色 D、戊烷的一氯代物有8种同分异构体