相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、I.元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。回答下列问题:
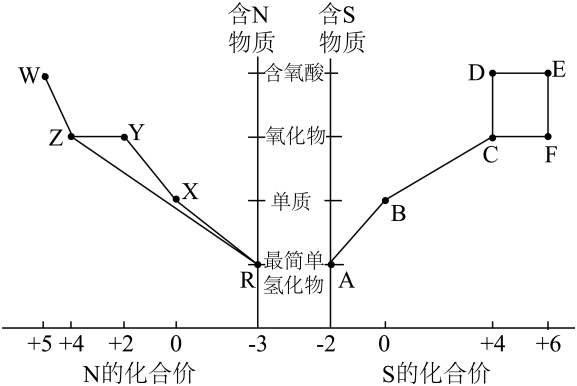 (1)、写出实验室利用两种固体物质加热制备物质R的化学方程式。(2)、下列有关图中所示含N、S物质的叙述,正确的是(填标号)。
(1)、写出实验室利用两种固体物质加热制备物质R的化学方程式。(2)、下列有关图中所示含N、S物质的叙述,正确的是(填标号)。a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
(3)、II.粗盐中含有泥沙及、、等杂质,其提纯过程一般经过以下流程:
某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、溶液、溶液等药品以及必备的实验仪器若干。请回答下列问题:
操作③按a、b、c顺序依次加入稍过量的试剂。若a为NaOH溶液,则c为溶液(写化学式)。
(4)、加盐酸调溶液pH的目的是。(5)、步骤⑥操作名称是。 -
2、为了测定乙醇的结构式,利用乙醇和钠的反应,设计如图1装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。
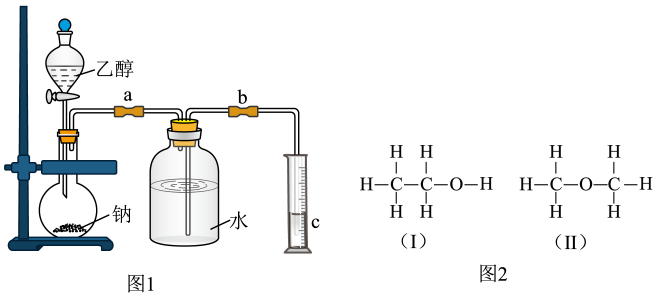 (1)、实验前检验该装置的气密性的实验操作是。(2)、有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为(填“正确”或“不正确”)。(3)、若实验中所用乙醇含有少量水则实验结果将(填“偏大”或“偏小”),若实验开始前b导管内未充满水则实验结果将(填“偏大”或“偏小”)。(4)、若测得有1.15gC2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确。
(1)、实验前检验该装置的气密性的实验操作是。(2)、有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为(填“正确”或“不正确”)。(3)、若实验中所用乙醇含有少量水则实验结果将(填“偏大”或“偏小”),若实验开始前b导管内未充满水则实验结果将(填“偏大”或“偏小”)。(4)、若测得有1.15gC2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确。 -
3、下图为元素周期表的一部分,请参照元素①~⑦在表中的位置,回答下列问题:
 (1)、元素⑥在周期表中的位置是。(2)、③④⑤的简单离子半径由大到小的顺序为(用离子符号和“>”表示)。(3)、④和⑦形成的化合物中含有化学键类型为。(4)、④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物发生反应的离子方程式为。
(1)、元素⑥在周期表中的位置是。(2)、③④⑤的简单离子半径由大到小的顺序为(用离子符号和“>”表示)。(3)、④和⑦形成的化合物中含有化学键类型为。(4)、④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物发生反应的离子方程式为。 -
4、下列有关苯和乙烯的说法中,不正确的是( )A、苯和乙烯都属于不饱和烃 B、苯和乙烯常温下都是气体 C、苯和乙烯分子中的所有原子都在同一个平面内 D、苯和乙烯都能燃烧
-
5、如图为一种氢氧燃料电池的装置示意图,下列说法不正确的是( )
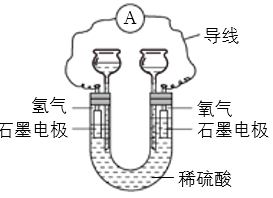 A、该装置中氧化反应和还原反应在不同区域进行 B、石墨是电极材料 C、O2是正极反应物、H2是负极反应物 D、H2SO4可以传导电子和离子
A、该装置中氧化反应和还原反应在不同区域进行 B、石墨是电极材料 C、O2是正极反应物、H2是负极反应物 D、H2SO4可以传导电子和离子 -
6、金合欢醇广泛应用于多种香型的香精中,其结构简式如图所示。下列说法不正确的是( )
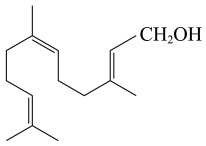 A、金合欢醇的同分异构体中不可能有芳香烃类 B、金合欢醇可发生加成反应、取代反应、氧化反应 C、金合欢醇分子的分子式为C15H26O D、1 mol金合欢醇与足量Na反应生成0.5 mol氢气, 与足量NaHCO3溶液反应生成1 mol CO2
A、金合欢醇的同分异构体中不可能有芳香烃类 B、金合欢醇可发生加成反应、取代反应、氧化反应 C、金合欢醇分子的分子式为C15H26O D、1 mol金合欢醇与足量Na反应生成0.5 mol氢气, 与足量NaHCO3溶液反应生成1 mol CO2 -
7、反应过程中的能量变化如图所示,(已知代表反应为放热反应,代表反应为吸热反应)则下列表述正确的是( )
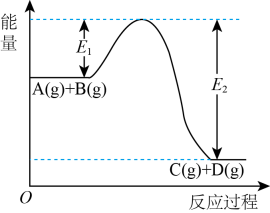 A、 B、 C、反应 , 是吸热反应 D、反应物键能高于生成物的键能
A、 B、 C、反应 , 是吸热反应 D、反应物键能高于生成物的键能 -
8、下列叙述正确的是( )A、同主族非金属元素的原子半径越小,其单质的沸点越高 B、同周期元素形成的简单离子,核电荷数越大半径越大 C、同周期主族元素的原子半径越大,其原子越易失去电子 D、同主族非金属元素的原子半径越大,其气态氢化物越稳定
-
9、下列有机反应属于取代反应的是( )A、 B、 C、 D、
-
10、下列说法不正确的是( )A、煤的气化、液化和干馏都是物理变化 B、向鸡蛋清的溶液中加入硫酸铜溶液,鸡蛋清凝聚,蛋白质变性 C、沥青来自于石油经减压蒸馏后的剩余物质 D、在催化剂作用下利用太阳能光解水可以制取氢气
-
11、下列化学用语正确的是( )A、乙烯的分子式: B、甲烷分子的空间填充模型为
 C、含有8个中子的氧原子:
D、次氯酸的结构式:H-Cl-O
C、含有8个中子的氧原子:
D、次氯酸的结构式:H-Cl-O
-
12、一学生用如图装置研究原电池原理,下列说法错误的是( )
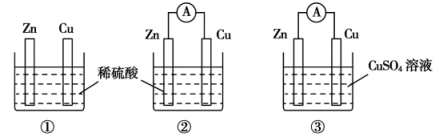 A、图③中Zn片增重质量与Cu棒减轻质量的比为65∶64 B、图②电子从Zn极经外电路转移到Cu极 C、图①中Cu棒上没有气体产生 D、图②与图③中正极产物的质量比为1∶32时,Zn棒减轻的质量相等
A、图③中Zn片增重质量与Cu棒减轻质量的比为65∶64 B、图②电子从Zn极经外电路转移到Cu极 C、图①中Cu棒上没有气体产生 D、图②与图③中正极产物的质量比为1∶32时,Zn棒减轻的质量相等 -
13、下列有关有机物的说法正确的是( )A、甲烷分子具有平面正方形结构 B、正丁烷和异丁烷互称为同系物 C、乙烯能使溴的四氯化碳溶液褪色 D、苯分子中含有碳碳双键,可以和溴水发生加成反应
-
14、下列各元素中,原子半径依次增大的是( )A、Na、Mg、Al B、N、O、F C、P、Si、Al D、C、Si、P
-
15、中国是个文明古国,有灿烂的文化和历史,为世界文化的进步和发展作出了贡献。文房四宝即笔、墨、纸、砚,其中以湖笔、徽墨、宣纸和端砚最为称著。下列说法正确的是( )A、徽墨中墨的主要成分是石墨 B、宣纸的主要成分是无机碳和少量的纤维素 C、湖笔中羊毫的主要成分是蛋白质 D、含较多氧化铁的端砚呈黑色
-
16、有机化合物A的产量可以用来衡量一个国家石油化工的发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图甲所示。已知E是一种高分子材料。
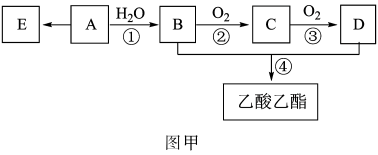 (1)、D的结构简式为。(2)、反应①的反应类型是 , B的官能团名称是。(3)、燃烧等质量的A和E,二者消耗氧气的物质的量(填“相等”或“不相等”)。(4)、在加热条件下,B转化成C的过程如图乙所示,下列说法正确的是____(填字母)。
(1)、D的结构简式为。(2)、反应①的反应类型是 , B的官能团名称是。(3)、燃烧等质量的A和E,二者消耗氧气的物质的量(填“相等”或“不相等”)。(4)、在加热条件下,B转化成C的过程如图乙所示,下列说法正确的是____(填字母)。 A、B和C具有相同的官能团 B、乙醇发生了氧化反应 C、氧化铜在反应中作催化剂 D、(1-丙醇)也能发生类似反应(5)、反应④的化学方程式为。制备乙酸乙酯的过程中,发现温度过高,乙酸乙酯的产率较低,可能的原因是(写出一个即可)。
A、B和C具有相同的官能团 B、乙醇发生了氧化反应 C、氧化铜在反应中作催化剂 D、(1-丙醇)也能发生类似反应(5)、反应④的化学方程式为。制备乙酸乙酯的过程中,发现温度过高,乙酸乙酯的产率较低,可能的原因是(写出一个即可)。 -
17、某工厂以黄铁矿(主要成分为)为原料,采用接触氧化法生产的流程如图甲所示。
 (1)、中S元素的化合价为。(2)、在“接触室”制备的反应化学方程式为。吸收时宜选用的试剂为(填“水”或“98.3%的浓硫酸”)。(3)、实验室常用浓硫酸来干燥某些气体,利用了浓硫酸的性。(4)、生产过程可用双碱法脱硫处理废气中的 , 原理如图乙所示,其中可循环使用的物质是 , 双碱法脱硫的总反应方程式为。
(1)、中S元素的化合价为。(2)、在“接触室”制备的反应化学方程式为。吸收时宜选用的试剂为(填“水”或“98.3%的浓硫酸”)。(3)、实验室常用浓硫酸来干燥某些气体,利用了浓硫酸的性。(4)、生产过程可用双碱法脱硫处理废气中的 , 原理如图乙所示,其中可循环使用的物质是 , 双碱法脱硫的总反应方程式为。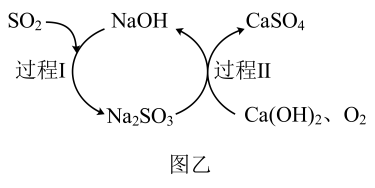 (5)、为测定空气中的含量,甲同学将空气样品经过管道通入密闭容器中的的酸性溶液。已知与该溶液反应的离子方程式为:。若管道中空气流量为aL/min,经过b分钟溶液恰好褪色,则该空气样品中的含量为g/L。
(5)、为测定空气中的含量,甲同学将空气样品经过管道通入密闭容器中的的酸性溶液。已知与该溶液反应的离子方程式为:。若管道中空气流量为aL/min,经过b分钟溶液恰好褪色,则该空气样品中的含量为g/L。 -
18、某学习小组设计实验验证能与反应,实验装置如图。
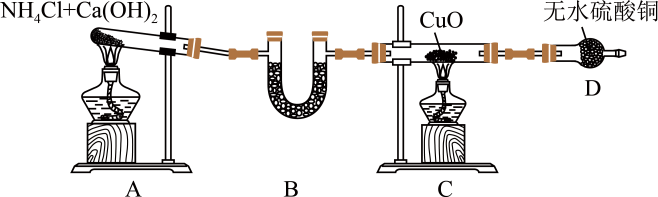 (1)、装置D的仪器名称是。(2)、装置A试管中发生反应的化学方程式为。(3)、装置B的作用是干燥 , 可选择的试剂是____(填字母)。A、浓硫酸 B、碱石灰 C、固体 D、无水固体(4)、实验中装置C的试管中有红色单质生成,还能收集到一种气体单质,且D装置中无水硫酸铜变蓝。则该反应说明具有(填“氧化性”或“还原性”),氧化剂和还原剂的物质的量之比为。(5)、已知难溶于。下列能用来吸收该实验尾气的装置是____(填字母)。A、
(1)、装置D的仪器名称是。(2)、装置A试管中发生反应的化学方程式为。(3)、装置B的作用是干燥 , 可选择的试剂是____(填字母)。A、浓硫酸 B、碱石灰 C、固体 D、无水固体(4)、实验中装置C的试管中有红色单质生成,还能收集到一种气体单质,且D装置中无水硫酸铜变蓝。则该反应说明具有(填“氧化性”或“还原性”),氧化剂和还原剂的物质的量之比为。(5)、已知难溶于。下列能用来吸收该实验尾气的装置是____(填字母)。A、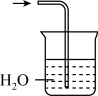 B、
B、 C、
C、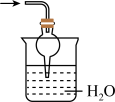 (6)、与的反应受的用量和反应温度影响,有时会生成副产物(砖红色固体),易对实验结论产生干扰。已知在酸性溶液中不稳定:。请设计实验方案验证完全反应后的红色固体产物中是否含有:。
(6)、与的反应受的用量和反应温度影响,有时会生成副产物(砖红色固体),易对实验结论产生干扰。已知在酸性溶液中不稳定:。请设计实验方案验证完全反应后的红色固体产物中是否含有:。 -
19、氢气是非常重要的化学能源,利用氢气可以实现化学能向热能、电能的直接转化。(1)、已知断开、、需要的能量依次是、、 , 则在中完全燃烧生成放出的热量为kJ。能正确表示反应中能量变化的是图(填“甲”或“乙”)。
 (2)、和组合形成的质子交换膜燃料电池的结构如下图:
(2)、和组合形成的质子交换膜燃料电池的结构如下图:
①电极d是(填“正极”或“负极”),电极c的电极反应式为。
②若电路中转移电子,则该燃料电池理论上消耗的在标准状况下的体积为L。
(3)、某温度下,向容积固定的密闭容器中充入和 , 在催化剂作用下发生反应。已知反应进行到时,的物质的量不再发生变化,此时测得的物质的量为。①反应进行到时,用浓度变化表示的平均反应速率为 , 此时的物质的量为。
②不能判断该反应达到平衡状态的是(填字母)。
A. B.容器内气体压强不再变化
C.容器内气体密度不再变化 D.和的物质的量浓度之比为
-
20、X、Y、Z、Q、W为原子序数依次增大的短周期主族元素,其中Z是地壳中含量最多的元素,Z与Q同主族,化合物与XW相遇会产生白烟。下列叙述正确的是( )A、非金属性:W>Q>Z>X B、元素Q的含氧酸均为强酸 C、Y与Z形成的化合物均能与水反应 D、X、Z、W组成的化合物可能具有漂白性