相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、是钙钛矿型太阳能电池的重要吸光材料,其晶胞结构如图所示。已知:B代表 , A的原子分数坐标为(0,0,0),摩尔质量为M g/mol,晶胞边长为a pm,为阿佛伽德罗常数的值。下列说法正确的是( )
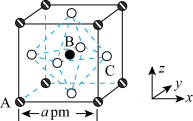 A、该晶体为共价晶体 B、的配位数为8 C、C的原子分数坐标为( , 1,) D、该晶体的密度为
A、该晶体为共价晶体 B、的配位数为8 C、C的原子分数坐标为( , 1,) D、该晶体的密度为 -
2、有一种由简单单体聚合而成的高分子,结构片段如图所示,下列有关说法正确的是( )
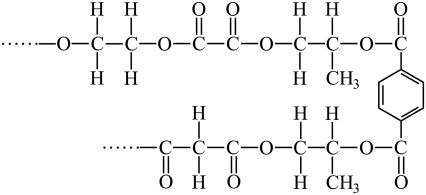 A、该高分子由4种单体缩聚而成 B、该高分子的几种羧酸单体互为同系物 C、该高分子的单体之一为乙二醇,乙二醇可被连续催化氧化生成单体之一的草酸 D、该高分子有固定熔、沸点,1 mol上述结构片段在NaOH溶液中完全水解,最多消耗5 mol NaOH
A、该高分子由4种单体缩聚而成 B、该高分子的几种羧酸单体互为同系物 C、该高分子的单体之一为乙二醇,乙二醇可被连续催化氧化生成单体之一的草酸 D、该高分子有固定熔、沸点,1 mol上述结构片段在NaOH溶液中完全水解,最多消耗5 mol NaOH -
3、下图是活性炭中的含氧基团催化双氧水氧化苯制苯酚的反应历程,下列说法正确的是( )
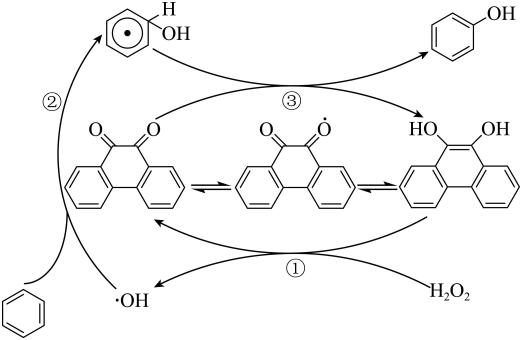 A、有7个 B、反应②中没有元素化合价变化 C、
A、有7个 B、反应②中没有元素化合价变化 C、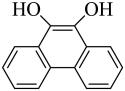 在反应过程中起催化作用
D、已知中的氧氧键比中的氧氧键的键长短,则氧化苯比容易
在反应过程中起催化作用
D、已知中的氧氧键比中的氧氧键的键长短,则氧化苯比容易
-
4、利用如图所示的有机物X可生产Y。下列说法正确的是( )
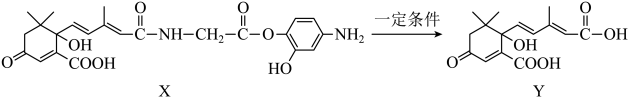 A、Y可以发生加聚反应、缩聚反应、取代反应、银镜反应 B、X既能与酸反应生成盐和水又能与碱反应生成盐和水 C、Y既可以与溶液发生显色反应,又可使酸性溶液褪色 D、1 mol X分别与足量的氢氧化钠溶液、氢气反应,消耗二者的物质的量之比为5∶7
A、Y可以发生加聚反应、缩聚反应、取代反应、银镜反应 B、X既能与酸反应生成盐和水又能与碱反应生成盐和水 C、Y既可以与溶液发生显色反应,又可使酸性溶液褪色 D、1 mol X分别与足量的氢氧化钠溶液、氢气反应,消耗二者的物质的量之比为5∶7 -
5、下列关于分子式为C4H8O2的有机物的同分异构体的说法中,不正确的是( )A、属于酯类的有4种 B、属于羧酸类的有2种 C、存在分子中含有六元环的同分异构体 D、既含有羟基又含有醛基的有3种
-
6、下列实验操作能达到相应实验目的是( )
实验目的
实验操作
A
检验淀粉已经完全水解
取少量水解液加适量氢氧化钠溶液使其呈碱性,加入银氨溶液混合加热,观察是否有有光亮的银镜生成
B
证明Y中是否含有醛基
向1 mL 1%的NaOH溶液中加入2 mL 2%的溶液,振荡后再加入0.5 mL有机物Y,加热,观察是否出现砖红色沉淀
C
除去苯中混有的少量苯酚
加入NaOH溶液,振荡,静置分层后,用分液漏斗可分离出苯
D
检验RX是溴代烷
将RX与NaOH水溶液共热,经充分反应后冷却,向冷却液中加溶液,观察沉淀颜色
A、A B、B C、C D、D -
7、药物“达芦那韦”可用于治疗HIV感染,合成“达芦那韦”的部分路线如图所示,下列说法不正确的是( )
 A、A分子中所有原子可能在同一平面 B、B的同分异构体有7种(含B且不考虑立体异构) C、C
A、A分子中所有原子可能在同一平面 B、B的同分异构体有7种(含B且不考虑立体异构) C、C 分子式为
D、反应②为还原反应
分子式为
D、反应②为还原反应
-
8、国家一类抗癌新药乙烷硒啉(Ethaselen)进入临床研究,其结构如图。下列说法正确的是( )
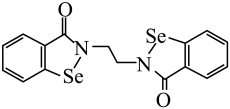 A、基态Se原子的价层电子排布式为 B、分子所含元素中第一电离能最大的为O C、分子中的碳原子都采取杂化 D、分子中有8种不同化学环境的碳原子
A、基态Se原子的价层电子排布式为 B、分子所含元素中第一电离能最大的为O C、分子中的碳原子都采取杂化 D、分子中有8种不同化学环境的碳原子 -
9、Tf2O在医药领域有广泛的应用前景,其结构如图所示,其中W、X、Y、Z为原子半径依次增大的短周期非金属元素,W位于元素周期表的p区。下列说法不正确的是( )
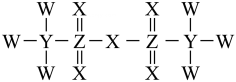 A、沸点: B、基态原子未成对电子数: C、中元素的化合价为价 D、Y形成的氢化物可能既含极性键,又含非极性键
A、沸点: B、基态原子未成对电子数: C、中元素的化合价为价 D、Y形成的氢化物可能既含极性键,又含非极性键 -
10、下列实验装置能达到相应实验目的的是( )
 A、图1证明乙炔可使溴水褪色 B、图2制备硝基苯 C、图3证明溴乙烷与NaOH醇溶液共热生成了乙烯 D、图4制备乙烯
A、图1证明乙炔可使溴水褪色 B、图2制备硝基苯 C、图3证明溴乙烷与NaOH醇溶液共热生成了乙烯 D、图4制备乙烯 -
11、下列说法正确的是( )A、根据“相似相溶”原理,能溶于水,不溶于 B、邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高 C、水加热到很高的温度都难以分解是因为水分子间存在氢键 D、烷基是推电子基团,所以甲酸、乙酸、丙酸的酸性逐渐增强
-
12、可用于制造火柴,其分子结构如图所示。下列说法不正确的是( )
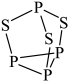 A、S元素的电负性大于P元素 B、的键角小于 C、1 mol 分子中孤电子对的数目为 D、该分子结构中S、P最外层电子数均达到8电子稳定结构
A、S元素的电负性大于P元素 B、的键角小于 C、1 mol 分子中孤电子对的数目为 D、该分子结构中S、P最外层电子数均达到8电子稳定结构 -
13、下列比较正确的是( )A、键长由小到大:金刚石<碳化硅<硅 B、熔点由低到高:二氧化碳<氧化镁<氯化钠 C、硬度由大到小:C60>铁>氯化钠 D、共价键的极性由强到弱:
-
14、配离子球棍模型如下图所示。下列关于该配离子的说法中不正确的是( )
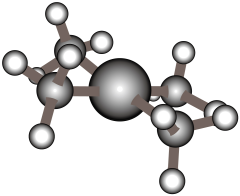 A、配位数为4 B、中的采用杂化 C、配体是 , 的空间构型为三角锥形 D、若用代替与形成配位键,则配位键的强度将减弱
A、配位数为4 B、中的采用杂化 C、配体是 , 的空间构型为三角锥形 D、若用代替与形成配位键,则配位键的强度将减弱 -
15、下列关于有机物说法正确的是( )
①酯在碱性条件下的水解反应称为皂化反应
②核酸检测是确认病毒类型
 有效手段,核酸属于天然高分子化合物
有效手段,核酸属于天然高分子化合物③油脂水解可得到氨基酸和甘油
④纤维素和淀粉都是多糖,二者互为同分异构体
⑤溴乙烷、酰胺和蛋白质在一定条件都能水解
⑥过氧化氢、乙醇、过氧乙酸等消毒液均可以将病毒氧化而达到消毒的目的
A、①②③ B、②⑤ C、⑤⑥ D、④⑤ -
16、设为阿佛伽德罗常数的值,下列说法正确的是( )A、(无机苯)的结构与苯相似,1 mol无机苯中键数目为 B、1 mol配合物中键数目为 C、100 g 46%的乙醇溶液中,含键的数目为 D、78 g苯和苯乙烯()的混合物中,含有的碳氢键数为
-
17、下列化学用语表示正确的是( )A、的VSEPR模型:
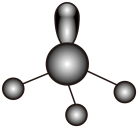 B、葡萄糖的结构简式:
C、乙酸乙酯的实验式:
D、
B、葡萄糖的结构简式:
C、乙酸乙酯的实验式:
D、 的名称为2,4,4-三甲基戊烷
的名称为2,4,4-三甲基戊烷
-
18、《凉州词》中写道“葡萄美酒夜光杯,欲饮琵琶马上催”。夜光杯的主要成分为 , 古代制作琵琶的主要原料为木料或竹料、丝线等,下列说法不正确的是( )A、美酒酿制过程中有气体产生 B、夜光杯的主要成分属于氧化物 C、木料或竹料的主要成分为纤维素 D、由蚕丝搓纺而成的丝线的主要成分为蛋白质
-
19、贝诺酯是新型的消炎、解热、镇痛、治疗风湿病的药物,可由泰诺与阿司匹林合成。

已知:ⅰ.


ii.羧酸与苯酚直接酯化困难,一般通过如下方法得到苯酚酯。
RCOOHRCOCl

ⅲ.邻羟基苯甲醛
 可形成分子内氢键,影响其熔、沸点。
可形成分子内氢键,影响其熔、沸点。 用下列方法能合成泰诺(部分反应物、条件、产物略去)。
 X
X

 (1)、中间产物X的结构简式是 , 泰诺分子中的官能团名称。(2)、写出步骤③反应的化学方程式:。(3)、步骤①的反应类型 , 在步骤①中,除X外还会得到它的同分异构体X , 工业上用蒸馏法分离X和X的混合物时,先蒸出物质的结构简式为 , 结合分子结构解释原因:。(4)、参照以上合成路线和条件,以
(1)、中间产物X的结构简式是 , 泰诺分子中的官能团名称。(2)、写出步骤③反应的化学方程式:。(3)、步骤①的反应类型 , 在步骤①中,除X外还会得到它的同分异构体X , 工业上用蒸馏法分离X和X的混合物时,先蒸出物质的结构简式为 , 结合分子结构解释原因:。(4)、参照以上合成路线和条件,以 和CH3COOH为起始原料,其他试剂任选,结合题中信息,合成阿司匹林后,再与泰诺继续合成贝诺酯(
和CH3COOH为起始原料,其他试剂任选,结合题中信息,合成阿司匹林后,再与泰诺继续合成贝诺酯( )。写出合成路线(用结构简式表示有机物) 。
)。写出合成路线(用结构简式表示有机物) 。 -
20、(1)、苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一,可采用苯乙腈为原料在实验室进行合成。请回答:
制备苯乙酸的装置如图(加热和夹持装置等略)。已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。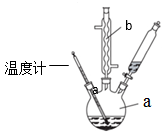
在250mL三口瓶a中加入70mL质量分数为70%的硫酸,加热至100℃,再缓缓滴入40g苯乙腈,然后升温至130℃,发生反应:
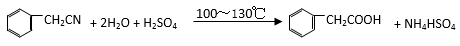
仪器b的名称是。反应结束后加适量冷水再分离出苯乙酸粗品,加入冷水的目的是。
(2)、分离出粗苯乙酸所用到的仪器是(填字母)。a.漏斗 b.分液漏斗 c.烧杯 d.玻璃棒 e.直形冷凝管
(3)、将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后加入Cu(OH)2 , 搅拌30min,过滤,滤液静置一段时间可以析出苯乙酸铜晶体,写出发生反应的化学方程式 , 混合溶剂中乙醇的作用是。(4)、下列实验不可行的是。
①将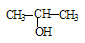 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2
②向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热,检验混合物中是否含有甲醛
③向丙烯醛(CH2=CH—CHO)中滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键
④为验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再滴入几滴硝酸银溶液,观察现象