相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、正确使用化学用语是学习化学必需的基本技能。下列化学用语表达正确的是( )A、中子数为8的碳核素: B、过氧化氢的电子式:
 C、葡萄糖的分子式:
D、聚丙烯的键线式
C、葡萄糖的分子式:
D、聚丙烯的键线式
-
2、2022年春晚,舞蹈节目《只此青绿》惊艳众人,再度将深藏博物馆的艺术史名作《千里江山图》推向了全民关注的文化热点中心。下列关于成画工序涉及化学知识的描述错误的是( )
选项
成画工序
化学知识
A
以绢为画布
蚕丝是绢的主要成分,属于蛋白质
B
以水墨描底,画出粉本
炭黑是墨的主要成分,炭黑和石墨互为同素异形体
C
以孔雀石上绿色
碱式碳酸铜是孔雀石的主要成分,常温易分解
D
以赭石 ()上红色
性质稳定不易被空气氧化
A、A B、B C、C D、D -
3、从分银渣(含Sb2S3、SnO2以及铅等杂质)中分离提取Na2SbO4和CaSnO3流程如图所示:
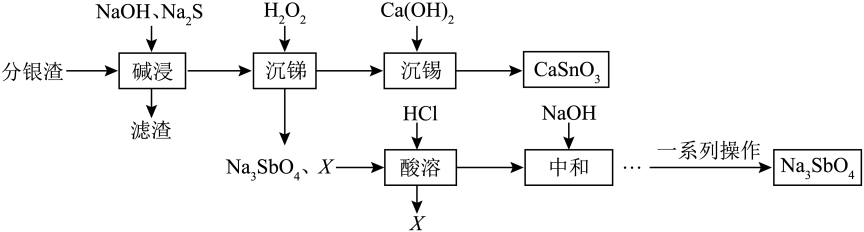
查阅资料:①Sn和C属于同主族元素,Sb和N属于同主族元素。
②“碱浸”中Sb元素发生反应的离子方程式为:、
(1)、Sn原子的质子数为50,其原子结构示意图为。(2)、“碱浸”中,可采取的方法提高浸取速率,其中,SnO2与NaOH反应的离子方程式为。(3)、“沉锑”中,X为。(4)、“沉锑”中,金属沉淀率与H2O2质量浓度关系如下图所示。为分离Sb元素和Sn元素,需控制H2O2质量浓度为 , 原因是 , 该过程Na3SbS3转化为Na2SbO4的离子方程式为。 (5)、“一系列操作”为。(6)、用1t分银渣(含Sb元素质量分数6.1%)制得51kgNa3SbO4 , 则Na3SbO4的产率为。(7)、该流程中,可循环利用的物质是(填化学式)。
(5)、“一系列操作”为。(6)、用1t分银渣(含Sb元素质量分数6.1%)制得51kgNa3SbO4 , 则Na3SbO4的产率为。(7)、该流程中,可循环利用的物质是(填化学式)。 -
4、某实验小组利用下图装置探究H2C2O4溶液与酸性KMnO4溶液的反应(夹持装置略去)。
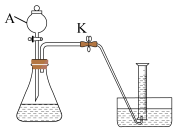
查阅资料:①H2C2O4为二元弱酸。
②溶液浓度越大,越不利于气体的扩散。
(1)、H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为。(2)、仪器A的名称为。(3)、检查装置气密性的方法为。(4)、若以单位时间内生成的气体体积作为反应速率的观测指标,则量筒中的试剂为____。A、饱和NaHCO3溶液 B、饱和NaCl溶液 C、水 D、饱和Na2CO3溶液(5)、探究H2C2O4溶液与酸性KMnO4溶液的浓度对反应速率的影响,实验数据如下表所示:实验
序号
KMnO4溶液
H2C2O4溶液
H2SO4溶液
褪色时间
c/(mol·L-1)
V/mL
c/(mol·L-1)
V/mL
c/(mol·L-1)
t/s
1
0.005
4.0
0.2
2.0
0.120
307
2
0.020
4.0
0.2
2.0
0.120
545
3
0.010
4.0
0.5
2.0
0.120
201
4
0.010
4.0
0.7
2.0
0.120
163
5
0.010
4.0
0.9
2.0
0.120
360
6
0.010
4.0
1.0
2.0
c1
512
①c1=。
②某同学从实验1和2的褪色时间分析出实验2的反应速率小于实验1,请分析该结论是否正确,并说明原因:。
③结合实验数据,下列说法错误的是。(填标号)
A.其他条件不变时,c(H2C2O4)浓度越高,反应速率越快
B.其他条件不变时,当c(H2C2O4)为0.8mol·L-1 , 褪色时间一定介于163s至360s之间
C.实验5中v(H2C2O4)=0.15mol·L-1·min-1
D.其他条件不变时,当c(H2C2O4)>0.9mol·L-1 , 溶液浓度增大,不利于CO2扩散,可能导致褪色时间延长
(6)、H2C2O4溶液与酸性KMnO4溶液生成的Mn2+对该反应有催化作用。请以实验1为对照组,设计实验方案证明Mn2+的催化作用。 -
5、木质素中的对乙基苯酚转化为苯酚与乙烯的过程如下:
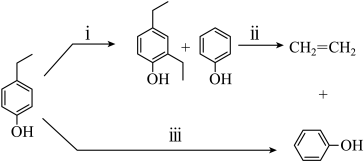 (1)、可用溴水鉴别气体产物是C2H4还是C2H6 , 化学方程式为 , 反应类型为。(2)、
(1)、可用溴水鉴别气体产物是C2H4还是C2H6 , 化学方程式为 , 反应类型为。(2)、 中苯环上的一氯代物有种。
中苯环上的一氯代物有种。 中最多个原子共平面。 (3)、反应iii能量变化如下图所示,该反应为反应(填“吸热”或“放热”),反应过程中能量的转换值为。
中最多个原子共平面。 (3)、反应iii能量变化如下图所示,该反应为反应(填“吸热”或“放热”),反应过程中能量的转换值为。 (4)、对乙基苯酚经过系列转化会生成对羟基苯甲酸。
(4)、对乙基苯酚经过系列转化会生成对羟基苯甲酸。
①可用(填试剂名称)检验物质b中的醛基。
②0.2mol c和足量的钠反应可生成LH2(标准状况)。
(5)、以乙烯为原料经过系列反应可得聚四氟乙烯。使用液态磷酸(磷酸包含在聚四氟乙烯键合的碳化硅基质中)作为电解质的氢氧燃料电池如图所示:
①利用四氟乙烯合成聚四氟乙烯的化学方程式为。
②b极的电极反应式为。
③若反应生成18gH2O,理论上外电路转移的电子的数目是。
-
6、微生物构成的氮的循环如图所示。
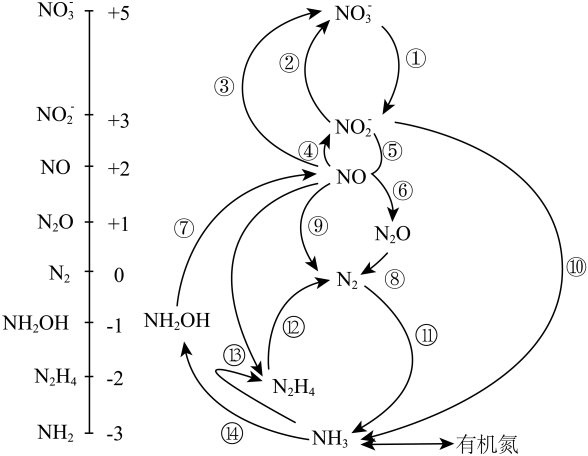 (1)、NH3的电子式为 , 与N同周期的非金属元素的气态氢化物稳定性最强的为。(2)、实验室制备NH3的化学方程式为。检验NH3是否收集满的方法为。(3)、过程⑬的化学方程式为。反应中若将H替换成D(氘),当生成20gD2O时,产物中含有的N-D键的数目为NA。(4)、羟胺(NH2OH)的结构式为 , 其与H2O2反应可实现⑦的转化,化学方程式为 , 为提高反应速率可适当升高温度,但温度过高该反应速率反而降低的原因是。
(1)、NH3的电子式为 , 与N同周期的非金属元素的气态氢化物稳定性最强的为。(2)、实验室制备NH3的化学方程式为。检验NH3是否收集满的方法为。(3)、过程⑬的化学方程式为。反应中若将H替换成D(氘),当生成20gD2O时,产物中含有的N-D键的数目为NA。(4)、羟胺(NH2OH)的结构式为 , 其与H2O2反应可实现⑦的转化,化学方程式为 , 为提高反应速率可适当升高温度,但温度过高该反应速率反而降低的原因是。 -
7、W、X、Y、Z是原子序数依次增大的短周期元素,其中只有Y和Z同周期。由上述元素组成的物质甲~已转化关系如图。其中,乙为气体,丁为有机混合物,已为淡黄色固体。下列说法正确的是( )
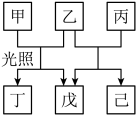 A、元素原子得电子能力:Z>W>Y>X B、甲一定属于烃类 C、氧化性:乙<己 D、X与Z可形成含非极性键的化合物
A、元素原子得电子能力:Z>W>Y>X B、甲一定属于烃类 C、氧化性:乙<己 D、X与Z可形成含非极性键的化合物 -
8、我国科学家研发了高效催化转化为NH3的路径,如图所示,下列说法错误的是( )
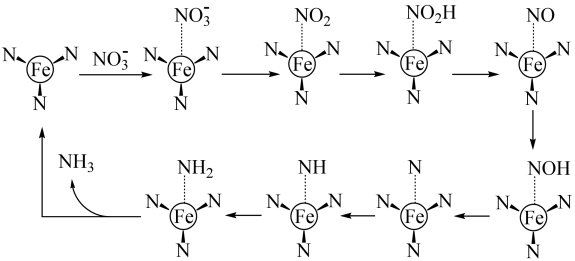 A、FeN3是催化剂 B、该路径中N元素化合价逐步降低 C、用15N标记 , 反应结束后会在FeN3中检测出15N D、该路径的总反应式为:
A、FeN3是催化剂 B、该路径中N元素化合价逐步降低 C、用15N标记 , 反应结束后会在FeN3中检测出15N D、该路径的总反应式为: -
9、我国科学家设计了一款高能量密度新型电池,装置如图所示。下列说法错误的是( )
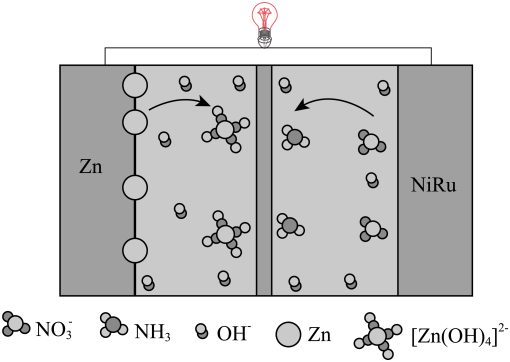 A、NiRu为正极 B、Zn电极的电极反应式为: C、工作时,电解质溶液中的OH-向Zn电极移动 D、理论上生成11.2L(标准状况)NH3时,外电路转移电子数目为8NA
A、NiRu为正极 B、Zn电极的电极反应式为: C、工作时,电解质溶液中的OH-向Zn电极移动 D、理论上生成11.2L(标准状况)NH3时,外电路转移电子数目为8NA -
10、恒温恒容下,进行反应: , 下列说法不能说明该反应已达到化学平衡状态的是( )A、生成N2的速率与消耗H2的速率相等 B、容器内压强不再改变 C、反应混合物中N2、H2、NH3的百分组成不再改变 D、单位时间内,断裂3mol H-H键的同时断裂6mol N-H键
-
11、利用CO2 , H2 , C2H2和CH3OH生产丁二酸二甲酯,其过程如图所示,下列说法错误的是( )
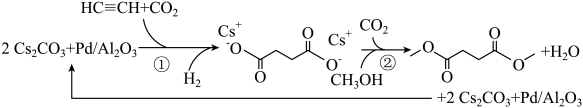 A、C2H2分子中碳碳三键和碳氢键之间的夹角为180° B、丁二酸二甲酯的分子式为C6H10O4 C、过程①未涉及碳氢键的断裂 D、过程②实现了Cs2CO3的再生
A、C2H2分子中碳碳三键和碳氢键之间的夹角为180° B、丁二酸二甲酯的分子式为C6H10O4 C、过程①未涉及碳氢键的断裂 D、过程②实现了Cs2CO3的再生 -
12、下列实验能达到目的的是( )
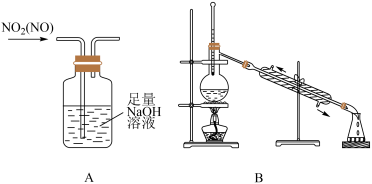
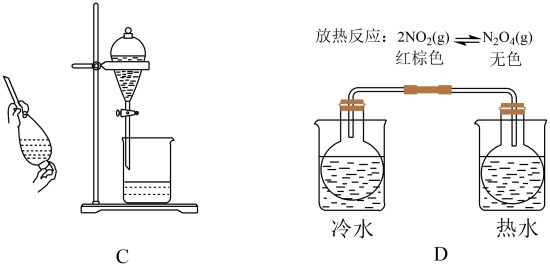 A、图A是除去NO2中的NO B、图B是米酒蒸馏 C、图C是乙醇萃取碘水中的碘 D、图D是探究温度对平衡状态的影响
A、图A是除去NO2中的NO B、图B是米酒蒸馏 C、图C是乙醇萃取碘水中的碘 D、图D是探究温度对平衡状态的影响 -
13、用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分如图所示。下列说法正确的是( )
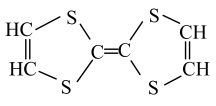 A、该有机物属于烯烃 B、四个硫原子一定共平面 C、1mol该有机物可与2mol氢气加成 D、一氯代物有2种
A、该有机物属于烯烃 B、四个硫原子一定共平面 C、1mol该有机物可与2mol氢气加成 D、一氯代物有2种 -
14、下列有关元素周期律的说法正确的是( )A、热稳定性:HCl>H2S>PH3 B、离子半径:O2->Al3+>Na+ C、元素原子失电子能力:Be>K>Mg D、酸性:HNO3>H2SiO3>H2CO3
-
15、甲酸和乙醇在浓硫酸作用下反应生成甲酸乙酯,该反应中各物质的化学用语或模型错误的是( )A、甲酸的结构式为:
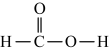 B、乙醇的球棍模型:
B、乙醇的球棍模型: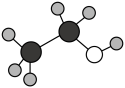 C、甲酸乙酯的结构简式:CH3COOCH3
D、H2O的电子式:
C、甲酸乙酯的结构简式:CH3COOCH3
D、H2O的电子式: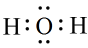
-
16、福建土楼的外墙是用糯米,石灰、黏土和细砂混合而成。夯筑时,往墙体中间埋入竹片作为“墙骨”。下列说法错误的是( )A、糯米的主要成分是淀粉,其作用是充当粘合剂 B、石灰的主要成分是CaSO4 , 其作用是防水 C、细砂的主要成分是SiO2 , 其作用是增大墙体的强度 D、“墙骨”的主要成分是纤维素,其作用是增加墙体的韧性
-
17、化合物G是一种药物合成中间体,其合成路线如下:
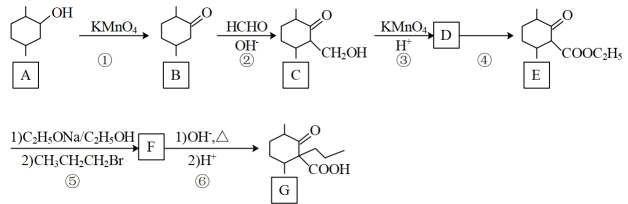
回答下列问题:
(1)、E中的官能团名称是 , ②的反应类型是。(2)、碳原子上连有4个不同的原子或基团时,该碳称为手性碳。用星号(*)标出B中的手性碳。。(3)、B的同分异构体中,含有六元环且能发生银镜反应的化合物共有种(不考虑立体异构)。写出其中核磁共振氢谱有6种不同化学环境的氢,峰面积比为1:1:1:4:4:3的结构简式。(4)、D→E的化学方程式为。(5)、下列说法正确的是____。A、E→F的反应类型为加成反应 B、化合物A与乙醇互为同系物 C、化合物G的分子式是 D、化合物B一氯代物有7种(6)、设计由甲苯和乙酰乙酸乙酯()制备 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。 -
18、对氨基苯磺酸是制备药物的重要中间体,可用苯胺(
 )、浓硫酸为原料合成。实验流程、装置示意图如下。
)、浓硫酸为原料合成。实验流程、装置示意图如下。 
相关数据如下表:
名称
相对分子质量
熔点/℃
沸点/℃
溶解性
苯胺
93
184
微溶于水,溶于乙醇、乙醚等有机溶剂
对氨基苯磺酸
173
288
——
微溶于冷水,溶于热水,不溶于乙醇、乙醚等有机溶剂
回答下列问题:
(1)、仪器A的名称。(2)、写出该反应的化学方程式。(3)、步骤1中加热方式是(填“水浴”、“油浴”或“直接加热”)。步骤1加入浓硫酸时,为防止温度过高致苯胺被氧化,可采取的措施有。(4)、下列有关说法正确是____A、反应产物中可能有邻氨基苯磺酸 B、冷凝管进出水方向是b进a出 C、如果加热后发现忘加沸石,应立刻补加 D、步骤2将混合液倒入盛有冷水烧杯中,用玻璃棒摩擦器壁可促使晶体析出(5)、对氨基苯磺酸粗产品因含杂质而显色,可用重结晶法进行提纯。从下列选项中选择合理操作并排序:()→()→()→()→过滤→洗涤→干燥。a.沸水溶解 b.过滤 c.趁热过滤 d.蒸发结晶 e.冷却结晶 f.加入活性炭
(6)、对氨基苯磺酸与对二甲氨基苯甲醛在一定条件下可以发生显色反应。利用这一原理,用分光光度法可以测定对氨基苯磺酸的含量,吸光度与对氨基苯磺酸浓度关系如图所示。
取1.00 g对氨基苯磺酸样品,配成1 L溶液,取样加入显色剂,测得吸光度为0.52。则样品中对氨基苯磺酸的质量分数是。
-
19、第Ⅷ族元素铁、钴、镍性质相似,称为铁系元素。单质及其化合物在生命科学、工业生产等领域有着重要的应用。回答下列问题。(1)、卟吩分子中所有原子共平面,具有独特的电子结构,其结构如图1。血红素是由中心与配体卟吩衍生物结合成的大环配位化合物,其结构如图2。
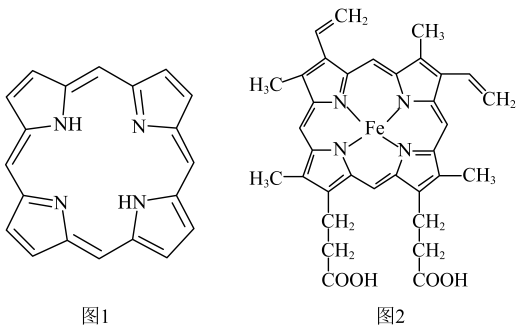
卟吩分子中N原子采取杂化,血红素中心离子的配位数为 , 血红素中含有的化学键有(填序号)。
a.离子键 b.共价键 c.氢键 d.配位键 e.金属键
(2)、某种半导体NiO具有NaCl型结构(如图),其晶胞参数为a pm。
①已知阿伏加德罗常数为 , 则NiO晶体的摩尔体积。(列出算式)
②NiO晶体中部分O原子被N原子替代后可以改善半导体的性能,键中离子键成分的百分数小于键,原因是。
③若该晶胞中氧原子有25%被氮原子替代,则该晶体的化学式为;N所替代的O的位置可能是。
-
20、完成下列问题(1)、基态的核外电子排布式。(2)、
 的系统命名法为 , (3)、苯酚钠溶液中通入少量二氧化碳反应的离子方程式。(4)、肉桂醛(
的系统命名法为 , (3)、苯酚钠溶液中通入少量二氧化碳反应的离子方程式。(4)、肉桂醛( )发生银镜反应的化学方程式。
)发生银镜反应的化学方程式。