相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、NA为阿伏加德罗常数的值,下列说法正确的是( )A、标准状况下,44.8L CH2Cl2含有的分子数为2NA B、34gH2S气体中含有的H+数目为2NA C、常温下,pH=13 的Na3PO4溶液中含有的OH-数目为0.1NA D、64g环状(S8)分子中含有的S-S键数为2NA
-
2、工业上以氯化钠为原料可制得、、、和等。下列说法正确的是( )A、、中氯原子都满足8电子稳定结构,它们的化学性质相同 B、中夹角大于中夹角 C、是含有极性键的非极性分子 D、、、的酸性依次增强
-
3、下列化学用语或图示表达正确的是( )A、、、都是碱性氧化物 B、顺-2-丁烯的结构简式:
 C、中子数为10的氧原子:
D、基态的价层电子的轨道表示式:
C、中子数为10的氧原子:
D、基态的价层电子的轨道表示式:
-
4、下列应用中末涉及氧化还原反应的是( )A、、溶液均不能保存在玻璃试剂瓶中 B、常温下,浓硫酸、浓硝酸常保存在铁罐中 C、保存溶液时,通常在溶液中加入少量的单质铁 D、可用于自来水的消毒、净化
-
5、化学与生产、生活、科技密切相关。下列说法错误的是( )A、用于火箭发动机的碳化硅陶瓷是一种新型无机非金属材料 B、“一带一路”是现代版的“丝绸之路”,丝绸的主要成分是纤维素 C、马家窑文化遗址出土的单刃青铜刀属于青铜制品,青铜是一种合金 D、船体上镶嵌的锌块是利用牺牲阳极法来避免船体遭受腐蚀
-
6、锰酸锂(LiMn2O4)可作为锂离子电池的正极材料,在工业上可利用软锰矿浆(主要成分为MnO2 , 含少量Fe2O3、FeO、Al2O3、SiO2等杂质)吸收含硫烟气(主要成分SO2)制备锰酸锂,生产流程:

已知:①软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强。
②在此流程中部分金属阳离子生成氢氧化物沉淀的pH如表:
沉淀物
Fe(OH)3
Fe(OH)2
Al(OH)3
Mn(OH)2
开始沉淀
2.7
7.6
3.4
7.7
完全沉淀
3.7
9.6
4.7
9.8
(1)、含硫烟气在通入软锰矿浆前需要先冷却,冷却的原因是。(2)、滤液1中所含金属阳离子有(填离子符号)。(3)、在实际生产中,Li2CO3与MnO2按物质的量之比1∶4混合均匀加热制取LiMn2O4 , 反应过程:升温到515℃时,Li2CO3开始分解产生CO2和碱性氧化物A,写出A的名称 , 此时比预计Li2CO3的分解温度(723℃)低得多,可能原因是。(4)、由“滤液1”得到“滤液2”同时回收Al(OH)3的实验方案如下:边搅拌边向滤液1中加入 , 再加入NaOH溶液调节pH范围为 , 过滤得到滤液2和滤渣,向滤渣中加入NaOH溶液pH≥12,搅拌、过滤,再向所得滤液中通入过量的CO2过滤、洗涤、低温烘干得Al(OH)3。(5)、工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺:a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是 , 宜选用(“阳”或“阴”)离子交换膜。
②b中,生成Li2CO3反应的化学方程式是。
-
7、钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。工业制备钴常用硫钴矿石(主要成分常含钙、镁、铜、铁等化合物),流程如下:

已知:①常温相关氢氧化物的值如下:
物质
②酸性条件下极难被氧化。
(1)、基态钴原子价层电子排布式为。(2)、已知钴与铁均为Ⅷ族元素,具有类似的化合价,中的化合价。(3)、硫酸浸取焙砂的过程中,温度及硫酸的浓度对金属离子浸出的影响如图所示,考虑生产成本和效率,最佳的浸出温度为℃,最佳的硫酸浓度为mol/L。 (4)、向浸取液中加入发生的主要反应的离子方程式为 , 滤渣1的主要成分是。(5)、电解精炼的过程中,粗钴与电源极相连,用硫酸钴溶液作为电解质,控制阴极室为3~5之间,若值过低,在纯钴的电极表面产生气体,该气体可能是。
(4)、向浸取液中加入发生的主要反应的离子方程式为 , 滤渣1的主要成分是。(5)、电解精炼的过程中,粗钴与电源极相连,用硫酸钴溶液作为电解质,控制阴极室为3~5之间,若值过低,在纯钴的电极表面产生气体,该气体可能是。A. B. C. D.
(6)、若沉钴中得到二水合草酸钴()热分解质量变化过程如图所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物,请写出从反应B点到C点的化学方程式。
-
8、是离子晶体,其晶胞如下图1所示(已知氟化钙晶胞参数为a pm,表示阿伏加德罗常数的值),难溶于水、可溶于酸。常温下,用盐酸调节浊液的pH,测得在不同pH条件下,体系中与(X为或)的关系如图2所示。下列说法错误的是。( )
 A、每个氟化钙晶胞中含有的数目为4个 B、氟化钙的晶体密度为 C、表示与的变化曲线 D、的数量级为
A、每个氟化钙晶胞中含有的数目为4个 B、氟化钙的晶体密度为 C、表示与的变化曲线 D、的数量级为 -
9、已知:CH4(g)+2H2S(g) CS2(g)+4H2(g)。向恒容密闭容器中充入0.1molCH4和0.2molH2S,下图所示:

下列说法正确的是( )
A、该反应的△H<0 B、X 点CH4的转化率为30% C、X点与Y点容器内压强比为55:51 D、维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1mol 时v(正)<v(逆) -
10、一种生物电化学方法脱除水体中NH的原理如图所示:

下列说法正确的是( )
A、装置工作时,化学能转变为电能 B、装置工作时,a极周围溶液pH降低 C、装置内工作温度越高,NH脱除率一定越大 D、电极b上发生的反应之一是:2NO-2e-=N2↑+3O2↑ -
11、根据下列实验,不能证明一元酸HR为弱酸的是( )A、室温下,NaR溶液的pH大于7 B、25℃时,0.01mol/L的HR溶液pH=2.8 C、加热NaR溶液时,溶液的pH变小 D、HR溶液加入少量NaR固体,溶解后溶液的pH变大
-
12、根据下列实验操作和现象所得到的结论正确的是( )
选项
实验操作和现象
实验结论
A
向酸性含碘废水中加入淀粉溶液,然后滴入少量Na2SO3溶液,废水立刻变蓝色
该废水中可能含IO3-
B
向Fe(NO3) 3 溶液中加入铁粉,充分振荡,再滴加少量盐酸酸化后,滴入1滴KSCN溶液,溶液变红
原Fe(NO3)3 只有部分被Fe还原
C
向1-溴丙烷中加入KOH溶液,加热并充分振荡,然后取少量液体滴入AgNO3溶液,出现棕黑色沉淀
1-溴丙烷中混有杂质
D
将乙醇与浓硫酸混合溶液加热,产生的气体直接通入酸性KMnO4溶液,溶液紫色逐渐褪去
产生的气体一定是乙烯
A、A B、B C、C D、D -
13、已知: 常温下,(1) Ka1(H2CO3)=4.3×10-7 , Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
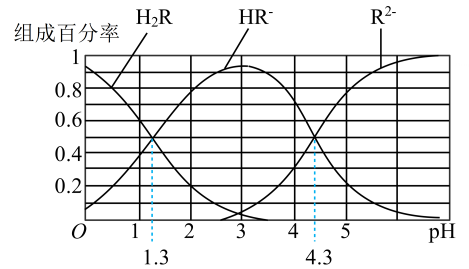 A、在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-) B、等体积等浓度的NaOH溶液与H2R溶液混合后,溶液中水的电离程度比纯水大 C、在pH=3的溶液中存在c(R2−)×c(H2R)/c2(HR−)=10-3 D、向Na2CO3溶液中加入少量H2R溶液,发生反应:2+H2R=2HCO3-+R2-
A、在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-) B、等体积等浓度的NaOH溶液与H2R溶液混合后,溶液中水的电离程度比纯水大 C、在pH=3的溶液中存在c(R2−)×c(H2R)/c2(HR−)=10-3 D、向Na2CO3溶液中加入少量H2R溶液,发生反应:2+H2R=2HCO3-+R2- -
14、下列物质的转化在给定条件下能实现的是( )A、H2SO4(稀) SO2NH4HSO3(NH4)2SO3 B、NH3NONO2HNO3 C、FeFeCl2Fe(OH)2Fe(OH)3 D、AlNaAlO2AlCl3溶液无水AlCl3
-
15、2021年中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二氧化碳转化为甲烷的新型催化转化方法: , 这是迄今最接近人造光合作用的方法,加氢制的一种催化机理如图。下列说法正确的是( )
 A、反应中是中间产物 B、转化为利用了的氧化性 C、经过活性中心裂解产生带负电荷的H D、使用催化剂可以降低反应的焓变,从而提高化学反应速率
A、反应中是中间产物 B、转化为利用了的氧化性 C、经过活性中心裂解产生带负电荷的H D、使用催化剂可以降低反应的焓变,从而提高化学反应速率 -
16、设NA为阿伏加德罗常数的值。下列叙述正确的是( )A、标准状况下,2.24 L 二氯甲烷中含有的碳氯共价键数目为0.2NA B、50 mL 12 mol/L盐酸与足量MnO2加热反应,转移的电子数目为0.3NA C、向含0.1 molNH4Al(SO4)2的溶液中滴加NaOH溶液至沉淀恰好完全溶解,消耗OH-数目为0.5NA D、电解精炼铜时,若阴极得电子数为2NA , 则阳极质量减少64克
-
17、下列根据反应原理设计的应用,不正确的是( )A、CO+H2O⇌HCO+OH- 热的纯碱溶液清洗油污 B、Al3++3H2O⇌Al(OH)3(胶体)+3H+ 明矾净水 C、TiCl4+(x+2)H2O(过量)=TiO2·xH2O↓+4HCl 用TiCl4制备TiO2 D、SnCl2+H2O⇌Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入NaOH固体
-
18、常温下,下列各组离子在指定溶液中不能大量共存的是( )A、透明澄清的溶液中:、、、 B、氨水溶液中:、、、 C、的溶液中:、 , 、 D、无色溶液中:、、、
-
19、设为阿伏加德罗常数的值。下列说法正确的是( )A、在标准状况下,分子中含氯原子数目为 B、1LpH均为2的硫酸和醋酸溶液,氢离子数均为 C、64g铜与足量硫粉加热充分反应,转移电子数为 D、30g由乙酸和葡萄糖组成的混合物中含氢原子个数为
-
20、下列物质性质与用途具有对应关系的是( )A、浓硫酸具有脱水性,可用于干燥、气体 B、密度比空气大,可用作镁着火时的灭火剂 C、溶液能与Cu反应,可用作铜制线路板的蚀刻剂 D、易溶于水,可用作木材防火剂