相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、短周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y最外层电子数是K层的3倍,Z与Y同主族。下列说法正确的是( )A、原子半径:X<Y<Z<W B、X、Y可形成一种红棕色气体 C、Z的简单气态氢化物的热稳定性比W的强 D、X、Z、W形成的氧化物均为酸性氧化物
-
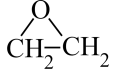
2、下列反应符合最理想的“原子经济性反应”的是( )A、 B、 C、 D、2CH2=CH2+O22
-
3、2023年4月22日,中国海军举行海军成立纪念日舰艇开放日活动,下列开放日展示的物品不涉及有机高分子材料的是( )A、直8直升机驾驶舱前的硅酸盐玻璃 B、防毒面具上的橡胶软壳 C、由功能纤维制成的防护服 D、由涤纶布制成的国旗
-
4、在给定条件下,下列物质间的转化不能实现的是( )A、NH3NO B、FeFe3O4 C、SiO2Na2SiO3 D、CuNO2
-
5、己烷[CH3(CH2)4CH3]是一种具有汽油味的有机溶剂,被广泛应用于有机合成、机械设备表面清洗去污等。下列与己烷互为同分异构体的是( )A、
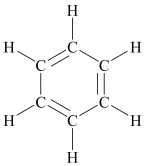 B、
B、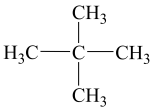 C、
C、 D、CH3-CH2-CH=CH-CH2-CH3
D、CH3-CH2-CH=CH-CH2-CH3
-
6、唐三彩、秦兵马俑制品的主要材料在成分上属于( )A、氧化铝 B、硅酸盐 C、二氧化硅 D、合金
-
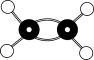
7、下列化学用语的表示错误的是( )A、丙烯的结构简式: B、乙酸的分子式: C、含有1个中子的氢核素:1H D、乙烯的球棍模型:
-
8、我国积极启动“蓝天工程”和“绿水工程”,是保护生态环境、提高全体人民生活质量的重要举措。下列措施不利于以上工程实施的是( )A、在燃煤中添加生石灰 B、在燃油汽车上安装尾气催化转化器 C、将废旧电池分类回收,深埋处理 D、工业废水排放前要“脱硝”、“除磷”,防止水体富营养化
-
9、利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实,某化学兴趣小组在实验室中模拟上述过程。其设计的模拟装置如图所示:

完成下列填空:
(1)、装置C中发生反应的化学方程式为(只写第一步)。(2)、若C中参加反应的甲烷与氯气的体积之比为1∶2,两者反应后得到的产物中物质的量最大的是(填化学式)。(3)、装置B有三种功能:①控制气体流速;②干燥气体;③。(4)、装置D的石棉浸有足量KI溶液,其作用是。(5)、甲同学认为若E中有氯化氢产生,则一定可以说明甲烷与氯气发生了取代反应,这个观点(填“正确”或“不正确”),理由是。(6)、有机物M是甲烷的同系物,M的相对分子质量为86,则有机物M的结构有种。 -
10、甲、乙、丙三位同学分别用如图实验装置及化学药品(碱石灰为氢氧化钠和生石灰的混合物)制取氨气。
 (1)、他们制取氨气的化学方程式为。(2)、他们收集氨气的方法是。(3)、三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是(填“甲”、“乙”或“丙”)。(4)、检验氨气是否收集满的方法是(简述操作方法、现象和结论)。(5)、三位同学都认为,采用上述各自的装置,还可用于加热碳酸氢铵固体的方法来制取纯净的氨气,你认为哪位同学能够达到实验目的(填“甲”、“乙”或“丙”)。他们还认为,装置中的NH4HCO3固体可用NH4Cl固体代替,你认为(填“能”或“不能”)。(6)、氨气被催化氧化的化学方程式是。
(1)、他们制取氨气的化学方程式为。(2)、他们收集氨气的方法是。(3)、三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是(填“甲”、“乙”或“丙”)。(4)、检验氨气是否收集满的方法是(简述操作方法、现象和结论)。(5)、三位同学都认为,采用上述各自的装置,还可用于加热碳酸氢铵固体的方法来制取纯净的氨气,你认为哪位同学能够达到实验目的(填“甲”、“乙”或“丙”)。他们还认为,装置中的NH4HCO3固体可用NH4Cl固体代替,你认为(填“能”或“不能”)。(6)、氨气被催化氧化的化学方程式是。 -
11、如图所示为原电池装置示意图。回答下列问题:
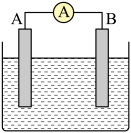 (1)、将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是____(填字母)。A、铝片、铜片 B、铜片、铝片 C、铝片、铝片 D、铜片、铜片(2)、若A为Pb,B为PbO2 , 电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出A电极反应式:;该电池在工作时,B电极的质量将(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1molH2SO4 , 则转移电子的数目为。(3)、若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2 , 该电池即为甲烷燃料电池,写出A电极反应式:;该电池在工作过程中,正极附近溶液的pH值(填“增大”、“减小”或“不变”)若该电池工作时转移了0.4mol电子,则生成水的质量为。
(1)、将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是____(填字母)。A、铝片、铜片 B、铜片、铝片 C、铝片、铝片 D、铜片、铜片(2)、若A为Pb,B为PbO2 , 电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出A电极反应式:;该电池在工作时,B电极的质量将(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1molH2SO4 , 则转移电子的数目为。(3)、若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2 , 该电池即为甲烷燃料电池,写出A电极反应式:;该电池在工作过程中,正极附近溶液的pH值(填“增大”、“减小”或“不变”)若该电池工作时转移了0.4mol电子,则生成水的质量为。 -
12、回答下列问题:(1)、1902年德国化学家哈伯研究出合成氨的方法。断开1molH-H键、N-H键、N≡N键分别需要吸收的能量为436kJ,391kJ,946kJ。则氮气和氢气生成1molNH3(填“吸收”或“放出”)的热量Q=kJ。在密闭容器中0.5molN2和1.5molH2充分反应后热量变化小于Q,原因是:。(2)、推测反应2NH3(l)2N2(g)+3H2(g)比反应2NH3(g)2N2(g)+3H2(g)(填“吸收”或“放出”)的热量(填“多”或“少”)。(3)、已知稀溶液中1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出稀溶液中H2SO4与NaOH发生中和反应时,表示中和热的热化学反应方程式:。(4)、已知下列热化学方程式:
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3kJ·mol-1
②C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
③2H2(g)+O2(g)=2H2O(1)△H3=-571.6kJ·mol-1
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:。
-
13、向绝热恒容密闭容器(绝热容器指该容器可阻止热量的传递,散失,对流)中通入和 , 在一定条件下发生反应 , 正反应速率随时间变化的示意图如图所示,下列结论中正确的个数为( )
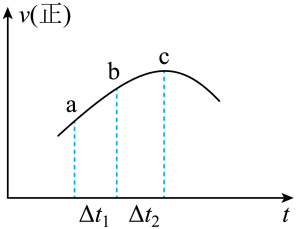
①反应在c点达到反应进行的限度
②浓度:a点小于c点
③逆反应速率图像在此时间段内和图中趋势相同
④ , ab段的消耗量小于bc段的消耗量
⑤混合物颜色不再变化,说明反应达到平衡
⑥体系压强不再变化,说明反应达到平衡
A、2个 B、3个 C、4个 D、5个 -
14、同温同压下,某有机物和过量Na反应得到V1 L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2 L二氧化碳,V2= 2V1≠0,则该有机物可能是( )A、
 B、HOOCCH2CH2COOH
C、HOCH2CH2OH
D、
B、HOOCCH2CH2COOH
C、HOCH2CH2OH
D、
-
15、某稀硫酸和稀硝酸的混合溶液200 mL,其中c(H+)=1.5 mol/L,c( )=0.55 mol/L。向该混合溶液加入5.76g铜粉(若硝酸只被还原为NO气体),待充分反应后(不考虑溶液体积的变化),下列说法错误的是( )A、原混合溶液中c(HNO3)=0.4 mol/L B、反应后铜有剩余,加盐酸,铜会继续溶解 C、反应中转移了0.18mol电子 D、溶液中Cu2+的物质的量浓度为0.45mol/L
-
16、鱼雷采用的动力电池是以溶有KOH的流动海水为电解液,电池反应为 , 下列说法正确的是( )A、电池工作过程中正极附近区域碱性增强 B、负极的电极反应式为 C、电子由电极经外电路流向Al电极 D、电池工作过程中,向电极移动
-
17、工业上用X(
 )合成Y(
)合成Y( ),下列有关分析正确的是( ) A、X与HCl气体加成,产物只有一种结构 B、若Y的相对分子质量(平均值)为19600,则n=380 C、Y的相对分子质量为X的n倍 D、Y能使溴的溶液褪色
),下列有关分析正确的是( ) A、X与HCl气体加成,产物只有一种结构 B、若Y的相对分子质量(平均值)为19600,则n=380 C、Y的相对分子质量为X的n倍 D、Y能使溴的溶液褪色 -
18、有机物M是一种重要的化工原料,结构简式如图所示,下列有关M的说法正确的是( )
 A、有机物M为烃类 B、该有机物的分子式为C17H16O2 C、分子中的所有原子可能共平面 D、能发生加成反应,不能发生取代反应
A、有机物M为烃类 B、该有机物的分子式为C17H16O2 C、分子中的所有原子可能共平面 D、能发生加成反应,不能发生取代反应 -
19、化学反应速率和化学反应限度是化工生产研究的主要问题之一,下列对化学反应速率和反应限度的认识错误的是( )A、使用催化剂是为了增大反应速率,提高生产效率 B、对任何化学反应来说,反应速率越大,对应现象越明显 C、任何可逆反应都有一定的限度,且限度是可以改变的 D、影响化学反应速率的客观因素是温度、浓度、压强和催化剂
-
20、某化学兴趣小组利用乙醇和乙酸制备乙酸乙酯的装置如图。下列有关叙述中错误的是( )
 A、试管a中发生的反应中乙酸断开碳氧单键 B、试管b中可观察到有无色透明油状液体产生 C、乙醇可被酸性重铬酸钾一步氧化为乙酸 D、油脂与乙酸乙酯互为同系物
A、试管a中发生的反应中乙酸断开碳氧单键 B、试管b中可观察到有无色透明油状液体产生 C、乙醇可被酸性重铬酸钾一步氧化为乙酸 D、油脂与乙酸乙酯互为同系物