相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、某物质的结构简式为
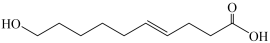 ,下列有关该物质的叙述正确的是( ) A、该物质有三种含氧官能团 B、既是乙醇的同系物也是乙酸的同系物 C、与
,下列有关该物质的叙述正确的是( ) A、该物质有三种含氧官能团 B、既是乙醇的同系物也是乙酸的同系物 C、与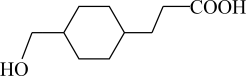 互为同分异构体
D、1mol该物质与碳酸钠反应得
互为同分异构体
D、1mol该物质与碳酸钠反应得
-
2、变量控制是科学研究的重要方法。四支相同的试管中分别盛有2mL5%H2O2溶液,向其中加入水或1mol·L-1FeCl3溶液,在下列条件下发生反应,其中化学反应速率最大的是( )
A
B
C
D
加入试剂
2滴水
2滴水
2滴FeCl3溶液
2滴FeCl3溶液
水浴温度/℃
20
40
20
40
A、A B、B C、C D、D -
3、类比法是一种学习化学的重要方法。下列“类比”合理的是( )
选项
已知
类比
A
稀溶液构成原电池,Mg做负极
稀溶液构成原电池,Mg做负极
B
工业上,电解熔融冶炼金属Mg
工业上,电解熔融冶炼金属Al
C
与反应生产 , 是酸性氧化物
与反应生产 , 是酸性氧化物
D
能使溶液和溴水褪色,且原理相同
能使溶液和溴水褪色,且原理相同
A、A B、B C、C D、D -
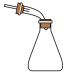
4、下列实验装置或操作正确且能达到实验目的的是( )
选项
A
B
C
D
装置操作

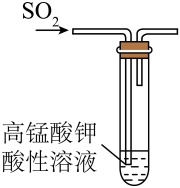
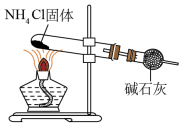
目的
熔化固体
检验二氧化硫的还原性
制备氨气
接收石油分馏所得馏分
A、A B、B C、C D、D -
5、设为阿伏加德罗常数的值,下列说法不正确的是( )A、和的固体混合物中含有的阳离子数为 B、标准状况下,含有的原子数为 C、某密闭容器中盛有和各充分反应后,分子的数目为 D、加热条件下,足量的硫黄与64克的铜反应转移的电子数为
-
6、下列关于基本营养物质说法正确的是( )A、淀粉和纤维素是天然有机高分子化合物,互为同分异构体 B、蛋白质在酸、碱或酶的作用下能发生水解反应 C、植物油含较多饱和脂肪酸的甘油酯,动物油含较多不饱和脂肪酸的甘油酯 D、糖类、油脂、蛋白质均是由C、H、O、N四种元素组成的
-
7、a、b、c、d四种金属,已知:①a+b2+=b+a2+;②将金属片a、c插入稀硫酸中,用导线将它们与电流表相连,a表面有大量气泡逸出;③b、d用导线连接放入d的硫酸盐溶液中,电极反应为d2++2e-=d,b-2e-=b2+。则这四种金属的活动性由强到弱的顺序是( )A、c>a>b>d B、d>b>a>c C、c>b>a>d D、d>c>a>b
-
8、下列离子方程式正确的是( )A、向稀中滴加溶液: B、向溶液中通入过量 C、铅酸蓄电池放电时的正极反应: D、燃料电池,当电解质为溶液时,负极反应:
-
9、一氯取代物没有同分异构体的烷烃是( )A、2-甲基丙烷 B、2,2-二甲基丙烷 C、2-甲基丁烷 D、2,3-二甲基丁烷
-
10、下列有关化学用语正确的是( )A、乙醇的结构式:
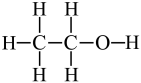 B、的电子式:
B、的电子式: C、葡萄糖的结构简式:
D、的结构式
C、葡萄糖的结构简式:
D、的结构式
-
11、以庚烷等为原料合成高分子材料E和I的合成路线如下:
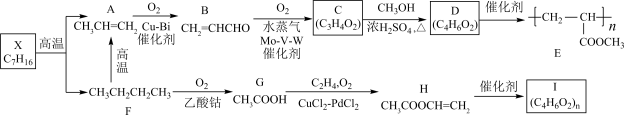
回答下列问题:
(1)、B→C的反应类型为。(2)、C→D的化学方程式为。(3)、物质E的单体为。(4)、G的化学名称是。(5)、H中官能团的名称为。(6)、G→H的过程中有乙烯参与反应,下列关于乙烯的说法正确的是____(填字母)。A、乙烯为不饱和烃 B、乙烯与苯均含有碳碳双键 C、乙烯在空气中燃烧火焰明亮并伴有黑烟 D、除去乙烷中混有的乙烯,可在催化剂加热条件下向混合气中通入过量氢气(7)、I的结构简式为。 -
12、某化学学习小组为了探究铁质材料碳素钢(仅含有C和Fe)和浓硫酸反应的气体产物,利用下列装置(部分夹持仪器已省略)进行了如下实验探究活动:

回答下列问题:
(1)、仪器X的名称为。(2)、能证明实验生成的实验现象为;进入装置C中被氧化为 , 被还原为 , 写出该反应的离子方程式:。(3)、实验过程中观察到G中无水硫酸铜由白色变成蓝色,F中发生反应的化学方程式为;产生该气体(F中的反应物)的原因为。(4)、若装置D中澄清石灰水变浑浊,装置H中澄清石灰水未变浑浊,再结合(3)推知碳素钢与浓硫酸反应产生的气体中除了含有外,还有(填化学式);铁质材料中碳与浓硫酸反应的化学方程式为。装置H后增加装置I的目的是。 -
13、放热反应在生产、生活中用途广泛。回答下列问题:(1)、前期的火箭曾用液态肼()与双氧水反应来提供能量。已知0.4mol(l)与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量。
①此反应的化学方程式为。
②16g液态肼与足量的双氧水发生上述反应,放出kJ热量。
(2)、甲烷可以消除氮氧化物污染:。温度为800℃的条件下,向恒容密闭的容器中通入(g)和(g),使 , , 在不同催化剂作用下进行反应,测得随时间的变化情况如下表:实验序号
10
20
30
40
50
1
800
0.80
0.67
0.57
0.50
0.50
2
800
0.60
0.50
0.50
0.50
0.50
实验1中,在10~20min内, , 40min时v(正)(填“大于”“小于”或“等于”)v(逆)。
(3)、催化效率:实验1(填“>”“<”或“=”)实验2.(4)、乙醇()应用于燃料电池,该电池采用可传导的固体氧化物为电解质,其工作原理如图所示。a极为原电池的(填“正”或“负”)极;b极电极反应式为。 (5)、乙醇在Cu作催化剂时与氧气反应的关系如图所示,整个反应中物质B属于(填“催化剂”或“中间产物”)。
(5)、乙醇在Cu作催化剂时与氧气反应的关系如图所示,整个反应中物质B属于(填“催化剂”或“中间产物”)。
-
14、海洋中蕴含着丰富的资源,我们通过“浓缩、氧化、提取”等步骤获取溴、碘单质等资源。回答下列问题:(1)、Ⅰ.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲:苦卤含溴海水含溴空气溴水混合物溴蒸气液溴
乙:苦卤含溴海水溴蒸气液溴
对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中较符合实际工业生产要求且能耗较低的是 (填“甲”或“乙”)。(2)、甲同学设计的流程中,步骤③通入热空气或水蒸气吹出Br2 , 利用了溴的性;步骤④中发生反应的化学方程式为 。(3)、Ⅱ.对比溴元素的提取,碘元素是从海洋植物如海带、海藻中提取,某提取碘单质的工艺流程如图。
步骤③操作名称为 ;步骤④的离子方程式为 。 (4)、从含碘的某溶液中提取碘,还要经过蒸馏,指出下列蒸馏装置中的错误之处:(任写两点)。
(4)、从含碘的某溶液中提取碘,还要经过蒸馏,指出下列蒸馏装置中的错误之处:(任写两点)。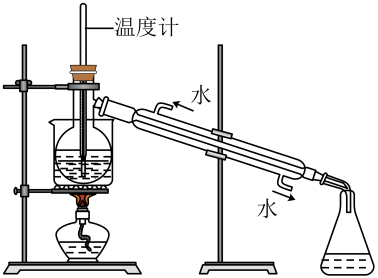
-
15、下列实验操作和现象能达到实验目的的是( )
选项
实验操作和现象
实验目的
A
向两支盛有溶液的试管中分别加入溶液和1mol/LCuSO4溶液,溶液中产生气泡速率快
验证催化分解效果优于
B
两个封有和混合气体的圆底烧瓶分别浸泡在和的水中,的水中烧瓶里气体的颜色比较浅
验证调控温度可以改变可逆反应进行的程度
C
向稀硫酸中加入Zn粒,有气泡冒出,再加入几滴溶液,产生气泡的速度加快
验证是与稀硫酸反应的催化剂
D
向酸性高锰酸钾溶液中通入气体X后,酸性高锰酸钾溶液褪色
验证气体X中一定含有
A、A B、B C、C D、D -
16、下列实验无法达到预期实验目的的是( )
 A、用甲验证与浓硝酸反应的热量变化 B、用乙验证易溶于水 C、用丙制取并收集少量氨气 D、用丁验证与反应
A、用甲验证与浓硝酸反应的热量变化 B、用乙验证易溶于水 C、用丙制取并收集少量氨气 D、用丁验证与反应 -
17、下列对应离子方程式书写正确的是( )A、铜溶于稀硝酸:Cu+4HNO3=Cu2++2NO+2H2O+2NO2↑ B、向Al2O3中滴加NaOH溶液:Al2O3+2OH-=2AlO+H2O C、将少量Na2O2投入水中:Na2O2+H2O=2Na++2OH-+O2↑ D、向水中通入适量Cl2:Cl2+H2O2H++Cl-+ClO-
-
18、山梨酸是一种常用的食品防腐剂,其结构简式为(CH3-CH=CH-CH=CH-COOH。下列关于山梨酸的说法中错误的是( )A、可以发生加成、取代、氧化等反应 B、可以与NaHCO3溶液反应产生气泡 C、山梨酸属于烯烃 D、可以通过加聚反应制备高分子化合物
-
19、某锂离子电池的工作原理如图所示(a极材料为金属锂和石墨的复合材料),其电池反应为Li+FePO4=LiFePO4。下列关于该电池的说法正确的是( )
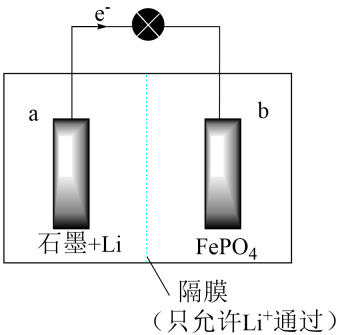 A、a极为正极 B、b极发生氧化反应 C、Li+从a极室向b极室移动 D、可以用稀硫酸作电解质溶液
A、a极为正极 B、b极发生氧化反应 C、Li+从a极室向b极室移动 D、可以用稀硫酸作电解质溶液 -
20、下列食品添加剂与类别对应正确的一组是( )A、着色剂——胡萝卜素、苯甲酸钠 B、调味剂——亚硝酸钠、味精 C、防腐剂——胭脂红、山梨酸钾 D、营养强化剂——酱油中加铁、粮食制品中加赖氨酸