相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、某原电池的总反应为 , 该原电池的正确组成是( )A、
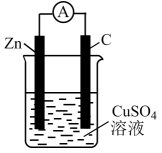 B、
B、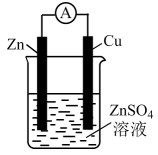 C、
C、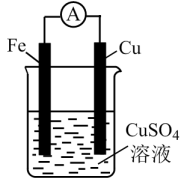 D、
D、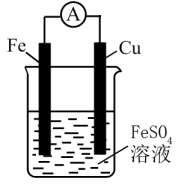
-
2、下列实验设计能达到相应实验目的的是( )
选项
A
B
C
D
实验设计
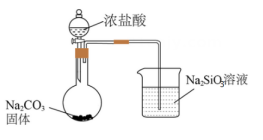
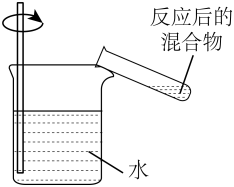
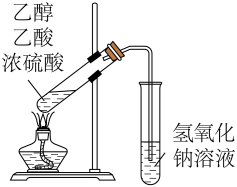
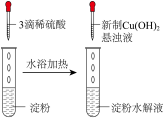
实验目的
比较HCl、H2CO3和H2SiO4的酸性强弱
检验浓硫酸与铜反应后的混合物中是否含有Cu2+
制取乙酸乙酯
验证淀粉在酸性条件下的水解产物
A、A B、B C、C D、D -
3、干洗衣服的干洗剂主要成分是四氯乙烯,家用不粘锅内侧涂覆物质的主要成分是聚四氟乙烯(
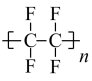 )。下列关于四氯乙烯和聚四氟乙烯的说法正确的是( ) A、均为纯净物 B、都能发生加成反应,都能使酸性高锰酸钾溶液褪色 C、都属于不饱和烃,分子中都不含氢原子 D、四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较稳定
)。下列关于四氯乙烯和聚四氟乙烯的说法正确的是( ) A、均为纯净物 B、都能发生加成反应,都能使酸性高锰酸钾溶液褪色 C、都属于不饱和烃,分子中都不含氢原子 D、四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较稳定 -
4、下列关于含硅物质的说法正确的是( )A、由于单质硅具有良好的半导体性能,所以常用作光导纤维 B、由于SiO2为酸性氧化物,所以不能与任何酸发生反应 C、盛放NaOH溶液不能使用玻璃瓶,是因为SiO2与NaOH溶液反应生成黏性的Na2SiO3 D、硅酸盐材料大多化学性质稳定,是因为其结构中含有硅氧四面体
-
5、某有机物的结构简式如图所示,下列说法错误的是( )
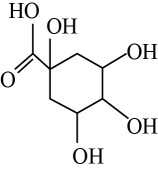 A、分子中有2种官能团 B、既是乙醇的同系物,也是乙酸的同系物 C、与
A、分子中有2种官能团 B、既是乙醇的同系物,也是乙酸的同系物 C、与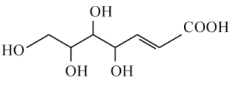 互为同分异构体
D、该物质最多能与发生反应
互为同分异构体
D、该物质最多能与发生反应
-
6、从海带提取碘的实验中,各步选用的实验用品不必都用到的是( )
选项
实验步骤
实验用品
A
步骤1:将海带灼烧灰化
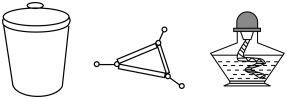
B
步骤2:将海带灰溶解、过滤
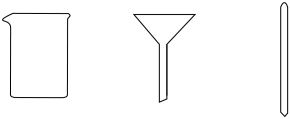
C
步骤3:氧化滤液中的I—
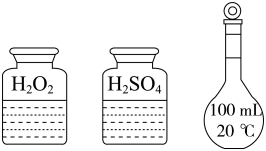
D
步骤4:检验碘单质
 A、A B、B C、C D、D
A、A B、B C、C D、D -
7、烷烃及卤代烃是重要的有机化工原料,下列有关说法正确的是( )A、一氯丁烷有3种不同的结构 B、甲烷可与氯水在光照条件下发生取代反应 C、
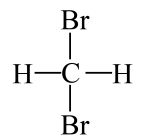 和
和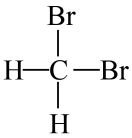 互为同分异构体
D、乙烷分子中最多有4个原子共平面
互为同分异构体
D、乙烷分子中最多有4个原子共平面
-
8、下列关于硫酸及硫酸盐的说法错误的是( )A、重晶石的主要成分为BaSO4 , 医疗上常用做“钡餐” B、检验浓硫酸与木炭反应的全部气体产物,可依次通过无水CuSO4、品红溶液和澄清石灰水 C、胆矾与石灰乳混合可配制农药波尔多液 D、收集的硫酸型酸雨久置后pH减小
-
9、下列关于化学反应中的能量变化说法正确的是( )A、需要加热才能发生的反应一定是吸热反应 B、化学反应不一定伴随能量变化 C、金刚石转化为石墨是放热反应,说明金刚石比石墨稳定 D、燃烧反应、酸碱中和反应是常见的放热反应
-
10、下列化学用语表达错误的是( )A、烯烃官能团的结构式:
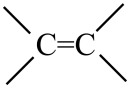 B、醛基的电子式:
B、醛基的电子式: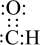 C、溴乙烷的空间填充模型:
C、溴乙烷的空间填充模型: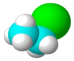 D、聚丙烯的链节:
D、聚丙烯的链节: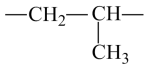
-
11、生活中的一些问题常常涉及化学知识。下列说法错误的是( )A、豆浆中加入石膏,能使豆浆聚沉为豆腐 B、利用液态植物油与氢气发生的加成反应可制造人造奶油 C、加酶洗衣粉(添加少量蛋白酶),不能用来洗涤羊毛织品 D、糯米中的淀粉一经水解就酿成酒
-
12、航天服的材料主要是由碳化硅和其它材料复合而成。下列有关说法正确的是( )A、航天服中使用的棉针织品、羊毛、氯丁橡胶等都属于天然高分子材料 B、碳化硅是一种高熔点、电绝缘性良好的传统无机非金属材料 C、航天服使用硫化橡胶,橡胶硫化的过程发生了化学变化 D、航天服中使用的棉花、合成纤维的主要成分均为纤维素
-
13、为治理雾霾天气,可采用多种方法实现工业废气脱硫。(1)、Ⅰ.软锰矿浆(主要成分 , 含有少量铁、铝等氧化物)可脱除燃煤烟气中的 , 又可制得电池材料。主要流程如图:
提高烟气吸收效率的可行措施有(写出两点)。 (2)、写出“沉锰”步骤发生反应的离子方程式:。(3)、现将该烟气以的流量通入到装有的溶液的装置中,后,恰好完全反应。计算该烟气中含量:。(4)、II.活性是一种固体脱硫剂(无水无脱硫作用),其原理是将废气中的含硫化合物化学吸附到脱硫剂的孔隙中,发生反应改变其化学组成。利用活性脱除沼气中的可转化成。
(2)、写出“沉锰”步骤发生反应的离子方程式:。(3)、现将该烟气以的流量通入到装有的溶液的装置中,后,恰好完全反应。计算该烟气中含量:。(4)、II.活性是一种固体脱硫剂(无水无脱硫作用),其原理是将废气中的含硫化合物化学吸附到脱硫剂的孔隙中,发生反应改变其化学组成。利用活性脱除沼气中的可转化成。
“脱除沼气中”反应的化学方程式为。(5)、工业上要求脱除过程温度不能超过 , 原因是。(6)、Ⅲ.有人设想利用电化学原理除去 , 并将化学能转化为电能。装置图如下。
电池的正极是。(填“a”或“b”)(7)、写出a电极的电极反应。 -
14、A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,E是具有香味的无色透明油状液体。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
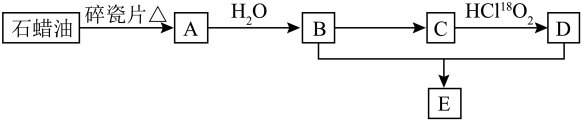
已知:
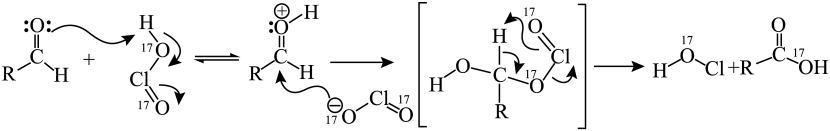 (1)、回答下列问题。
(1)、回答下列问题。①的反应类型是;
②A、D中官能团的名称分别是、;
③E的名称是。
(2)、下列关于有机物A、B、C、D、E的说法正确的。①通过煤的干馏可以得到A
②医疗上常用(体积分数)的B溶液做消毒剂
③由C的官能团预测:C可能与新制的氢氧化铜反应,生成砖红色的氧化铜沉淀
④当温度低于D的熔点时,D可凝结成类似冰一样的晶体
⑤E的密度大于水
(3)、根据已知信息,写出反应的化学方程式:。(4)、丁烷是由石蜡油获得A的过程中的中间产物之一,它的一氯代物同分异构体有种。写出其中含有三个甲基的有机物结构简式:。(5)、三名科学家因在有机合成的复分解反应研究方面做出重大贡献而获得诺贝尔化学奖。一种利用该类型反应生产乙烯的合成路线如下图所示。
①步骤Ⅰ~Ⅳ中属于加成反应的是(填序号)
②写出上述合成路线的总反应方程式:。
-
15、图表蕴含大量的信息,是分析解决化学问题的重要工具。(1)、I.结合下图回答问题
图中三种分子最稳定的是(填化学式)。 (2)、若反应生成气体(选“吸收”或“放出”)kJ热量。(3)、Ⅱ.某温度时,在一个的密闭容器中,A、B、C三种气体的浓度随时间的变化曲线如下图所示。根据图中数据,回答下列问题:
(2)、若反应生成气体(选“吸收”或“放出”)kJ热量。(3)、Ⅱ.某温度时,在一个的密闭容器中,A、B、C三种气体的浓度随时间的变化曲线如下图所示。根据图中数据,回答下列问题:
该反应的化学方程式为;(4)、从开始至 , B的平均反应速率为;平衡时,C的物质的量为;(5)、Ⅲ.已知:“零级反应”是指反应速率与反应物浓度无关的化学反应。某温度下,在恒容密闭容器中发生反应 , 有关数据如下表:
下列说法正确的是。时间段 产物Z的平均生成速率 0~2 0.20 0~4 0.15 0~6 0.10 ①时,Z的浓度可能等于
②时,可逆反应可能建立平衡状态
③时,无论反应是否为零级反应,Y的体积分数一定约为
④时,无论反应是否为零级反应,可逆反应都不可能建立平衡状态
⑤时,X的物质的量为
⑥时,可逆反应可能刚刚建立平衡状态
-
16、某化学学习小组探究浓度对硝酸氧化能力的影响。(1)、Ⅰ.资料显示:浓硝酸能将NO氧化成 , 而稀硝酸不能氧化NO;氢氧化钠能吸收 , 但不能吸收NO。该学习小组按如图装置进行验证实验(夹持仪器已略去)。

回答下列问题:
装置a的名称。(2)、写出装置①中反应的离子反应方程式。(3)、写出装置②中反应的化学反应方程式。(4)、①~⑥装置中,没有发生氧化还原反应的是。(填装置序号)(5)、下列说法正确的是。A.能证明氧化性的相对强弱的实验现象为③中溶液上方出现红棕色气体
B.②中的试剂为水
C.滴加浓硝酸前要先打开弹簧夹通一段时间氮气
D.⑥的作用是吸收尾气NO
(6)、Ⅱ.测得铁与不同浓度硝酸反应时各还原产物的物质的量相对含量与硝酸溶液浓度的关系如图所示:
下列说法正确的是____。A、硝酸的浓度越大,其还原产物中高价态的N元素成分越多 B、硝酸与铁反应往往同时生成多种还原产物 C、铁能与大于溶液反应说明不存在“钝化”现象(7)、已知:在上述反应条件下,反应后铁以形式存在于溶液中。当硝酸浓度为时,计算氧化剂与还原剂的物质的量之比为:。 -
17、温度时,向容积为的密闭容器中加入D(足量)和A,发生反应 , 第后 , 温度调整到(忽略调整温度时所用的时间)。测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是( )
0
2.00
1.50
1.25
1.15
1.00
0.95
0.93
A、 , 生成B的平均速率为 B、可以利用混合气的平均相对分子质量不变,判断平衡建立 C、由表中数据可知 D、若在恒容绝热装置中进行上述反应,可以利用装置压强不变判断平衡建立 -
18、在Pd催化剂表面脱氢的反应历程与能量的关系如图所示。下列说法不正确的( )
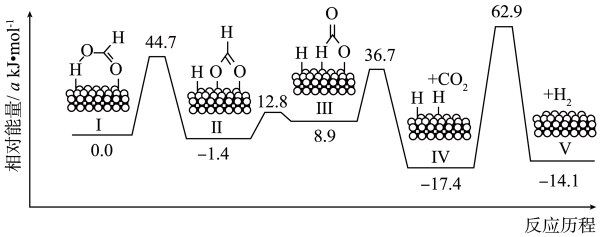 A、分解生成和放出热量 B、由图可知:相同微粒被Pd催化剂吸附后形成的体系,可能具有不同的能量 C、用或代替 , 得到的产物都有HD和 D、由反应历程预测:在Pd表面积一定时,当达到一定值时,再增大可能对反应速率没有影响
A、分解生成和放出热量 B、由图可知:相同微粒被Pd催化剂吸附后形成的体系,可能具有不同的能量 C、用或代替 , 得到的产物都有HD和 D、由反应历程预测:在Pd表面积一定时,当达到一定值时,再增大可能对反应速率没有影响 -
19、我国科研人员研制出“”电池。以钠箔和多壁碳纳米管(MWCNT)为电极材料,放电时总反应的化学方程式为:。其工作原理如图所示,下列说法不正确的是( )
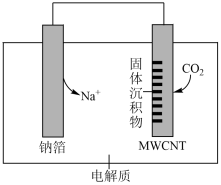 A、放电时,电子流向为:钠箔导线 B、放电时,向正极移动 C、放电时,正极的电极反应式为 D、该电池可用溶液做电解质
A、放电时,电子流向为:钠箔导线 B、放电时,向正极移动 C、放电时,正极的电极反应式为 D、该电池可用溶液做电解质 -
20、按照自左向右的顺序连接实验仪器,能证明亚硫酸的酸性强于次氯酸的是( )
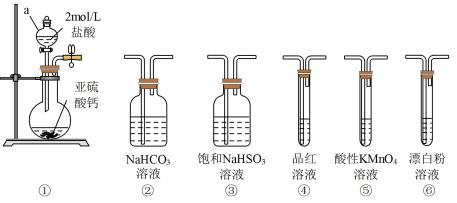 A、①③②⑤④⑥ B、①③⑥⑤④ C、①②③⑥④⑤ D、①②⑥⑤④
A、①③②⑤④⑥ B、①③⑥⑤④ C、①②③⑥④⑤ D、①②⑥⑤④