相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列事实不能用勒夏特列原理解释的是( )A、新制氯水久置后酸性增强 B、压缩装有气体的注射器,气体颜色加深 C、生产硫酸中使用过量的空气来提高的转化率 D、工业上通常在的压强下生产
-
2、下列两组热化学方程式中,有关的比较正确的是( )
;
;
A、; B、; C、; D、; -
3、氨水溶液中存在如下电离平衡: , 下列叙述正确的是( )A、加入少量水,电离平衡正向移动,溶液中增大 B、加入少量浓盐酸,电离平衡正向移动,溶液中增大 C、加入少量浓溶液,电离平衡正向移动,溶液中增大 D、加入少量固体,电离平衡逆向移动,溶液中减少
-
4、下列说法中正确的是( )A、凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 B、自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 C、熵增加且放热的反应一定是自发反应 D、非自发反应在任何条件下都不能发生
-
5、加热到 , 不考虑水挥发,下列溶液的变大的是( )A、溶液 B、溶液 C、硫酸溶液 D、的溶液
-
6、下列仪器常用于量取一定体积液体的是( )A、
 B、
B、 C、
C、 D、
D、
-
7、下列各项中电解质的电离方程式正确的是( )A、熔融态的: B、的水溶液: C、的水溶液: D、熔融态的:
-
8、下列反应既属于氧化还原反应,又属于放热反应的是( )A、灼热的木炭与反应 B、铝热反应 C、氢氧化钠溶液与稀硫酸反应 D、溶于水
-
9、下列物质的水溶液因水解而呈酸性的是( )A、 B、 C、 D、
-
10、下列物质属于非电解质,但溶于水后水溶液可以导电的是( )A、 B、冰醋酸 C、氢氧化钠 D、乙醇
-
11、一氧化二氯()是国际公认的高效安全灭菌消毒剂,其部分性质如下:现用如图所示装置制备少量.
已知:常温下,是棕黄色、有刺激性气味的气体,易溶于水;熔点:-120.6℃;沸点2.0℃.
 (1)、盛有浓盐酸的仪器的名称是.(2)、装置A中发生反应的离子方程式为.(3)、装置B中的试剂是(填名称).(4)、装置C中固体产物为和 , 写出该反应的化学方程式.(5)、装置E中的收率与装置C的温度和纯碱的含水量的关系如表1所示,下列猜想明显不合理的是.
(1)、盛有浓盐酸的仪器的名称是.(2)、装置A中发生反应的离子方程式为.(3)、装置B中的试剂是(填名称).(4)、装置C中固体产物为和 , 写出该反应的化学方程式.(5)、装置E中的收率与装置C的温度和纯碱的含水量的关系如表1所示,下列猜想明显不合理的是.A.温度越高,的收率越低
B.纯碱含水量越高,的收率越高
C.随着纯碱含水量增大,的收率先增大后减小
D.温度较低时,纯碱含水量越高,的收率越高,温度较高时,纯碱含水量越高,的收率越低
温度/℃
纯碱含水量/%
收率/%
0~10
5.44
67.85
0~10
7.88
89.26
10~20
8.00
64.24
30~40
10.25
52.63
30~40
12.50
30.38
表1
已知潮湿的碳酸钠中含碳酸钠的物质的量为0.2mol,实验中得到的质量为5.6g,计算该实验的产率为%(保留三位有效数字)
(6)、若C中盛装含水碳酸钠(与水按照质量调制而成)吸收氯气制备.如果用表示含水碳酸钠,则x为.(7)、请设计实验,检验G溶液中是否含有. -
12、高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理.工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:.回答下列问题:(1)、用氯气制备的反应原理为(化学方程式)(2)、制备高铁酸钠的反应中体现了(填“还原性”、“氧化性”或“氧化性和还原性”)(3)、该反应的离子方程式为.(4)、中Fe的价态为价,可用于自来水杀菌消毒的原因是.(5)、该反应中,每消耗 , 生成的物质的量mol,转移的电子数目为(用表示阿伏加德罗常数的值)
-
13、一定物质的量浓度溶液的配制在生产与科学研究中有着广泛的应用.(1)、容量瓶是配制溶液所用的主要仪器.容量瓶上需标有(填序号).
①温度②浓度③容量④压强⑤刻度线⑥酸式或碱式
下列关于容量瓶操作的说法中,正确的是(填序号).
A.如果检漏时发现漏水,应当用滤纸吸干后再使用
B.定容时,慢慢将蒸馏水倒至凹液面最低处与刻度线相平
C.查漏时,应将活塞旋转180°再次检验是否漏水
D.定容摇匀后,若发现液面变低,应补加蒸馏水至刻度线
(2)、“84消毒液”是生活中常用的杀菌消毒剂.已知某“84消毒液”瓶体标签部分内容如图所示.则该“84消毒液”有效成分的物质的量浓度为.写出其有效成分在水中的电离方程式:.现欲用固体配制80mL上述消毒溶液,除了烧杯、玻璃棒外,还必需的玻璃仪器有 , 需要称量固体g. (3)、下图是配制溶液的几个关键实验步骤的操作.
(3)、下图是配制溶液的几个关键实验步骤的操作.
将上述实验步骤A~F按实验过程先后次序排列.
(4)、若所配制的次氯酸钠溶液浓度偏低,原因可能是____(填序号).A、配制前,容量瓶中有少量蒸馏水 B、固体溶解后将溶液立即转移到容量瓶中 C、定容时水多、超过刻度线,用胶头滴管吸出 D、定容时,俯视溶液的凹液面(5)、次氯酸钠生成器是一种新型的消毒设备,通过直接电解2.5%~3.0%食盐水生成次氯酸钠,则其反应原理为:(用化学方程式表示). -
14、某兴趣小组设计如图所示实验装置,验证Na与能否发生反应.已知能被CO还原得到黑色的金属Pd.请回答下列问题:
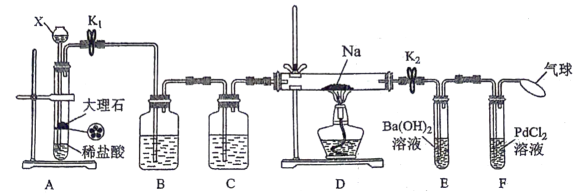 (1)、猜想:Na与能发生反应.理论依据是.(2)、装置B中的试剂是 , C装置的作用是.(3)、将样品装入硬质玻璃管中,再按如下顺序进行实验操作.
(1)、猜想:Na与能发生反应.理论依据是.(2)、装置B中的试剂是 , C装置的作用是.(3)、将样品装入硬质玻璃管中,再按如下顺序进行实验操作.①打开和 , 通入待E中出现时,再点燃酒精灯,此操作的目的是;②熄灭酒精灯;③冷却到室温;④关闭和.
(4)、加热D装置中硬质玻璃管一段时间,观察到以下现象:①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生.
③F中试管内壁有黑色固体生成
实验探究Ⅰ:探究硬质玻璃管中固体产物中钠元素的存在形式
假设一:白色固体是;假设二:白色固体是;假设三:白色固体是和的混合物.请完成下列实验设计,验证上述假设;
步骤1:将硬质玻璃管中的固体产物溶于水后,过滤;
步骤2:往步骤1所得滤液中加入足量的溶液产生白色沉淀,过滤;
步骤3:往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色.
结论:假设一成立.
实验探究Ⅱ:钠与二氧化碳反应产物中碳元素的存在形式.
实验说明:钠与二氧化碳反应的产物中除了碳酸钠以外,还有存在(填化学式)
-
15、用图1所示装置向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示.下列说法正确的是( )
 A、阶段①说明氯气溶于水,溶于水的氯气全部与水反应 B、阶段②的压强变小,可利用该过程发生的反应制备漂白粉 C、阶段③发生反应的离子方程式为 D、若将换成 , 则压强变化不会出现图2趋势
A、阶段①说明氯气溶于水,溶于水的氯气全部与水反应 B、阶段②的压强变小,可利用该过程发生的反应制备漂白粉 C、阶段③发生反应的离子方程式为 D、若将换成 , 则压强变化不会出现图2趋势 -
16、四氯化钛极易水解,遇空气中的水蒸汽即产生“白烟”,常用作烟幕弹.其熔点-25℃,沸点136.4℃.某实验小组设计如下装置(部分加热和夹持装置省略),用与炭粉、制备.下列说法正确的是( )
 A、产品最后在装置④中收集 B、②中应盛装饱和氯化钠溶液 C、反应时应先在③处加热,再开始①处的加热 D、该实验设计存在不足,应在⑤后连接装有碱石灰的干燥管,防止空气中的水蒸气进入反应装置
A、产品最后在装置④中收集 B、②中应盛装饱和氯化钠溶液 C、反应时应先在③处加热,再开始①处的加热 D、该实验设计存在不足,应在⑤后连接装有碱石灰的干燥管,防止空气中的水蒸气进入反应装置 -
17、易发生分解反应生成和.若受热分解恢复到室温后气体产物(简称a)质量为44g,下列说法错误的是( )A、a中两种气体的体积比(同温同压)为1:1 B、a的密度为 C、a中两种气体的质量比为44:17 D、a的平均摩尔质量为
-
18、湿润的土壤中,氮元素的转化过程如下图所示.下列说法正确的是( )
 A、上述转化环境为酸性环境 B、过程Ⅰ可说明在该条件下的氧化性弱于 C、过程Ⅱ中为还原产物 D、上述过程中,与恰好完全反应的物质的量之比为
A、上述转化环境为酸性环境 B、过程Ⅰ可说明在该条件下的氧化性弱于 C、过程Ⅱ中为还原产物 D、上述过程中,与恰好完全反应的物质的量之比为 -
19、为探究物质的氧化性,某实验小组设计如图实验,在实验过程中,观察到氯化亚铁溶液变黄,四氯化碳溶液变为紫红色.下列说法错误的是(已知:碘单质易溶于四氯化碳,可得到紫红色溶液)( )
 A、烧瓶中的反应为: B、浸有溶液的棉花起吸收尾气的作用 C、可用淀粉溶液替换 D、试管下层出现紫红色,可证明氧化性:
A、烧瓶中的反应为: B、浸有溶液的棉花起吸收尾气的作用 C、可用淀粉溶液替换 D、试管下层出现紫红色,可证明氧化性: -
20、某混合溶液中含有的离子种类及其浓度(不考虑水的电离)如表所示:( )
所含离子
M
浓度(mol/L)
4
2
c
6
A、若M为 , 则 B、若c为6,M可能为 C、M可能为 D、加入氢氧化钠溶液后,可能生成沉淀