相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、(1)、Ⅰ.氨气是一种重要的工业原料。
氨气的制备
①氨气的发生装置可以选择上图中的 , 反应的化学方程式为。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→(按气流方向,用小写字母表示)。
③新制的氨水中含氮元素的微粒有3种:、和 , 试用合理的方程式解释:。
(2)、设计实验,探究对稀氨水中存在的溶质的电离平衡的影响。已知:影响电离平衡的因素有浓度、温度等。
①限制试剂与仪器:0.1mol/L氨水、、、、、量筒、烧杯、玻璃棒、药匙、天平、pH计、恒温水浴槽(可控制温度)。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量,数据用字母表示)。
物理量
实验序号V(0.1mol/L氨水)/mL m(铵盐)/g t/℃ 1 100 0 25 b 2 100 a 25 c ③表中物理量“m(铵盐)/g”的铵盐是(填字母)。
A. B. C. D.
(已知25℃几种弱电解质的电离常数分别为: 、醋酸、碳酸和)
④按实验序号2所拟数据进行实验,则一水合氨的电离度(平衡转化率)为。(可忽略水的电离)
-
2、中国科学院研究团队在碱性锌铁液流二次电池电池研究方面取得新进展。下列叙述不正确的是( )
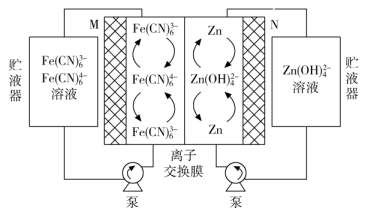 A、充电时,电极M与电源正极相连 B、充电时,阳极的电极反应式为Fe(CN)64--e-=Fe(CN)63- C、放电时,电极N发生氧化反应 D、放电时,电路中转移2 mol电子时,负极区电解质溶液增重65g
A、充电时,电极M与电源正极相连 B、充电时,阳极的电极反应式为Fe(CN)64--e-=Fe(CN)63- C、放电时,电极N发生氧化反应 D、放电时,电路中转移2 mol电子时,负极区电解质溶液增重65g -
3、部分含氮、硫元素的化合物的价-类二维图如图所示。下列关于各物质的说法正确的是。( )
 A、i在一定条件下均可以与a、b、c发生反应 B、e的浓溶液可用于干燥c、f、g C、实验室中产生的g可用NaOH溶液吸收 D、b在纯氧气中点燃可生成d
A、i在一定条件下均可以与a、b、c发生反应 B、e的浓溶液可用于干燥c、f、g C、实验室中产生的g可用NaOH溶液吸收 D、b在纯氧气中点燃可生成d -
4、物质X能发生如下反应:①X→mY;②X→nZ(m、n均为正整数)。恒容体系中X、Y、Z的浓度c随时间t的变化曲线如图所示,下列说法不正确的是( )
 A、m=n=1 B、t1时,c(X)=c(Y) C、反应的活化能:①<② D、t2时,X的消耗速率等于Z的生成速率
A、m=n=1 B、t1时,c(X)=c(Y) C、反应的活化能:①<② D、t2时,X的消耗速率等于Z的生成速率 -
5、对浓盐酸与高锰酸钾反应产生的气体进行如下图所示的探究实验,下列分析正确的是( )
 A、a处酚酞褪色,说明了氯气有漂白性 B、b处湿润的红布条褪色,说明氯气有漂白性 C、c湿润的蓝色石蕊试纸先变红后褪色,说明氯气与水生成了酸性物质和漂白性物质 D、d处溶液变成橙黄色、e处试纸变成蓝色,说明氧化性:
A、a处酚酞褪色,说明了氯气有漂白性 B、b处湿润的红布条褪色,说明氯气有漂白性 C、c湿润的蓝色石蕊试纸先变红后褪色,说明氯气与水生成了酸性物质和漂白性物质 D、d处溶液变成橙黄色、e处试纸变成蓝色,说明氧化性: -
6、甲到丁均为短周期元素,在元素周期表中的相对位置如图所示。丙的单质是空气中主要组成成分之一。下列说法不正确的是( )
 A、原子半径:甲>乙 B、丁的氢化物水溶液可能用于雕刻玻璃 C、丙的简单液态氢化物之间一定存在氢键 D、甲的最高价氧化物一定可以与水反应生成对应的酸
A、原子半径:甲>乙 B、丁的氢化物水溶液可能用于雕刻玻璃 C、丙的简单液态氢化物之间一定存在氢键 D、甲的最高价氧化物一定可以与水反应生成对应的酸 -
7、下列实验中,所采取的分离方法或对应原理不正确的是( )
选项
目的
分离方法
原理
A
除去淀粉胶体中的NaCl
过滤
淀粉胶体不能透过滤纸,NaCl则可以透过
B
除去中的HCl
洗气
在饱和食盐水中的溶解度很小而HCl易溶
C
除去粗苯甲酸晶体中的沙子
重结晶
苯甲酸的溶解度受温度影响较大,沙子在水中溶解度小
D
分离食用油和汽油
蒸馏
食用油和汽油的沸点不同
A、A B、B C、C D、D -
8、下列有关物质结构与性质的说法正确的是( )
 A、基态碳原子价电子排布图:
A、基态碳原子价电子排布图: B、CO32-的空间结构:平面三角形
C、C60和高温高压下可转变为结构类似金刚石的碳玻璃,该碳玻璃中碳原子为杂化
D、硫单质和氢气低温高压下可形成一种新型超导材料,其晶胞如右上图,该晶体属分子晶体
B、CO32-的空间结构:平面三角形
C、C60和高温高压下可转变为结构类似金刚石的碳玻璃,该碳玻璃中碳原子为杂化
D、硫单质和氢气低温高压下可形成一种新型超导材料,其晶胞如右上图,该晶体属分子晶体
-
9、把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中,经过一段时间后,下列说法中正确的是(提示:Fe2+遇K3[Fe(CN)6]产生蓝色沉淀)( )
 A、Ⅰ附近产生黄绿色气体 B、Ⅱ附近铁受保护而几乎不被腐蚀 C、Ⅲ附近开始时无明显现象 D、Ⅳ附近很快出现蓝色沉淀
A、Ⅰ附近产生黄绿色气体 B、Ⅱ附近铁受保护而几乎不被腐蚀 C、Ⅲ附近开始时无明显现象 D、Ⅳ附近很快出现蓝色沉淀 -
10、宏观辨识与微观探析是化学学科核心素养之一。下列性质实验对应的离子方程式书写正确的是( )A、往饱和NaCl溶液中先通氨气,再通入过量的CO2:NH3+ CO2 + H2O = HCO3- + NH4+ B、往NaClO溶液中通入过量SO2:SO2 + ClO- + H2O = SO42- + 2H+ +Cl- C、把足量醋酸加入Na2CO3溶液中:CO32- + 2H+ = CO2↑ + H2O D、过量铁粉加入稀硝酸中:
-
11、下列实验装置不能达到实验目的的是( )
 A、图Ⅰ:由海水制取蒸馏水 B、图Ⅱ:验证NH3易溶于水 C、图Ⅲ:将红热的Pt丝伸入盛有浓氨水的锥形瓶中,瓶口可观察到的白烟是NH4NO3 D、图Ⅳ:用SO2做喷泉实验
A、图Ⅰ:由海水制取蒸馏水 B、图Ⅱ:验证NH3易溶于水 C、图Ⅲ:将红热的Pt丝伸入盛有浓氨水的锥形瓶中,瓶口可观察到的白烟是NH4NO3 D、图Ⅳ:用SO2做喷泉实验 -
12、劳动是幸福的源泉,下列劳动项日与所述的化学知识没有关联的是( )
选项
劳动项目
化学知识
A
社区消毒:向不同区域喷洒“84”消毒液消毒
NaClO具有强氧化性
B
生产活动:葡萄酒中添加适量SO2
SO2可以漂白,防氧化
C
日常防火:用水玻璃浸泡木材或纺织品防火
Na2SiO3水溶液阻燃、耐高温
D
医疗健康:医生用氢氧化铝给病人治疗胃酸过多
氢氧化铝能与盐酸反应
A、A B、B C、C D、D -
13、2021年,我国科学家利用为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程中发生反应: , 设为阿伏加德罗常数,下列有关说法正确的是。( )A、17 g H2O2中含有过氧键数目为0.5 NA B、标况下,22.4 L CH3OH中含有的羟基数为NA C、18 g D2O中含有氧原子的数目为1 NA D、1 mol O2参与反应转移电子数为4 NA
-
14、化学在生活生产中应用广泛,下列有关叙述正确的是( )A、钢水注入干燥的模具,是为了防止铁与水蒸气高温下产生H2和Fe2O3 B、利用FeCl3溶液作为“腐蚀液”制作覆铜板电路时发生了置换反应 C、硬铝常用于制造飞机的外壳,利用了合金熔点比任一组成金属低的特点 D、过氧化钠可在呼吸面具或潜水艇中作为氧气的来源
-
15、我国近年取得了很多世界瞩目的科技成果,化学发挥了重要作用,下列正确的是( )A、神舟十四号飞船的燃料是偏二甲肼 , 偏二甲肼属于烃类 B、中国天眼FAST用到的高性能碳化硅属于新型无机非金属材料 C、2022年10月19日,中国“人造太阳”取得突破性进展,技术水平处于世界前列,反应堆中使用的、互为同位素,其物理性质和化学性质均相同 D、我国最新研发的航空发动机使用了含铼(Re)合金材料,合金是纯净物
-
16、世界文明史上,中华文化是世界上唯一从未间断的文明,始终显示出顽强的生命力和无穷的魅力。
下列文物主要由硅酸盐材料制成的是( )




A.东汉青铜奔马“马踏飞燕”
B.唐代“鎏金舞马衔杯纹银壶”
C.秦“兵马俑”
D.仅49 g的西汉“直裾素纱禅衣”
A、A B、B C、C D、D -
17、抗帕金森病药物恩他卡朋的一种合成路线如下(部分反应条件已省略):

已知:
(Ⅰ)R1-OHR1-X;
(Ⅱ)R2COOHR2-COX;
(Ⅲ)R-COXR3-CONH2
请回答:
(1)、恩他卡朋含氧官能团的名称是。(2)、化合物J的结构简式是。(3)、下列有关说法不正确的是____。A、恩他卡朋的分子式是C14H14N2O5 B、反应①②③④⑤涉及取代、氧化、加成等反应类型 C、化合物D与足量H2充分还原后的产物中共含3个手性碳原子 D、工业上在低温、CH2Cl2溶剂条件下实现D→E转化主要为了调控反应的速率(4)、写出反应⑥的化学方程式。(5)、设计上图中以甲醛(HCHO)为原料制备化合物G的路线 (用流程图表示,无机试剂任选)。(6)、化合物E同时符合以下条件的同分异构体(不包括立体异构体)中,其结构简式除 外还有。
外还有。①只含有一个环的芳香族化合物
②核磁共振氢谱显示共有3组峰,强度比为2:2:3
③分子中不含有亚硝基(-N=O)和酯基
-
18、某化学兴趣小组拟按如下步骤合成铁系催化剂的中间体[Fe(CO)2Cl2]:

其中步骤①实验装置如图所示:

已知:
(I)多聚甲醛为(CH2O)n(n=6~100),当n<12的多聚甲醛可溶于水,当n≥12则不溶于水;加酸或160~200℃加热时会解聚。
(Ⅰ)[Fe(CO)2Cl2]遇氧气、水都会反应,其中Fe的化合价为+2价。
(Ⅱ)SnCl2有强还原性,可被弱氧化剂HgCl2氧化:2HgCl2+SnCl2=Hg2Cl2↓+SnCl4
请回答:
(1)、步骤③产物干燥后仍需放置在干燥器中,以下称为干燥器的是____。A、 B、
B、 C、
C、 D、
D、 (2)、操作步骤②时仍需在氩气氛围下完成,理由是。(3)、写出生成[Fe(CO)2Cl2]的化学反应方程式。(4)、仪器a中盛放的试剂为 , 装置b的作用是。(5)、测定产品纯度时,先称取一定量[Fe(CO)2Cl2],经多步处理并转化为Fe2+后,再用KMnO4标准溶液(用Na2C2O4标准溶液标定)滴定其含量。从下列选项中选出合理的操作并排序: 。
(2)、操作步骤②时仍需在氩气氛围下完成,理由是。(3)、写出生成[Fe(CO)2Cl2]的化学反应方程式。(4)、仪器a中盛放的试剂为 , 装置b的作用是。(5)、测定产品纯度时,先称取一定量[Fe(CO)2Cl2],经多步处理并转化为Fe2+后,再用KMnO4标准溶液(用Na2C2O4标准溶液标定)滴定其含量。从下列选项中选出合理的操作并排序: 。c→→a→→→f
a.将准确称量的[Fe(CO)2Cl2]溶解于水
b.准确称量Na2C2O4并配制一定物质的量浓度的溶液,进行滴定
c.将制备的KMnO4溶液加热煮沸,冷却后滤去MnO2
d.用HgCl2除过量的SnCl2 , 滤去沉淀
e.加入足量SnCl2进行还原
f.用Na2C2O4标准溶液标定后的KMnO4溶液进行滴定
下列情况会导致测量结果偏大的是。
A.[Fe(CO)2Cl2]产品含少量多聚甲醛杂质
B.过量的SnCl2未被除尽
C.[Fe(CO)2Cl2]产品部分氧化或潮解
D.配好的KMnO4标准溶液久置后使用
-
19、研究海洋中珊瑚礁(主要成分CaCO3)的形成机制及其影响具有重要意义,相关主要反应有:
反应Ⅰ:CO2(aq)+H2O(l)(aq)+H+(aq) K1=4.5×10-7
反应Ⅱ:(aq)(aq)+H+(aq) K2= 4.7×10-11
反应Ⅲ:CaCO3(s)Ca2+(aq)+(aq) K3=3.4×10-9
请回答:
(1)、珊瑚礁形成的总反应可表示为Ca2+(aq)+2(aq)=CaCO3(s)+CO2(aq)+H2O(l)。有利于珊瑚礁形成的环境是(填“温暖海域”或“冰冷海域”),该反应的平衡常数K=(用K1、K2、K3表示)。(2)、海水的pH为8.0~8.3,下列有关珊瑚礁形成过程的叙述中正确的是____。A、海水中最主要的含碳微粒为 B、海水中的c(Ca2+)>c()+c() C、、的水解反应是海水呈弱碱性的主要原因 D、珊瑚礁形成的反应阻碍了的电离(3)、温室气体CO2的浓度上升,会导致海水酸化,促使珊瑚礁的溶解。科学家模拟海洋环境探究不同温度下海水中CO2浓度与浓度间的关系。已知T1℃下测得c(CO2)与c()的关系如图,请画出T2℃(T2>T1)时c()随c(CO2)的变化趋势。 (4)、工业上可用(NH4)2CO3溶液捕获CO2以减少其排放:(NH4)2CO3(aq)+H2O(1)+CO2(g)=2NH4HCO3(aq) △H。不同温度下,在同一密闭容器中充入同浓度的CO2 , 加入同浓度同体积的(NH4)2CO3溶液,经相同时间,测得CO2浓度如图,则△H0(填“>”“<”或“=”);随温度的升高,容器中CO2的浓度在T3温度下出现最低值的原因是。
(4)、工业上可用(NH4)2CO3溶液捕获CO2以减少其排放:(NH4)2CO3(aq)+H2O(1)+CO2(g)=2NH4HCO3(aq) △H。不同温度下,在同一密闭容器中充入同浓度的CO2 , 加入同浓度同体积的(NH4)2CO3溶液,经相同时间,测得CO2浓度如图,则△H0(填“>”“<”或“=”);随温度的升高,容器中CO2的浓度在T3温度下出现最低值的原因是。
-
20、亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。

已知:亚硝酰氯有毒,沸点-5.5℃,分子中各原子均满足8电子稳定结构。
请回答:
(1)、NOCl的电子式为 , 化合物X的结构简式为。(2)、下列说法正确的是____。A、NOCl中的氮元素呈正价 B、NOCl分子的空间结构为V形 C、化合物X的沸点低于氯乙酰胺( )
D、工业上可以用蒸馏水吸收多余的NOCl,防止污染环境
(3)、已知浓盐酸和浓硝酸混合配制王水时也会产生亚硝酰氯,写出该反应的化学方程式。(4)、设计实验验证化合物X中含有Cl元素;写出实验过程中涉及的反应方程式。
)
D、工业上可以用蒸馏水吸收多余的NOCl,防止污染环境
(3)、已知浓盐酸和浓硝酸混合配制王水时也会产生亚硝酰氯,写出该反应的化学方程式。(4)、设计实验验证化合物X中含有Cl元素;写出实验过程中涉及的反应方程式。