相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、铜的化合物种类繁多,应用广泛。请回答:(1)、Cu在周期表中的区,当焰色试验时Cu的一个3d轨道电子会跃迁至4p轨道,写出该激发态Cu核外的电子排布式。(2)、[Cu(NH3)4]SO4·H2O是一种农业杀虫剂。
①下列相关说法正确的是。
A.该化合物中NH3的中心原子的杂化轨道类型为sp3
B.该化合物中存在的化学键有离子键、共价键、配位键和氢键
C.组成该化合物的元素N、O、S中,第一电离能最大的是N
D.根据VSEPR模型预测的的空间结构是正四面体形
②比较键角∠H-N-H的大小:NH3[Cu(NH3)]2+(填“>”或“<”),理由是。
(3)、某磷青铜晶体的晶胞结构如图所示,则该晶体中与磷原子距离最近的铜原子共有个,若晶体的密度为g/cm3 , 阿伏加德罗常数的值为NA , 则晶胞的边长a=nm。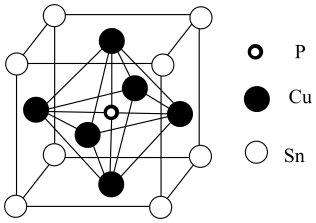
-
2、探究氧族元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是( )
实验方案
现象
结论
A
向H2O2溶液中滴入几滴FeCl3溶液,并在试管口放置带火星的木条
带火星的木条复燃
FeCl3能催化H2O2分解产生O2
B
向滴有酚酞的NaOH溶液中通入SO2
溶液的红色褪去
SO2具有漂白性
C
向盛有少量Na2SO3固体、NaBr固体的两支试管中分别加入等量浓H2SO4
分别产生无色和红棕色的刺激性气味气体
氧化性:Br2>SO2
D
向Na2S溶液中依次加入几滴酸性KMnO4溶液、BaCl2溶液
产生大量白色沉淀
S2-能被氧化为
A、A B、B C、C D、D -
3、已知: , , CuR难溶于水。常温下,Ka1()=1×10-9 , Ka2()=2×10-13 , 当10mL0.1mol/LH2R溶液中缓慢加入少量CuSO4粉末,溶液中c(H+)与(Cu2+)的变化如图所示(忽略溶液的体积变化)。下列有关说法不正确的是( )
 A、X点溶液的pH≈5 B、根据Y点数据可求得Ksp(CuR)=1×10-24 C、Z点溶液中含R微粒的主要存在形式为H2R D、Y点对应的溶液中:c(H+)+2c(Cu2+)=2c(R2-)+c(HR-)+2c()+c(OH-)
A、X点溶液的pH≈5 B、根据Y点数据可求得Ksp(CuR)=1×10-24 C、Z点溶液中含R微粒的主要存在形式为H2R D、Y点对应的溶液中:c(H+)+2c(Cu2+)=2c(R2-)+c(HR-)+2c()+c(OH-) -
4、苯与Br2在一定条件下能发生如下反应,其中部分转化历程与能量变化如图所示:

下列说法不正确的是( )
A、反应焓变:反应Ⅰ>反应Ⅱ B、在该条件下,反应Ⅲ能自发进行 C、苯与Br2主要发生取代反应,生成有机主产物Ⅱ D、选择相对较短的反应时间能有效增加产物Ⅰ的比例 -
5、利用如图装置,工业上燃料燃烧产生的SO2废气可与O2协同转化为重要的化工原料。下列说法不正确的是( )
 A、电极A为负极,X为阴离子交换膜 B、电极B上发生的电极反应为:O2+4e-+4H+=2H2O C、电池工作时,消耗O2、SO2物质的量之比为1:1 D、电池工作段时间后,右室中电解质溶液的pH无明显变化
A、电极A为负极,X为阴离子交换膜 B、电极B上发生的电极反应为:O2+4e-+4H+=2H2O C、电池工作时,消耗O2、SO2物质的量之比为1:1 D、电池工作段时间后,右室中电解质溶液的pH无明显变化 -
6、某学习小组按下图探究金属电化学腐蚀与防护的原理,下列说法正确的是( )
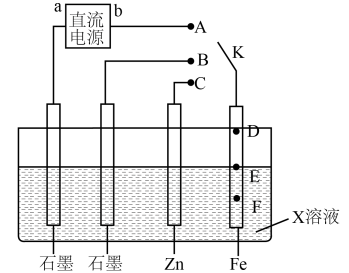 A、若b为正极,K连接A时,铁棒防腐的方式称为牺牲阳极的阴极保护法 B、相同条件下,若X为食盐水,K分别连接B、C时前者铁棒的腐蚀速度更慢 C、若X为模拟海水,K未闭合时铁棒上E点表面铁锈最多,腐蚀最严重的位置则是F D、若在X溶液中预先加入适量的K4[Fe(CN)6]溶液,可有效提升铁棒腐蚀或防腐的观察效果
A、若b为正极,K连接A时,铁棒防腐的方式称为牺牲阳极的阴极保护法 B、相同条件下,若X为食盐水,K分别连接B、C时前者铁棒的腐蚀速度更慢 C、若X为模拟海水,K未闭合时铁棒上E点表面铁锈最多,腐蚀最严重的位置则是F D、若在X溶液中预先加入适量的K4[Fe(CN)6]溶液,可有效提升铁棒腐蚀或防腐的观察效果 -
7、原子序数依次增大的4种短周期主族元素X、Y、Z、M,已知基态X原子含3个未成对电子,Y在同周期元素中的原子半径最小,Z的价层电子只有一种自旋方向,基态M原子s能级上电子总数比p能级少1。下列说法正确的是( )A、元素最高正价:Y>X>M>Z B、简单离子半径:M> Z>X>Y C、第一电离能:X>Y>Z>M D、最简单氢化物的稳定性:Y>X
-
8、奥培米芬是一种雌激素受体调节剂,下列说法正确的是( )
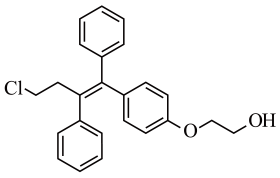 A、属于芳香烃 B、存在3种官能团 C、含有-OH等亲水基团,具有较好的水溶性 D、在KOH醇溶液或浓硫酸中加热均能发生消去反应
A、属于芳香烃 B、存在3种官能团 C、含有-OH等亲水基团,具有较好的水溶性 D、在KOH醇溶液或浓硫酸中加热均能发生消去反应 -
9、下列离子方程式书写正确的是( )A、MgSO4与Ba(OH)2溶液反应:Ba2++=BaSO4↓ B、FeCl3溶液刻蚀电路铜板:2Fe3++3Cu=2Fe+3Cu2+ C、在Ca(HCO3)2溶液中加入过量澄清石灰水:Ca2+++OH-=CaCO3↓+H2O D、向苯酚钠溶液中通入少量CO2:2
 +CO2+H2O→2
+CO2+H2O→2 +
+
-
10、下列说法正确的是( )A、如果苯酚浓溶液沾到皮肤,应立即用酒精洗 B、糖类都能发生水解反应,但各自水解的产物不相同 C、汽油和植物油都属于烃类,所以汽油和植物油都可以燃烧 D、向2mL蛋白质溶液中加入适量饱和硫酸铵溶液,产生沉淀,说明蛋白质发生了变性
-
11、设NA为阿伏加德罗常数的值,下列说法正确的是( )A、1molCH3COOH中含有的σ键数目为8NA B、0.01mol/LBaCl2溶液含有的Ba2+数目为0.01NA C、加热条件下,3.2g铜与足量浓硫酸充分反应生成的SO2分子数目为0.05NA D、0.1molFeCl3加入沸水中充分反应,生成的Fe(OH)3胶体粒子的数目为0.1NA
-
12、硼氢化钾制备纳米铜粉的反应方程式为:Cu2++2+6H2O=Cu+2HBO3+7H2↑,已知反应前后B元素价态不变。下列说法不正确的是( )A、还原剂是KBH4 B、还原产物是H2 C、生成3.2g铜时共转移0.4mol电子 D、若用Ag+替换Cu2+参加反应,可能制得纳米银粉
-
13、下列说法不正确的是( )
 A、图①装置可用于加热分解NaHCO3固体 B、图②装置可通过喷泉现象证明氨气极易溶于水 C、图③装置可用于探究温度对化学平衡移动的影响 D、图④装置可用于测定中和反应的反应热
A、图①装置可用于加热分解NaHCO3固体 B、图②装置可通过喷泉现象证明氨气极易溶于水 C、图③装置可用于探究温度对化学平衡移动的影响 D、图④装置可用于测定中和反应的反应热 -
14、物质的性质决定用途,下列两者对应关系不正确的是( )A、Al(OH)3有弱碱性,可用于治疗胃酸过多 B、生铁硬度大、抗压性强,可用于铸造机器底座 C、稀硝酸有强氧化性,可清洗附着在试管内壁的银镜 D、单晶硅是良好的半导体材料,常用于制备光导纤维
-
15、过氧化钠是一种常用的化工试剂,下列说法不正确的是( )A、过氧化钠属于氧化物 B、过氧化钠可由钠和氧气反应制得 C、过氧化钠可用作呼吸面具中的氧气来源 D、过氧化钠在工业上常用于制备氢氧化钠
-
16、下列化学用语表示正确的是( )A、HClO的结构式:H-Cl-O B、有机物(CH3CH2)2CHCH3的名称:3-甲基戊烷 C、乙二酸的实验式:C2H2O4 D、基态氧原子的轨道表示式:

-
17、电解质对维持人体健康具有诸多作用,下列物质属于电解质的是( )A、SiO2 B、C2H5OH C、KCl D、Cu
-
18、三氧化碳的回收及综合利用越来越受到国际社会的重视,将二氧化碳转化为高附加值化学品是目前研究的热点之一。利用和合成甲醇,在催化剂作用下可发生如下两个平行反应。
反应I:
反应Ⅱ:
请回答:
(1)、有利于提高甲醇平衡产率的条件是____。A、低温低压 B、低温高压 C、高温低压 D、高温高压(2)、反应的(3)、我国科研人员研究了在催化剂上加氢制甲醇过程中水的作用机理,其主反应历程如图(),下列说法正确的是____。 A、使用更高效的催化剂能提高甲醇的平衡产率 B、第④步的反应式为 C、加氢制甲醇符合绿色化学理念 D、若实验前用少量水对催化剂进行预处理,可能提升甲醇产率(4)、在催化剂下,向恒容密闭容器充入一定量及 , 起始和平衡时各组分的量如下:
A、使用更高效的催化剂能提高甲醇的平衡产率 B、第④步的反应式为 C、加氢制甲醇符合绿色化学理念 D、若实验前用少量水对催化剂进行预处理,可能提升甲醇产率(4)、在催化剂下,向恒容密闭容器充入一定量及 , 起始和平衡时各组分的量如下:总压/
起始/
10
3.0
0
0
0
平衡/
p
若反应均达平衡时, , 则表中;若此时 , 则反应I的平衡常数(无需带单位,用含总压p的式子表示)。
(5)、一定比例的合成气在装有催化剂的反应器中反应 , 体系中甲醇的产率和催化剂的催化活性与温度的关系如下图所示,此温度范围内,催化剂活性不受影响
①当温度高于后,甲醇产率减小的原因可能是。
②请在图中画出甲醇平衡产率随温度变化的曲线图。
-
19、工业上纳米的制备过程是以为载体,用和水蒸气反应生成 , 再控制温度生成纳米 , 测定产物组成的方法如下:
步骤一:取样品用稀硫酸充分溶解得到溶液,再用足量铝将还原为 , 过滤并洗涤,将所得滤液和洗涤液混合并注入容量瓶,定容得到待测液。
步骤二:取待测液于锥形瓶中,加入几滴指示剂,用的标准溶液滴定,将氧化为 , 三次滴定测得数据记录如下:
实验编号
待测溶液的体积/mL
滴定前标准液的体积读数/mL
滴定后标准液的体积读数/mL
1
25.00
0.20
24.22
2
25.00
1.21
29.21
3
25.00
150
25.48
回答下列问题:
(1)、若对步骤一所得的溶液加水稀释,溶液中会产生少量偏钛酸沉淀,写出该反应的离子方程式。(2)、上述滴定实验中,可选择为指示剂,判断到达滴定终点的方法是。(3)、下列关于滴定分析的操作,错误的是____。A、滴定时要适当控制滴定速率 B、用量筒量取待测液转移至锥形瓶 C、滴定时应一直观察滴定管中溶液体积的变化 D、平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下 E、在接近终点时,滴加药品应慢慢控制滴定管,使滴定管尖嘴悬挂一滴液体,用锥形瓶内壁将其靠下,并用蒸馏水将其冲入锥形瓶内。(4)、通过分析、计算,该样品的组成为;若滴定前滴定管尖端有气泡,滴定过程中气泡消失,则测得比实际值(填“偏大”、“偏小”或“无影响”)。 -
20、工业合成氨是20世纪的伟大成就之一,但化肥的过度使用、硝酸工业废气和动车尾气的排放,给水体和大气带来了一定程度的污染,需要进行综合处理。(1)、工业合成氨反应为: kJ·mol , 下列说法正确的是____。A、采用高温以提高反应的平衡转化率 B、采用高压以加快反应速率,提高的产量 C、为提高转化率,可适当增大的浓度 D、生产过程中将液化分离,有利于氨的合成(2)、一种电化学合成氨的原理如图所示。产生的电极反应式是。
 (3)、Ⅱ.含氮污染的处理
(3)、Ⅱ.含氮污染的处理水体中氨氮处理:在微生物作用下,废水中经两步反应被氧化成:
kJ·mol
kJ·mol
则全部氧化成的热化学方程式是。
(4)、大气中NO处理:电解NaCl溶液(调节起始pH约为9)获得NaClO溶液,可用于去除大气中NO。其他条件相同,电解所得溶液中相关成分的浓度与电流强度的关系如图所示。
①用电解所得NaClO溶液氧化NO生成和 , 其离子方程式为。
②电流强度大于4A,随着电流强度增大,电解所得溶液对NO去除率下降,其原因是。