相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、雄黄(As4S4)、雌黄(As2S3)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:(1)、基态硫原子核外电子的空间运动状态有种;其核外电子运动最高能级的电子云轮廓图的形状为。(2)、基态砷原子的价层电子的轨道表示式为。(3)、第一电离能AsSe(填“>”或“<”)。(4)、基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是(填元素符号,下同),其价层电子排布式为。该元素处于周期表的区。
-
2、下列实验操作、现象及结论均正确是( )
选项
操作和现象
结论
A
常温下,用pH计分别测定等体积溶液和溶液的pH,pH均为7
两种溶液中水的电离程度相同
B
向2mL的KI溶液中滴加2mL的溶液,充分反应后加入2mL , 取上层溶液滴加KSCN溶液,溶液变红色
与KI的反应存在限度
C
向溶有的的溶液中通入气体X,出现白色沉淀
X具有强氧化性
D
向2mL溶液中滴入3滴NaOH溶液,再滴入4滴溶液,先产生白色沉淀,后产生红褐色沉淀
同温度下的:
A、A B、B C、C D、D -
3、我国科学家研究化合物催化氢化生成甲酸的机理,其中由化合物生成化合物过程的机理和相对能量曲线如下图所示。均为过渡态。下列说法正确的是( )
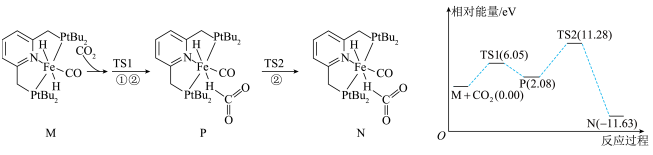 A、过渡态TS1比化合物Р更稳定 B、过程M→P为化合物M生成化合物N的决速步骤 C、化合物M催化氢化生成甲酸的反应过程中一定有键的生成和断裂 D、由生成的热化学方程式:
A、过渡态TS1比化合物Р更稳定 B、过程M→P为化合物M生成化合物N的决速步骤 C、化合物M催化氢化生成甲酸的反应过程中一定有键的生成和断裂 D、由生成的热化学方程式: -
4、已知:T℃时,Ksp(CaSO4)=4.0×10-6、Ksp(CaCO3)=4.0×10-9、Ksp(PbCO3)=8.4×10-14 , 三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子)。下列说法错误的是( )
 A、a线是CaSO4沉淀溶解平衡曲线 B、T℃时,向0.001mol CaCO3沉淀中加入Na2SO4溶液(反应后溶液为1L),使CaCO3沉淀会转化为CaSO4沉淀,所需Na2SO4的物质的量至少为1.001mol C、T℃时,向10mL水中加入CaCO3和PbCO3至二者均饱和,溶液中= D、若d点表示CaCO3的饱和溶液加入CaSO4饱和溶液等体积混合则:c()<c(Ca2+)<c(SO)
A、a线是CaSO4沉淀溶解平衡曲线 B、T℃时,向0.001mol CaCO3沉淀中加入Na2SO4溶液(反应后溶液为1L),使CaCO3沉淀会转化为CaSO4沉淀,所需Na2SO4的物质的量至少为1.001mol C、T℃时,向10mL水中加入CaCO3和PbCO3至二者均饱和,溶液中= D、若d点表示CaCO3的饱和溶液加入CaSO4饱和溶液等体积混合则:c()<c(Ca2+)<c(SO) -
5、“类比”是预测物质性质与化学反应的重要方法之一,但“类比”不能违背客观事实,下列“类比”合理的是( )A、Na2O2与CO2反应生成Na2CO3和O2 , 则Na2O2与SO2反应生成Na2SO3和O2 B、Na在空气中燃烧生成Na2O2 , 则同族的Li在空气中燃烧也生成Li2O2 C、Al(OH)3溶于NaOH溶液生成Na[Al(OH)4],则Be(OH)2也能溶于NaOH溶液生成Na2[Be(OH)4] D、Al3+与S2﹣在水溶液中因水解无法大量共存,则Fe3+与S2﹣在水溶液中也因水解无法大量共存
-
6、NaOH标准溶液的配制和标定,需经过NaOH溶液配制、基准物质的称量以及用NaOH溶液滴定等操作。下列有关说法中正确的是( )
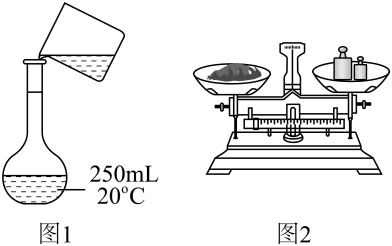
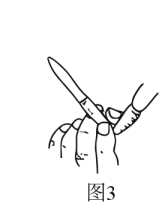
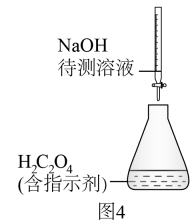 A、用图1所示操作转移NaOH溶液到容量瓶中 B、用图2所示装置准确称得固体 C、用图3所示操作排出碱式滴定管中的气泡 D、用图4所示装置以NaOH待测液滴定
A、用图1所示操作转移NaOH溶液到容量瓶中 B、用图2所示装置准确称得固体 C、用图3所示操作排出碱式滴定管中的气泡 D、用图4所示装置以NaOH待测液滴定 -
7、相同金属在其不同浓度盐溶液中可形成浓差电池。如图所示装置是利用浓差电池电解Na2SO4溶液(a、b电极均为石墨电极),可以制得O2、H2、H2SO4和NaOH.下列说法正确的是( )
 A、电池放电过程中,Cu(2)作正极,电极反应为Cu2++2e-═Cu B、c、d离子交换膜依次为阳离子交换膜和阴离子交换膜 C、b为电解池的阴极,电极反应为2H2O+2e-═H2↑+2OH- D、电池从开始工作到停止放电,电解池理论上可制得80gNaOH
A、电池放电过程中,Cu(2)作正极,电极反应为Cu2++2e-═Cu B、c、d离子交换膜依次为阳离子交换膜和阴离子交换膜 C、b为电解池的阴极,电极反应为2H2O+2e-═H2↑+2OH- D、电池从开始工作到停止放电,电解池理论上可制得80gNaOH -
8、某种离子液体的结构如图所示,X、Y、Z、M、Q为原子序数依次增大的短周期元素,Z的原子序数等于X、Y原子序数之和,Q为非金属性最强的元素。
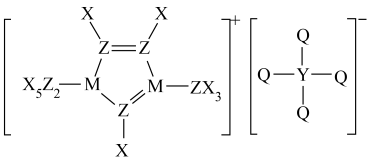
下列说法正确的是( )
A、氢化物的沸点: B、基态原子未成对电子数: C、简单离子半径: D、基态原子第一电离能由大到小的顺序为: -
9、下列说法一定正确的是( )A、25℃时,向溶液中加入的NaOH溶液,当水电离出的时,滴加氢氧化钠溶液的体积可能出现两种情况,则HA为弱酸 B、常温下,将pH=2的一元酸HA溶液与pH=12的一元碱BOH溶液等体积混合,所得溶液pH=7 C、相同温度下,的NaCl溶液和的NaCN溶液中的离子总数相等 D、将冰醋酸加水稀释,冰醋酸的电离度逐渐增加,但电离常数Ka不变,逐渐增大,导电性逐渐增强
-
10、根据杂化轨道理论和价层电子对互斥模型判断,下列说法不正确的是( )
选项
粒子
中心原子杂化方式
VSEPR模型
空间结构
A
直线形
直线形
B
四面体形
三角锥形
C
四面体形
平面三角形
D
四面体形
三角锥形
A、A B、B C、C D、D -
11、下列依据热化学方程式得出的结论正确的是( )A、已知 , 则氢气的燃烧热为 B、在一定温度和压强下,将和置于密闭容器中充分反应生成 , 放出热量19.3kJ,则其热化学方程式为 C、已知酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 D、已知 , 虽然该反应为可逆反应,但该反应的焓变仍可通过一定的实验方法直接测得
-
12、下列说法正确的是( )A、恒温恒容下, , 当混合气体的密度不再发生变化时,能表明该反应达到平衡状态 B、恒温恒容下,达到平衡,移走部分N,平衡向正反应方向移动 C、 , 反应达至平衡后,升温,则反应速率和的平衡转化率均增大 D、实验室制氢气,为了加快反应速率,可在稀硫酸中加少量固体
-
13、下列各组分子或离子中所有原子都可能处于同一平面的是( )A、、、 B、、、 C、、、 D、、、+
-
14、下列有关比较正确的是( )A、熔点: B、熔、沸点:NaBr>NaCl>MgO C、酸性: D、热稳定性:
-
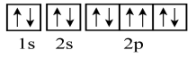
15、下列说法或有关化学用语的表达正确的是( )A、能级能量大小关系: B、基态铜原子(29Cu)的价层电子排布式: C、处于激发态的电子排布式可能为: D、基态的轨道表示式:
-
16、有5种元素X、Y、Z、Q、T。X原子M电子层上p能级有2个未成对电子且无空轨道;Y原子的价层电子排布式为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )A、元素Y和Q可形成化合物Y2Q3 B、简单离子半径:T>X>Q C、的中心原子价层电子对数为3 D、XQ2的空间结构是V形
-
17、下列物质的水溶液在空气中小心加热蒸干至质量不再减少,能得到较纯净的原溶质的是( )
① ② ③ ④ ⑤ ⑥
A、全部 B、仅①② C、仅①⑤ D、仅① -
18、下列离子方程式书写正确的是( )A、NaHCO3溶液的水解: B、向溶液中通入少量SO2: C、向溶液中滴加Na2CO3溶液: D、向CaCl2溶液中通入CO2:
-
19、下列说法错误的是( )A、下列离子在溶液中能大量共存:Al3+、Na+、S2﹣、NO B、为保存FeCl3溶液,要在溶液中加入少量盐酸 C、实验室盛放Na2CO3 , Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞 D、相同浓度的NaX、NaY、NaZ的溶液,其pH依次增大则HX、HY、HZ的酸性依次减弱
-
20、下列生活中常用的方法,其原理与盐类的水解反应有关的是( )A、用草木灰去除油污 B、用氢氢化铝中和过多胃酸 C、用食盐腌制腊肉 D、用白醋清洗水壶中的水垢