相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、含氮族元素的物质种类繁多,应用广泛。回答下列问题:(1)、基态As原子的简化电子排布式为。(2)、下列说法正确的是____。A、基态P原子核外电子的空间运动状态有9种 B、键角大小: C、水溶液中的碱性: D、甘氨酸()可分别与水、乙醇形成分子间氢键,故甘氨酸在水、乙醇中均可溶解(3)、磷酸通过分子间脱水缩合形成多磷酸,如:

如果有n个磷酸分子间脱水形成环状的多磷酸,则该酸的分子式为。
(4)、已知是次磷酸的正盐,的结构式为。(5)、我国科学家制备的超大晶体已应用于大功率固体激光器,填补了国家战略空白。分别用〇、●表示和 , 晶体的四方晶胞(晶胞为长方体)如图(a)所示,图(b)、图(c)分别显示的是、在晶胞xz面、yz面上的位置。
①与紧邻的数目为。
②若晶胞底边的边长均为anm、高为cnm,为阿伏加德罗常数的值,则晶胞的密度(写出表达式)。
-
2、探究硫元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是( )
实验方案
现象
结论
A
将硫黄与浓KOH溶液共热,待固体消失后,加入足量稀硫酸
溶液变浑浊
说明硫黄与碱反应生成硫化物和硫酸盐
B
测定均为离子化合物的和的熔点
的熔点更高
说明中离子键强于
C
向溶有的溶液中加入溶液
产生白色沉淀
说明可将氧化
D
将某固体溶于水,取上层清液,先滴加足量稀盐酸再滴加氯化钡溶液
滴加稀盐酸无明显现象,滴加氯化钡后产生白色沉淀
说明该固体中含有
A、A B、B C、C D、D -
3、向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应和 , 与的关系如下图所示(其中M代表、、或)。下列说法正确的是( )
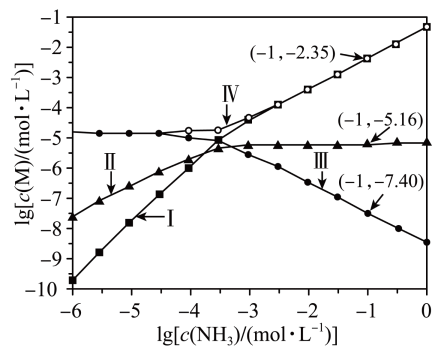 A、时,溶液中 B、曲线IV为随的变化曲线 C、时,溶液中 D、反应的平衡常数K的值为
A、时,溶液中 B、曲线IV为随的变化曲线 C、时,溶液中 D、反应的平衡常数K的值为 -
4、一定条件下,1mol和发生反应时,生成CO、或HCHO的能量变化如图所示[反应物和生成物略去]。下列说法不正确的是( )
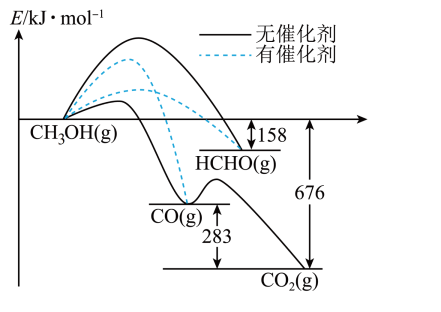 A、有催化剂时,主要产物为HCHO B、无催化剂时,升高温度更有利于提高甲醛的产率 C、该条件下比CO更稳定 D、加入该催化剂能提高图中各反应的速率,但不能改变反应的焓变
A、有催化剂时,主要产物为HCHO B、无催化剂时,升高温度更有利于提高甲醛的产率 C、该条件下比CO更稳定 D、加入该催化剂能提高图中各反应的速率,但不能改变反应的焓变 -
5、现在广泛使用的锂离子电池有多种类型,某可充电钴酸锂电池的工作原理如图所示。下列叙述正确的是( )
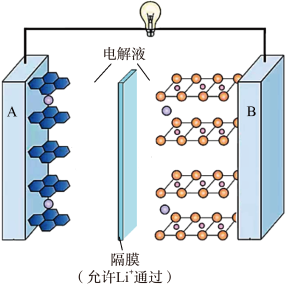 A、该电池放电时,其中正极的电极反应式是 B、充电时A极与电源的正极相连 C、放电时,移向电势较高的电极后得到电子发生还原反应 D、拆解废电池前先进行充电处理既可以保证安全又有利于回收锂
A、该电池放电时,其中正极的电极反应式是 B、充电时A极与电源的正极相连 C、放电时,移向电势较高的电极后得到电子发生还原反应 D、拆解废电池前先进行充电处理既可以保证安全又有利于回收锂 -
6、一水硫酸四氨合铜(Ⅱ)的化学式为是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
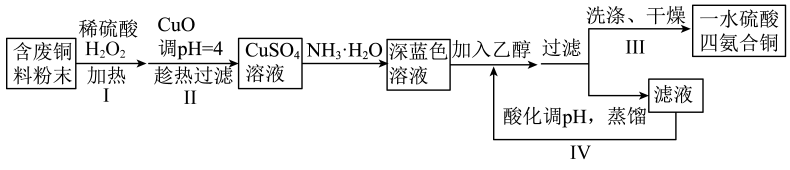
下列说法不正确的是( )
A、操作I中发生的主要反应为: B、操作II中趁热过滤除去的是难溶性杂质和氢氧化铁 C、操作III中洗涤可用乙醇和水的混合液,干燥可采用减压干燥方式 D、设计操作IV的目的是为了提高乙醇的利用率 -
7、X、Y、Z、R、Q是元素周期表中原子序数依次增大的前四周期元素,X是宇宙中含量最多的元素;Y与Z同周期,Y基态原子有3个未成对电子,Z元素原子的价层电子排布为;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法不正确的是( )A、是含有极性键和非极性键的极性分子 B、第一电离能: C、Q在周期表的ds区 D、电负性:
-
8、某药物具有清热解毒功效,其有效成分结构如下。下列有关该物质的说法不正确的是( )
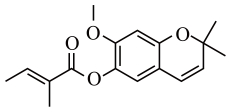 A、所有碳原子不可能处于同一平面上 B、存在顺反异构体 C、与足量充分反应后的产物中共含6个手性碳原子 D、1mol该物质最多可与2molNaOH反应
A、所有碳原子不可能处于同一平面上 B、存在顺反异构体 C、与足量充分反应后的产物中共含6个手性碳原子 D、1mol该物质最多可与2molNaOH反应 -
9、下列离子反应方程式正确的是( )A、硫酸铝铵溶液中加入过量氢氧化钡: B、常温下铁加入过量浓硝酸中: C、澄清石灰水与过量碳酸氢钠溶液混合: D、硫化钠溶液中加入少量氯化铁溶液:
-
10、下列说法不正确的是( )A、蒸馏、萃取、重结晶和色谱法都可用于分离、提纯有机物 B、核苷酸通过缩聚反应可以得到核酸,核酸属于生物大分子 C、根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花 D、糖类都含有醛基,对氢氧化铜等弱氧化剂表现出还原性
-
11、是阿伏加德罗常数的值,下列说法正确的是( )A、1L的溶液中,硫酸根和氢氧根的总数目为 B、标准状况下,11.2L分子所含的原子数为 C、5.8g含有的键数目为 D、向含1mol的水溶液中加入足量充分反应,转移的电子数为
-
12、是一种高效、环保的消毒剂,以下是常见的三种制备方法:
①
②
③
下列说法正确的是( )
A、反应①中发生还原反应 B、上述反应中是氧化剂 C、反应③中HCl既体现酸性,又体现还原性 D、消毒效率是的2.5倍(消毒效率:单位质量的消毒剂得到的电子数) -
13、下列说法正确的是( )
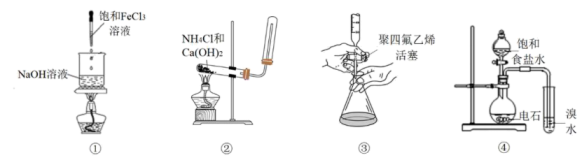 A、图①操作可用于实验室制取少量氢氧化铁胶体 B、图②装置可用于实验室制取并收集氨气 C、图③操作可用于氢氧化钠标准溶液滴定未知浓度的盐酸 D、图④装置可用于实验室制取乙炔并进行性质检验
A、图①操作可用于实验室制取少量氢氧化铁胶体 B、图②装置可用于实验室制取并收集氨气 C、图③操作可用于氢氧化钠标准溶液滴定未知浓度的盐酸 D、图④装置可用于实验室制取乙炔并进行性质检验 -
14、物质的性质决定用途,下列两者对应关系不正确的是( )A、漂白粉具有强氧化性,可用作游泳池等场所的消毒剂 B、纯铝的硬度和强度较小,可用来制造机器零件 C、碱石灰有吸水性,在实验室中常用作干燥剂 D、碳酸钠溶液显碱性,可用作食用碱或工业用碱
-
15、下列说法不正确的是( )A、胆矾可以和石灰乳混合制成农药波尔多液 B、食品中添加适量二氧化硫可以起到漂白、防腐和抗氧化等作用 C、用乙烯和氧气在银催化下制备环氧乙烷是理想的“原子经济性反应” D、不锈钢是最常见的一种合金钢,它的主要元素是铬和镍
-
16、下列化学用语或说法中正确的是( )A、在氨水中,与分子间的氢键主要形式可表示为:
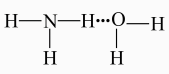 B、B原子由 , 时,由基态转化为激发态,形成吸收光谱
C、的VSEPR模型为
B、B原子由 , 时,由基态转化为激发态,形成吸收光谱
C、的VSEPR模型为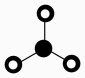 D、1个乙烯分子中有5个“”键和1个“”键
D、1个乙烯分子中有5个“”键和1个“”键
-
17、下列物质中属于新型无机非金属材料的是( )A、碳化硅 B、陶瓷 C、铝合金 D、普通玻璃
-
18、氨溴索(G)是β-内酰胺类的抗生素,可以治疗多种细菌感染。一种合成路线如下:
 (1)、A~C三种物质中(填“有”、“无”)易溶于水的物质。D中氮原子杂化类型为。(2)、
(1)、A~C三种物质中(填“有”、“无”)易溶于水的物质。D中氮原子杂化类型为。(2)、 中的官能团名称是 , 所涉及到的非金属元素第一电离能由大到小顺序为。 (3)、反应③的化学方程式是。(4)、反应⑤的反应类型是。(5)、B的芳香族同分异构体中,满足下列条件的有种;其中核磁共振氢谱有4组吸收峰且峰面积之比为2∶2∶2∶1的结构简式为。
中的官能团名称是 , 所涉及到的非金属元素第一电离能由大到小顺序为。 (3)、反应③的化学方程式是。(4)、反应⑤的反应类型是。(5)、B的芳香族同分异构体中,满足下列条件的有种;其中核磁共振氢谱有4组吸收峰且峰面积之比为2∶2∶2∶1的结构简式为。①能发生银镜反应;②能水解;③1 mol最多能与2 mol NaOH反应;
(6)、写出以 为原料制备
为原料制备 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。 -
19、SO2、CO、NO、NO2及其他氮氧化物都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题。(1)、上述四种气体中直接排入空气时会引起酸雨的有(填化学式)。(2)、回收大气污染物SO2的方法如下:
方法一:在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和液态H2O。已知:
CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(1) △H=-295.9kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-297.2kJ·mol-1
则CH4的燃烧热的热化学方程式为:。
方法二:在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图1所示),该过程中部分物质的物质的量浓度随时间的变化关系如图2所示:

①由分析可知X为(填化学式)。
②0~t1时间段H2的化学反应速率。
方法三:利用反应:NO2(g)+SO2(g)SO3(g)+NO(g)。
③一定条件下,将NO2与SO2以体积比1∶1置于恒温恒容的密闭容器中发生反应:NO2(g)+SO2(g)SO3(g)+NO(g),能说明反应达到平衡状态的是(填字母)。
a. 混合气体的密度保持不变 b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变 d.每生成1molSO3的同时消耗1molNO
e.容器内的混合气体平均相对分子质量保持不变
④已知该反应的平衡常数为 , 向某恒温恒容密闭容器中通入NO2、SO2、SO3、NO各1mol,此时v(正)v(逆)(填“>”、“<”或“=”)。
(3)、在发动机的高温下,空气中的N2和CO2可能发生:N2(g)+CO2(g)C(s)+2NO(g)。现向2L体积恒定的密闭容器中充入一定量N2和CO2来模拟此过程,其中N2、NO物质的量随时间变化的曲线如图所示。①图中A点v正v逆(填“>”“<”或“=”)。

②第10min时,外界改变的条件可能是(填字母)。
A. 加催化剂 B.增大C的物质的量
C.减小CO2的物质的量 D.升温 E.降温
-
20、绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
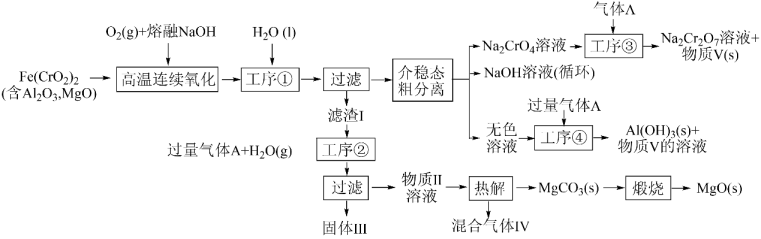
回答下列问题:
(1)、高温连续氧化工序中被氧化的元素是(填元素符号),Cr元素在元素周期表中的位置 ,(2)、滤渣I的主要成分是(填化学式)。(3)、工序③中发生反应的离子方程式为。(4)、物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为。钠在火焰上灼烧产生的黄光是一种(填“吸收光谱” 或“发射光谱”)。(5)、工序④溶液中的铝元素恰好完全转化为沉淀的pH为。(通常认为溶液中离子浓度小于10-5mol•L-1为沉淀完全;Al(OH)3+OH-⇌Al(OH):K=100.63 , Kw=10-14 , Ksp[Al(OH)3]=10-33)(6)、基态Al原子的核外电子排布式为。Fe的晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,若晶胞参数为a nm,则Fe晶胞的密度为g•cm-3(用含NA和a的代数式表示)。