相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列物质属于电解质的是( )A、盐酸 B、干冰 C、胆矾 D、石墨
-
2、以某工业废锰渣(含MnO2及少量KOH、MgO、Fe2O3)为原料制备MnSO4晶体,其工艺流程如下:
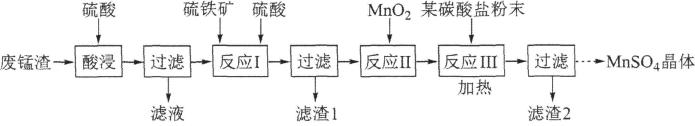
该工艺条件下金属离子开始沉淀和完全沉淀(c≤10-5mol/L)的pH如表所示:
金属离子
Fe3+
Fe2+
Mn2+
Mg2+
开始沉淀pH
2.10
7.45
9.27
9.60
完全沉淀pH
3.20
8.95
10.87
11.13
(1)、“反应I”中加入硫铁矿(主要成分FeS2)将MnO2还原为Mn2+。滤渣1的主要成分除FeS2外,还有一种相对分子质量为192的单质,该物质的化学式为。(2)、“反应I”的离子方程式为。(3)、“某碳酸盐”的化学式 , 加热的目的是。(4)、为检验MnSO4受热分解是否生成SO2或SO3 , 某同学设计探究实验装置如图所示: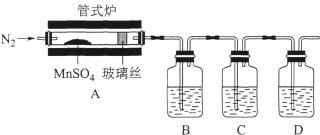
①装置B、C、D中的溶液依次为(填字母)。
a.Ba(NO3)2b.BaCl2c.品红 d.浓硫酸e.Ca(OH)2 f.NaOH
②实验结束时,为防止倒吸,正确的操作方法是。
(5)、测定产品纯度。取制得的MnSO4晶体0.1510g,溶于适量水中,加硫酸酸化;用过量NaBiO3(难溶于水)将Mn2+完全氧化为 , 过滤;洗涤未溶解固体2-3次,向滤液中加入Na2C2O4固体0.5360 g,振荡,充分溶解并反应后,用0.0320 mol·L-1KMnO4溶液滴定(被还原为Mn2+),用去20.00 mL。已知:Mr(Na2C2O4)=134,Mr(MnSO4)=151。①计算产品中MnSO4的质量分数(保留两位有效数字)。
②为提高测定的精度,应补充的实验操作。
-
3、废旧太阳能电池ClGS具有较高的回收利用价值,其主要组成为Culn0.5Ca0.5Se2。某探究小组回收处理流程如图:
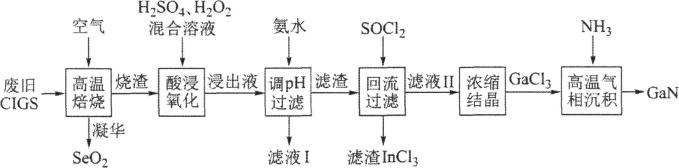
回答下列问题:
(1)、硒(Se)与硫为同族元素,Se的最外层电子数为;在化合物Culn0.5Ca0.5Se2中镓(Ga)和铟(In)均为+3价,则Cu的化合价为。(2)、“酸浸氧化”得蓝色溶液,则该过程发生的主要氧化还原反应的化学方程式为。(3)、氢氧化铜沉淀可溶于氨水,则滤液I中的阴离子主要有和两种。(4)、滤渣加入SOCl2混合前需要洗涤、干燥,并用试剂和来检验滤渣中的是否洗净。(5)、滤渣加入SOCl2可反生反应:2In(OH)3+3SOCl2=2InCl3+3X;对物质X的性质有如下判断,你认为不正确的是____。
A、有弱酸性 B、可使溴水褪色 C、与CaCl2溶液反应得白色沉淀 D、与烧碱溶液反应可生成两种盐(6)、“高温气相沉积”过程中发生的化学反应方程式为。 -
4、实验室制备SO2并探究其性质的方案如下,回答下列问题(1)、Ⅰ.制备SO2(部分固定装置略)

制备SO2可以选择的发生装置为(填大写字母)。(2)、选用如图装置制备并收集一瓶干燥的SO2 , 其连接顺序为:发生装置→(按气流方向,填小写字母)。(3)、Ⅱ.探究SO2与Cu(OH)2悬浊液的反应查阅资料:SO2在酸性条件下还原性较差,碱性条件下较强。
实验步骤:i.配制Cu(OH)2悬浊液:往NaOH溶液中加入CuSO4溶液可得到Cu(OH)2悬浊液。
ⅱ.将SO2通入Cu(OH)2悬浊液中(实验装置如图F)。
实验现象:F中出现少量红色固体,稍后,溶液呈绿色,与CuSO4溶液、CuCl2溶液的
颜色有明显不同。

配制Cu(OH)2悬浊液时,要保证溶液过量。(填“NaOH”或“CuSO4”)
(4)、为确定红色固体成分,进行如图实验:
①根据上述实验可得结论:该红色固体为。
②产生红色固体的原因是(用离子方程式表示)。
(5)、为探究F中溶液呈绿色而不是蓝色的原因,实验如下:ⅱ.取少量F中滤液,加入少量稀盐酸,产生无色刺激性气味的气体,得到澄清的蓝
色溶液。再加入BaCl2溶液,出现白色沉淀。
①实验i的目的是。
②溶液显绿色的原因可能是溶液中含有较多Cu (HSO3)2。小组同学通过进一步实验确认了这种可能性,在少量1mol·L-1的CuSO4溶液中加入(填化学式),得到绿色溶液。
-
5、(1)、书写对应的化学方程式:
①用氯气制备漂白粉:。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:。
③呼吸面具中过氧化钠与二氧化碳反应:。
④KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式。
(2)、书写对应的离子方程式:⑤制作印刷电路板时氯化铁溶液腐蚀铜:。
⑥用高锰酸钾酸性溶液检验溶液中的亚铁离子(还原产物为Mn2+):。
⑦在酸性条件下,向含铬废水中加入FeSO4 , 可将还原为Cr3+ , 该过程的离子
反应方程式为。
-
6、为探究新制氯水的性质,某学生做了如下实验。由上述实验可得新制氯水的性质与对应的解释或离子方程式不相符的是( )
实验 装置 试剂a 现象 ① 
紫色的石蕊试液 溶液先变红后褪色 ② NaHCO3溶液 产生气泡 ③ HNO3酸化的AgNO3溶液 产生白色沉淀 ④ FeCl2溶液、KSCN溶液 溶液变红 A、实验①说明新制氯水中含有H+、HClO B、实验②发生的反应为+HClO=ClO-+CO2↑+H2O C、实验③说明新制氯水中有Cl- , Cl- +Ag+=AgCl↓ D、实验④说明氯气具有强氧化性,Cl2+2Fe2+=2Cl-+ 2Fe3+ -
7、在酸性环境中,纳米Fe/Ni复合材料去除污染水体的的反应过程(Ni不参与反应)如图所示:下列表达反应过程或现象的方程式错误的是( )
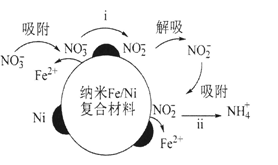 A、反应步骤i:+Fe+2H+ =+Fe2++H2O B、反应步骤ⅱ:+3Fe+8H+= 3Fe2+++2H2O C、反应进行一段时间,过滤出水体中出现的白色絮状物,白色絮状物在空气中最终变
A、反应步骤i:+Fe+2H+ =+Fe2++H2O B、反应步骤ⅱ:+3Fe+8H+= 3Fe2+++2H2O C、反应进行一段时间,过滤出水体中出现的白色絮状物,白色絮状物在空气中最终变成红褐色:4Fe(OH)2+O2+2H2O=4Fe(OH)3
D、硝酸亚铁溶液中滴加稀硫酸发现溶液变黄:2Fe2+++4H+= 2Fe3++SO2↑+ 2H2O -
8、利用浓缩海水,模拟侯氏制碱法制备NaHCO3 , 进一步处理得到产品Na2CO3和NH4Cl,实验流程如下。
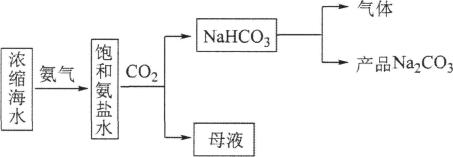
下列说法错误的是( )
A、将饱和氨盐水雾化后与CO2反应可使反应更快更充分 B、制备NaHCO3的化学方程式为NH3 +NaCl+ H2O+CO2=NaHCO3↓+NH4Cl C、流程中“气体”可循环利用 D、将“母液”低温蒸发结晶可得纯净的NH4Cl -
9、下列实验对应的离子方程式不正确的是( )A、浓硝酸用棕色瓶保存:4HNO3
 4NO2↑+ O2↑+ 2H2O
B、硫酸铵溶液显酸性:+H2O
4NO2↑+ O2↑+ 2H2O
B、硫酸铵溶液显酸性:+H2O NH3·H2O+H+
C、将少量SO2通入NaClO溶液:SO2+H2O+2ClO- =+ 2HClO
D、向AgCl悬浊液中滴加KI溶液产生黄色沉淀:AgCl(s)+I- (aq)
NH3·H2O+H+
C、将少量SO2通入NaClO溶液:SO2+H2O+2ClO- =+ 2HClO
D、向AgCl悬浊液中滴加KI溶液产生黄色沉淀:AgCl(s)+I- (aq) AgI(s)+Cl-(aq)
AgI(s)+Cl-(aq)
-
10、设NA为阿伏加德罗常数的数值。下列叙述正确的是( )A、0.1mol C2H5OH分子中含C-H键数为0.6NA B、由O与O组成的2.0g物质所含中子数为NA C、25℃,1L pH=13的Ba(OH)2溶液中OH-数为0.2 NA D、密闭容器中,2 mol SO2和1mol O2催化反应后分子总数为2 NA
-
11、某学习小组设计用98%的浓硫酸制取SO2并验证其部分性质的实验装置图如下(夹持装置省略)。下列叙述不正确的是( )
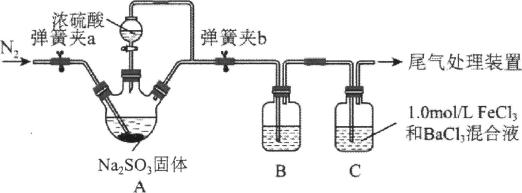 A、装置A中发生的离子反应方程式为:2H++= SO2↑+H2O B、若装置B中装有品红溶液,观察到B中溶液红色褪去,则说明SO2具有漂白性 C、若装置B中装有酸性高锰酸钾溶液,观察到B中溶液褪色,则说明SO2具有还原性 D、装置C产生的白色沉淀为BaSO4
A、装置A中发生的离子反应方程式为:2H++= SO2↑+H2O B、若装置B中装有品红溶液,观察到B中溶液红色褪去,则说明SO2具有漂白性 C、若装置B中装有酸性高锰酸钾溶液,观察到B中溶液褪色,则说明SO2具有还原性 D、装置C产生的白色沉淀为BaSO4 -
12、以下常见元素对应物质之间的每步转化中,都能通过一步反应实现的是( )
①Fe→FeCl2→Fe(OH)2→Fe(OH)3 ②Na→Na2O→Na2CO3→NaHCO3→NaOH
③NaAlO2→Al(OH)3→Al2O3→Al④H2S→S→SO3→H2SO4
⑤N2→NH3→NO→NO2→HNO3
A、①②③④ B、①③④⑤ C、①②③⑤ D、①②④⑤ -
13、中国传统文化对人类文明贡献巨大,古代文献中记载了古代化学研究成果。下列常见古诗文对应的化学知识正确的是( )
选
项
常见古诗文记载
化学知识
A
《梦溪笔谈》中对宝剑的记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折”
铁的合金硬度比纯铁的大,熔点比纯铁的高
B
《本草纲目拾遗》中对强水的记载:“性最烈,能蚀五金,其水甚强,惟玻璃可盛”
强水为氢氟酸
C
《天工开物》中记载:凡火药,硫为纯阳,硝为纯阴
硫指的是硫黄,硝指的是硝酸钾
D
《泉州府志》中记载:安南人黄姓者为宅煮糖,墙塌压糖,去土而糖白,后人遂效之
糖白的过程发生了化学变化
A、A B、B C、C D、D -
14、2023年3月, “三星堆”遗址考古又发掘出大量青铜器。火法炼铜主要发生的反应Cu2S+O2
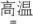 2Cu+SO2 , 下列说法正确的是( ) A、Cu2S中铜的化合价为+2 B、该反应为复分解反应 C、SO2是酸性氧化物 D、反应中氧化剂仅为O2
2Cu+SO2 , 下列说法正确的是( ) A、Cu2S中铜的化合价为+2 B、该反应为复分解反应 C、SO2是酸性氧化物 D、反应中氧化剂仅为O2 -
15、1827年,英国科学家法拉第进行了NH3喷泉实验。在此启发下,兴趣小组利用以下装置,进行如下实验。其中,难以达到预期目的的是( )
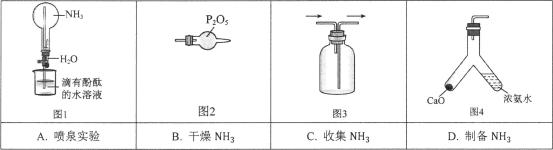 A、A B、B C、C D、D
A、A B、B C、C D、D -
16、化学创造美好生活。下列选项中生产活动和化学原理没有关联的是( )
选项
生产活动
化学原理
A
葡萄酒中添加少量SO2
SO2可杀菌且防止营养物质被氧化
B
用聚乙烯塑料制作食品保鲜膜
聚乙烯燃烧生成CO2和H2O
C
利用氧化银冶炼金属Ag
氧化银在一定条件下发生分解反应
D
用地沟油为原料制作肥皂
地沟油发生皂化反应
A、A B、B C、C D、D -
17、有机物H是一种新型大环芳酰胺的合成原料,可通过以下方法合成(部分反应条件已省略)。
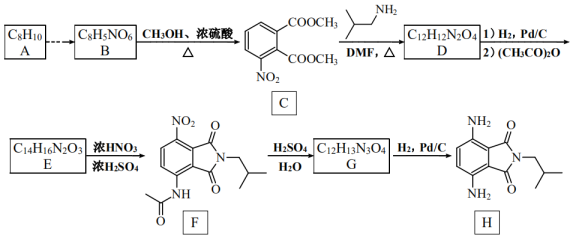
已知:①为邻、对位定位基,—COOH为间位定位基;
②苯胺有还原性,易被氧化。
(1)、化合物G的结构简式是 , F的官能团名称是。(2)、下列说法正确的是____。A、化合物B可与溶液反应 B、可依次通过取代反应、氧化反应实现A→B的转化 C、1mol化合物E最多可与3molNaOH发生反应 D、化合物H的分子式为(3)、写出C→D的化学方程式。(4)、B转化为C的过程中可能产生副产物I( ),写出4种同时符合下列条件的化合物I的同分异构体的结构简式。
),写出4种同时符合下列条件的化合物I的同分异构体的结构简式。①分子中含有苯环,无其他环;
②谱和IR谱检测表明:分子中有4种不同化学环境的氢原子,有
 , 无—OH和—O—O—(5)、凯夫拉(
, 无—OH和—O—O—(5)、凯夫拉(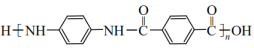 )材料广泛应用于防弹衣、坦克等兵器的生产。利用以上合成线路及已知信息,设计由苯胺(
)材料广泛应用于防弹衣、坦克等兵器的生产。利用以上合成线路及已知信息,设计由苯胺( )、、
)、、 为原料制备凯夫拉的合成路线(用流程图表示,无机试剂任选)。
为原料制备凯夫拉的合成路线(用流程图表示,无机试剂任选)。 -
18、某研究小组模拟工业湿法制备新型绿色消毒剂高铁酸钾,按如下流程开展实验。
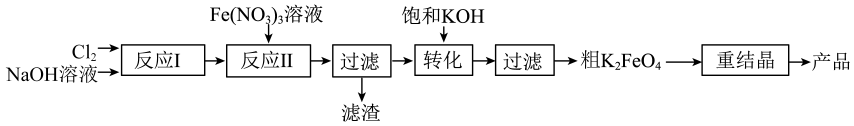
用以下装置可以完成上述反应I和反应Ⅱ:
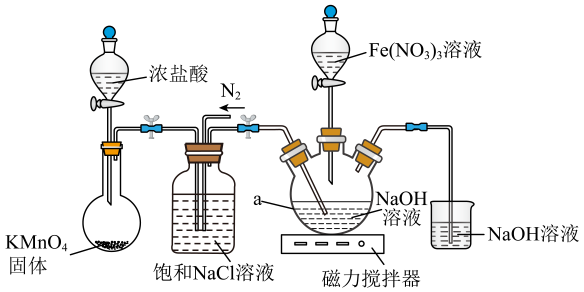
信息:①易溶于水,微溶于KOH溶液,难溶于乙醇;具有强氧化性,在酸性或中性溶液中快速产生;在0~5℃碱性溶液中较稳定。
②部分物质在水中的溶解度见下表
物质
溶解度/g
10℃
20℃
30℃
80℃
NaCl
35.8
36.0
36.3
38.4
80.0
88.0
96.0
148.0
(1)、仪器a的名称是 , 反应I中为了减少因反应过热而产生 , 可以采取的操作是。(2)、下列说法正确的是____。A、反应Ⅱ中为了加快反应速率,可进行搅拌与加热 B、反应Ⅱ结束后应通一段时间氮气,然后再拆下装置进行后续实验 C、加入饱和KOH溶液发生的是复分解反应 D、若用溶液代替溶液作铁源,的产率和纯度都会降低(3)、为了提高纯度需要对粗产品进行重结晶操作,从下列选项中选出合理的操作并排序:()→()→()→置于冰水浴中→()→用乙醇洗涤→干燥→得产品
a.将粗产品溶于水b.将粗产品溶于冷的稀KOH溶液 c.过滤取沉淀
d.过滤取滤液e.蒸发浓缩,趁热过滤f.加入饱和KOH溶液g.冷却结晶
(4)、测定产品的纯度(式量为M)称取ag左右碘化钾于碘量瓶中,加入100mLNaOH溶液和bg左右的固体氟化钠,待溶解完毕;准确称取mg样品于碘量瓶中,待样品充分溶解后,加硫酸酸化至反应完全;淀粉作指示剂,用标准溶液进行滴定,消耗标准液体积为VmL。已知: , (方程式未配平)
①本次实验测得纯度为 , 然后重复上述过程,平行测试3次。
②实验过程中往往需要加入过量且比理论计算所需量过量2~3倍左右的KI,理由是。
-
19、乙烷是一种重要的化工原料,可用作制冷剂、燃料、制备乙烯的原料。回答下列问题:
已知:①
②
③
(1)、乙烷催化氧化裂解法是一种新型的制备乙烯的方法,则。(2)、1000℃时,在某刚性密闭容器内充入一定量的 , 只发生反应①,若平衡时容器中总压为pPa,乙烷的转化率为 , 则该反应的平衡常数Pa(用含p、的代数式表示,为用分压表示的平衡常数)。达到平衡后,欲同时增大反应速率和乙烷的转化率,可采取的措施有(填选项字母)。A.升高温度B.通入惰性气体C.增加乙烷浓度D.加入催化剂
(3)、乙烷的氧化裂解反应产物中除了外,还存在、CO、C等副产物。图甲为温度对乙烷氧化裂解反应性能的影响,图乙为的值对乙烷氧化裂解反应性能的影响。
[乙烯选择性;乙烯收率=乙烷转化率×乙烯选择性]
下列说法正确的是____。
A、有利于提高乙烷平衡转化率的条件是高温低压 B、乙烷的转化率随温度的升高而增大的原因是此时反应未达平衡,升高温度,反应速率加快,反应物的转化率增大 C、较低时,生成乙烯的选择性较低的原因可能是氧气过量,乙烷发生深度氧化而导致乙烯的选择性降低 D、反应的最佳温度为700℃左右(4)、最新研究发现在乙烷的氧化裂解反应体系中充入一定量能更好的提高乙烷的转化率和乙烯的收率,请结合方程式说明原因。(5)、科技工作者结合实验与计算机模拟结果,研究了乙烷在催化剂表面脱氢制乙烯的反应,其部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS表示过渡态)。此部分历程中决速步骤的反应方程式为。
-
20、氨气用途非常广泛,以下是氨气的部分转化关系图。
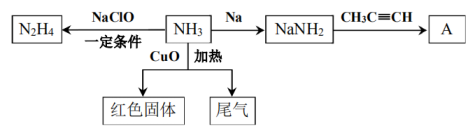
已知:①
②随着杂化轨道中s成分的增加,电子云更靠近原子核,核对电子的吸引力增强
(1)、又称联氨,不如氨气稳定,还原性强于氨气,与反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。①写出用于火箭推进剂反应的化学方程式。
②从分子结构角度分析,不如氨气稳定的原因是。
(2)、下列说法正确的是____。A、以上转化关系中只表现出还原性 B、若CuO无剩余,红色固体的组分可能有三种情况 C、制备氨基钠需在无水、无氧环境中进行 D、为了增加的产量,往往加入过量的NaClO(3)、结合已知信息,写出生成A的化学方程式。(4)、实验中在加热条件下通入过量的与CuO反应,设计实验验证尾气中比较活泼的两种气体。