相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、某研究小组按下列路线合成治疗细菌感染的药物氧氟沙星:

已知:

回答下列问题:
(1)、化合物C中含氧官能团名称是。(2)、化合物B的结构简式是。(3)、下列说法错误的是_______。A、有机物A能与溴水在FeBr3作用下发生取代反应 B、有机物E与乙酸乙酯属于同系物 C、有机物E→F的转化涉及加成、消去两步反应 D、氧氟沙星的分子式是C18H20FN3O4(4)、写出D与F生成G的化学方程式。(5)、以2—氨基乙醇( )与甲醛(HCHO)为原料,且利用以上合成路线中的相关信息,设计
)与甲醛(HCHO)为原料,且利用以上合成路线中的相关信息,设计 的合成路线(用流程图表示,无机试剂选)。 (6)、写出同时符合下列条件的化合物C的同分异构体的结构简式。
的合成路线(用流程图表示,无机试剂选)。 (6)、写出同时符合下列条件的化合物C的同分异构体的结构简式。①分子中含有苯环结构,并能发生银镜反应;
②1H-NMR谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,有
 , 没有−O−O−。
, 没有−O−O−。 -
2、甲醇是重要的化工原料之一,也可用作燃料,利用合成气(主要成分为CO、CO2和H2)可以合成甲醇,涉及的反应如下:
反应ⅰ:CO(g)+2H2(g)CH3OH(g) ΔH1
反应ⅱ:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH2=−49.9kJ·mol—1
反应ⅲ:CO2(g)+H2(g)CO(g)+H2O(g) ΔH3=+41.6kJ·mol—1
回答下列问题:
(1)、在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):
①反应ⅰ在(填“较低”或“较高”)温度下才能自发进行。
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式:。
③m=(计算结果保留两位有效数字,已知1eV=1.6×10—22kJ)。
(2)、将一定量的CO2(g)和H2(g)充入密闭容器中并加入合适的催化剂,只发生反应ⅱ和ⅲ.相同温度下,在不同压强下测得CO2的平衡转化率、CH3OH的选择性[×100%]和CO的选择性×100%随压强的变化曲线如图所示。
图中表示CO2的平衡转化率的曲线是(填“m”“n”或“p”),简述判断方法:。
(3)、有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现。保持温度T不变,向一恒容密闭容器中充入4molCO2和8molH2 , 在该催化剂作用下发生反应,经5min达到平衡,测得H2O(g)的物质的量为3mol,起始及达平衡时容器的总压强分别为1.5akPa、akPa,则从开始到平衡用H2分压表示的平均反应速率为kPa·min—1(用含a的式子表示,下同,分压=总压×物质的量分数);反应ⅱ的压强平衡常数Kp=(kpa)—2(Kp为用分压代替浓度计算的平衡常数)。(4)、光催化CO2制甲醇技术也是研究热点。铜基纳米光催化材料还原CO2的机理如图所示,光照时,低能价带失去电子并产生空穴(h+ , 具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为。
-
3、
实验室用废铁屑制取无水氯化铁并测其纯度。实验方案如下:
I.FeCl3·6H2O制备
①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后的废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)步骤①的主要目的是。
(2)步骤②控制温度在40~50℃的原因是。
II.无水FeCl3制备
已知SOCl2熔点-156℃,沸点77℃,易水解。
(3)按图装置进行实验。锥形瓶中生成无水FeCl3的总化学方程式为;仪器A的作用是。

III.产品纯度测定
(4)称取3.500g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用0.2000mol·L-1Na2S2O3溶液滴定(I+2S2O=3I—+S4O),经三次平行实验,消耗Na2S2O3溶液体积分别为19.50mL,20.02mL,19.98mL。
①所制产品的纯度为%(以无水FeCl3质量分数表示,保留三位有效数字)。
②所制产品中可能含有FeCl2杂质,检验FeCl2的试剂为(填化学式)溶液;产生FeCl2的原因可能是。
-
4、以锌灰(含及少量(PbO、CuO、Fe2O3、SiO2)和为原料可以制备脱硫剂 , 该脱硫剂的制备硫化、再生过程可表示为:

请回答下列问题:
(1)、“浸取”时需不断通入高温水蒸气,其目的是。(2)、“除杂”包括加适量锌粉、过滤、加氧化等步骤,除和外,与锌粉反应的离子还有(填离子符号)。(3)、“沉锌铁”时反应体系温度不能过高,可能的原因是。(4)、时,将一定比例、CO、CO2和H2S的混合气体以一定流速通过装有脱硫剂的硫化反应器,已知硫化过程中,与H2、H2S反应生成和 , 其化学方程式为。(5)、将硫化后的固体在的混合气体中加热再生,固体质量随温度变化的曲线如图所示,在范围内,固体质量增加的主要原因可能是。 (6)、能形成多种配离子,已知形成的一种配离子只有一种空间结构,则的空间结构为。
(6)、能形成多种配离子,已知形成的一种配离子只有一种空间结构,则的空间结构为。 -
5、难溶盐可溶于盐酸,常温下,用盐酸调节浊液的 , 测得体系中或与的关系如图。下列说法不正确的是
 A、N代表与的变化曲线 B、Y点的溶液中存在 C、常温下, D、Z点的溶液中存在
A、N代表与的变化曲线 B、Y点的溶液中存在 C、常温下, D、Z点的溶液中存在 -
6、工业上以软锰矿(主要成分为MnO2)为原料通过固体碱熔氧化法生产高锰酸钾,主要流程如下。下列说法错误的是
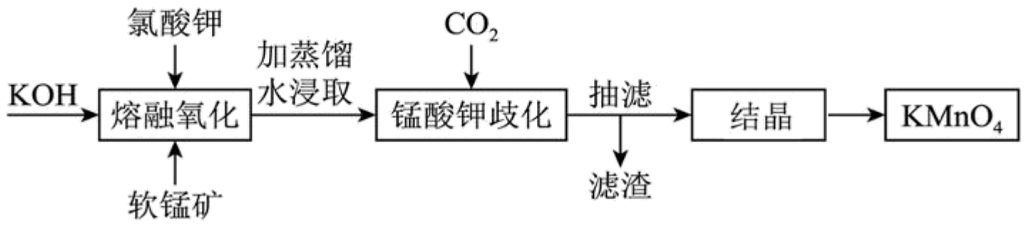 A、“熔融氧化”应在铁坩埚中进行,陶瓷坩埚或Al2O3坩埚均不行 B、“锰酸钾歧化”可以用H2SO4但不能用盐酸代替CO2 C、“结晶”操作与从NaCl溶液得NaCl晶体操作相同 D、该流程中可循环使用的物质是MnO2
A、“熔融氧化”应在铁坩埚中进行,陶瓷坩埚或Al2O3坩埚均不行 B、“锰酸钾歧化”可以用H2SO4但不能用盐酸代替CO2 C、“结晶”操作与从NaCl溶液得NaCl晶体操作相同 D、该流程中可循环使用的物质是MnO2 -
7、丙烯与氢卤酸的加成反应过程主要分两步完成,如图:

其中,反应速率主要由第一步烯烃与H+结合生成碳正离子决定。下列说法错误的是
A、反应物丙烯不存在顺反异构 B、上述条件下,丙烯生成中间产物a的反应活化能较低 C、若使用CF3CH=CH2进行上述反应,则主要产物可能为CF3CH2CH2Cl D、上述反应,在适当条件下氢卤酸中卤素离子浓度越大反应速率越快 -
8、电动汽车电池一直是研究热点,高能量密度的全固态电池有望在2027年投入应用,2030年左右实现大规模商用。现有某可充放电的全固态钠电池,工作原理如图所示,下列说法正确的是
 A、为了降低成本,可以将固态聚合物电解质换为Na3PO4溶液 B、放电时,电极电势N极高于M极 C、充电时,M极电极反应式为:Na3V2(PO4)3-2e—=NaV2(PO4)3+2Na+ D、充电时,Na+由N极迁移至M极
A、为了降低成本,可以将固态聚合物电解质换为Na3PO4溶液 B、放电时,电极电势N极高于M极 C、充电时,M极电极反应式为:Na3V2(PO4)3-2e—=NaV2(PO4)3+2Na+ D、充电时,Na+由N极迁移至M极 -
9、环六糊精(D-吡喃葡萄糖缩合物)具有空腔结构,腔内极性较小,腔外极性较大,可包含某些分子形成超分子。图1、2、3分别表环六糊精结构、超分子示意图及相关应用。下列说法正确的是
 A、环六糊精属于多糖 B、邻氯苯甲醚、对氯苯甲醚均易被环六糊精包合形成超分子 C、通过图2、图3可知对氯苯甲醚与环六糊精形成的超分子甲氧基、氯原子均暴露在反应环境中 D、由题目信息可知,分离环六糊精和氯代苯甲醚通常采用蒸馏法
A、环六糊精属于多糖 B、邻氯苯甲醚、对氯苯甲醚均易被环六糊精包合形成超分子 C、通过图2、图3可知对氯苯甲醚与环六糊精形成的超分子甲氧基、氯原子均暴露在反应环境中 D、由题目信息可知,分离环六糊精和氯代苯甲醚通常采用蒸馏法 -
10、下列实验操作或现象和相应结论均正确的是
选项
实验操作或现象
结论
A
向2mL0.1mol·L-1K2Cr2O7溶液中滴加5~10滴6mol/LNaOH溶液,溶液由橙色变黄色
减小生成物浓度,K2Cr2O7反应的平衡正移
B
用pH计测定SO2、CO2饱和溶液的pH,前者pH小
Ka:H2SO3>H2CO3
C
将含NaOH、乙醇的1-溴丁烷混合体系加热后产生的气体通入酸性KMnO4溶液中,紫红色褪去
1-溴丁烷发生了消去反应
D
用饱和Na2CO3溶液浸泡BaSO4一段时间后过滤洗涤,向所得的滤渣上滴加稀盐酸,有气泡冒出
Ksp(BaSO4)>Ksp(BaCO3)
A、A B、B C、C D、D -
11、实验室制取FeSO4溶液和NaHCO3溶液,并利用两者反应制取FeCO3 , 下列有关实验装置和操作不能达到实验目的的是
 A、用装置甲制取FeSO4溶液 B、用装置乙制取NaHCO3溶液 C、用装置丙制取FeCO3 D、用装置丁过滤所得的浊液
A、用装置甲制取FeSO4溶液 B、用装置乙制取NaHCO3溶液 C、用装置丙制取FeCO3 D、用装置丁过滤所得的浊液 -
12、M、W、X、Y、Z是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的核外s能级电子数等于p能级电子数,X的核外电子有4种空间运动状态;五种主族元素组成的化合物Q的结构如图所示。下列说法错误的是
 A、原子半径:X>Y>Z B、Y元素组成的最常见单质和M的单质,在加热条件下生成的化合物中只含离子键 C、Q的结构存在配位键,除M外的原子最外层均满足8电子稳定结构 D、含X、Y、Z等元素的化合物
A、原子半径:X>Y>Z B、Y元素组成的最常见单质和M的单质,在加热条件下生成的化合物中只含离子键 C、Q的结构存在配位键,除M外的原子最外层均满足8电子稳定结构 D、含X、Y、Z等元素的化合物 具有较高的熔沸点
具有较高的熔沸点
-
13、我国第一部中药学典籍《神农本草经》中记载的一种中药“昆布”,具有利水消肿的功效,其主要成分是3,5-二碘酪氨酸,结构简式如下图。下列关于该有机物说法错误的是
 A、该分子中含有1个手性碳原子 B、理论上1mol该物质最多消耗3molH2 C、既能与盐酸反应,也能与NaOH溶液反应 D、等量该物质最多消耗NaHCO3与Na2CO3的物质的量之比为1:1
A、该分子中含有1个手性碳原子 B、理论上1mol该物质最多消耗3molH2 C、既能与盐酸反应,也能与NaOH溶液反应 D、等量该物质最多消耗NaHCO3与Na2CO3的物质的量之比为1:1 -
14、下列反应方程式书写正确的是A、用醋酸和淀粉-KI溶液检验加碘盐中的IO:IO+5I-+6H+=3I2+3H2O B、利用FeS处理废水中的Hg2+:FeS(s)+Hg2+(aq)HgS(s)+Fe2+(aq) C、用Pt作电极电解MgCl2溶液:2Cl-+2H2OCl2↑+H2↑+2OH- D、煅烧硫铁矿:4FeS2+15O28SO3+2Fe2O3
-
15、设NA为阿伏加德罗常数的值。下列说法一定正确的是A、136gKHSO4晶体与CaSO4晶体混合物中离子总数为2NA B、标准状况下,22.4LC4H8中σ键数目为11NA C、78gNa2O2与足量的CO2和H2O混合物反应转移电子数为2NA D、电解精炼铜时,阳极减少32g,转移电子数为NA
-
16、实验是化学的基础。下列基本实验描述正确的是

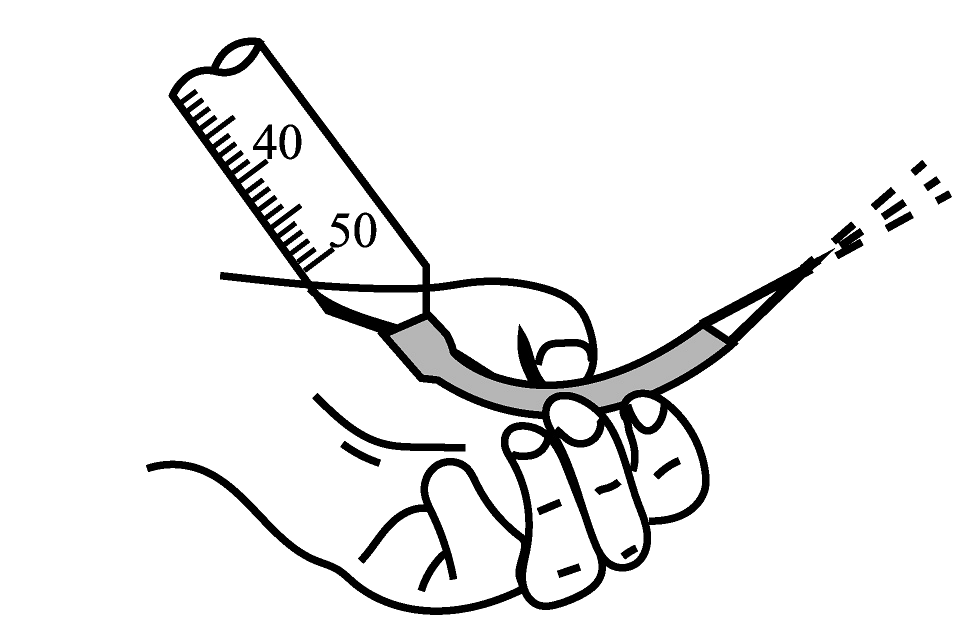
A.图中标识意为洗净手才可进行实验
B.排出盛有KMnO4溶液滴定管尖嘴内的气泡

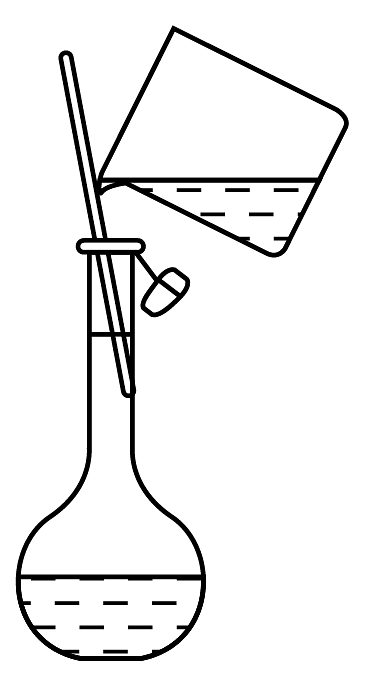
C.测新制氯水的pH
D.向容量瓶转移溶液
A、A B、B C、C D、D -
17、下列化学用语使用正确的是A、H2S、PCl3的VESPR模型一致 B、异戊烷的空间填充模型:
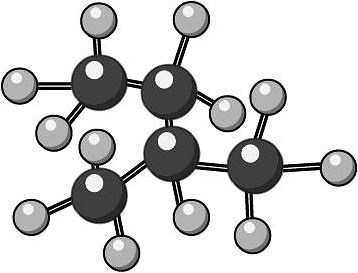 C、用系统命名法命名CH2ClCH2Cl:二氯乙烷
D、基态As原子简化电子排布式:[Ar]4s24p3
C、用系统命名法命名CH2ClCH2Cl:二氯乙烷
D、基态As原子简化电子排布式:[Ar]4s24p3
-
18、化学无处不在。下列说法错误的是A、微生物降解塑料的使用有利于消除“白色污染” B、汽车智能驾驶离不开强大汽车芯片,二氧化硅是该芯片的核心成分 C、《哪吒》电影中的结界兽原型是三星堆青铜器,青铜属于合金材料 D、加工馒头、面包和饼干时可加入适量碳酸氢铵、碳酸氢钠等,使其松软或酥脆
-
19、下列关于物质检验或推断一定正确的是A、向某溶液中滴加KSCN溶液,溶液呈现红色,则溶液中无Fe2+ B、对某溶液进行焰色试验,观察到黄色火焰,则该溶液中无K+ C、向某溶液中滴加盐酸,能产生无色能使品红溶液褪色的气体,则原溶液中一定存在 D、向某溶液中滴加NaOH溶液,加热,若产生能使湿润的红色石蕊试纸变蓝的气体,则证明原溶液中一定存在
-
20、物质类别和元素价态是研究物质性质的两个重要角度。下图为含氮物质的“价—类”二维图的部分信息。下列说法不正确的是
 A、从的转化是人工固氮的重要方法 B、Y的化学式为 C、从 , 必需加入氧化剂 D、使用和X制备硝酸铵氮肥时,氮元素的化合价没有发生变化
A、从的转化是人工固氮的重要方法 B、Y的化学式为 C、从 , 必需加入氧化剂 D、使用和X制备硝酸铵氮肥时,氮元素的化合价没有发生变化