相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、工业合成氨反应是在催化剂表面上进行的,其反应历程如下(*表示吸附态):
化学吸附:;
表面反应;;;
脱附;
(1)、298K时各化学键的键能如下:化学键
kJ/mol
436
946
391
已知反应的正反应活化能 , 则逆反应活化能。
(2)、一定温度下,在一固定容积的密闭容器中充入一定量的和发生上述反应,下列选项中能说明反应已达平衡状态的是_______。A、混合气体的密度保持不变 B、和的速率之比: C、单位时间内断开1mol的同时断开3mol D、混合气体的平均相对分子质量保持不变(3)、在反应历程中,的“吸附分解”决定了合成氨的整体反应速率,从结构角度分析,其原因是。(4)、由Arrhenius经验公式得 , 式中k为反应速率常数;为活化能,单位为kJ/mol;T为热力学温度;R、C为常数。根据的反应热、图1和图2,升高温度,的变化曲线为(为压力平衡常数),的变化曲线为(写字母标号)。 (5)、反应在恒温恒压()下进行,若、起始物质的量之比为1:3,的平衡产率为(),则(用、p列出表达式即可)。(6)、以浓差电池(电解质溶液浓度不同造成电势差)为电源,用石墨作电极将转化为高纯的装置如图,电解前Cu(1)和Cu(2)电极质量相同。
(5)、反应在恒温恒压()下进行,若、起始物质的量之比为1:3,的平衡产率为(),则(用、p列出表达式即可)。(6)、以浓差电池(电解质溶液浓度不同造成电势差)为电源,用石墨作电极将转化为高纯的装置如图,电解前Cu(1)和Cu(2)电极质量相同。
①M极电极反应式为。
②电解停止时,理论上Cu(1)和Cu(2)电极的质量差为g。
-
2、锡(Sn)是第IVA族元素,其常见的氯化物有SnCl4和SnCl2。SnCl4常温下为液体,遇水极易发生水解反应;SnCl2常温下为固体,具有还原性,可被空气中的氧气氧化。某化学实验小组制备SnCl4的装置如图(加热与夹持装置省略)。

回答下列问题:
(1)、仪器a的名称是;装置B中盛放的试剂是。(2)、制取SnCl4的操作步骤为:①连接好装置;②;③添加药品、滴加浓盐酸;④待装置D后,加热装置C;⑤收集SnCl4。请补充上述实验步骤。已知装置A中反应的还原产物为 , 写出该反应的离子方程式。(3)、装置E的作用是。(4)、经测定发现实验所得SnCl4 , 样品中含有少量的SnCl2 , 测定样品纯度的方案如下:取ag样品溶于足量稀盐酸中,加入淀粉溶液作指示剂,用碘酸钾标准溶液滴定至终点,消耗标准液。滴定过程中先后发生的反应为:
i.
ii.(均未配平)
则SnCl4样品的纯度为%;若滴定时间过长,会使测量结果(填“偏大”、“偏小”或“无影响”)。
-
3、劳动创造美好生活!下列劳动项目与所述化学知识没有关联的是
选项
劳动项目
化学知识
A
口腔医生:在牙齿表面涂一层含氟釉质防龋齿
B
桥梁工程师:用牺牲阳极法对黄茅海大桥钢管桩进行防护
Fe作电解池阴极被保护
C
环境工程师:测定某地雨水pH值为5.1
大气中等溶于雨水使其显酸性
D
珠宝鉴定师:用X射线鉴定钻石的真伪
不同的晶体具有独特的明锐衍射峰
A、A B、B C、C D、D -
4、
CO2转化为具有高附加值的化学品对实现“碳中和”具有重要意义。
I.通过以下反应可获得新型能源二甲醚。
①
②
③
(1)反应②正反应在________(填“较低温度”或“较高温度”)条件下能自发进行。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
A. 增大CO2浓度,反应①、②的正反应速率都增加 B. 移去部分CH3OH(g),反应②、③的平衡均向右移动 C. 加入反应①的催化剂,可提高CO2的平衡转化率 D. 降低反应温度,反应③的正反应速率增加、逆反应速率减小 (3)在5.0MPa下,将5molCO2和10mol H2在催化剂作用下仅发生上述反应①和②,平衡时CH3OH和CO的选择性S及的CO2转化率a随温度的变化如图所示。已知,选择性S为:S(CH3OH或CO)= , 表示平衡时CO的选择性的曲线是________(填“x”“y”或“z”),CO的选择性随温度改变呈现该变化的原因是:________。

(4)250℃时,平衡体系共有0.5molCH3OH,则CO2的平衡转化率________。
Ⅱ.CH4和CO2反应制备“合成气”反应历程分两步:
步骤
反应
正反应速率方程
逆反应速率方程
反应ⅰ
反应ⅱ
上述反应中为吸附性活性炭,反应历程的能量图变化如下图所示:

(5)该反应中的决速步骤为________(填反应ⅰ或反应ⅱ)
(6)一定温度下,反应的平衡常数________(用、、、表示)。
-
5、奥司他韦被称为流感特效药,具有抗病毒的生物学活性,其主流合成路线如图所示:
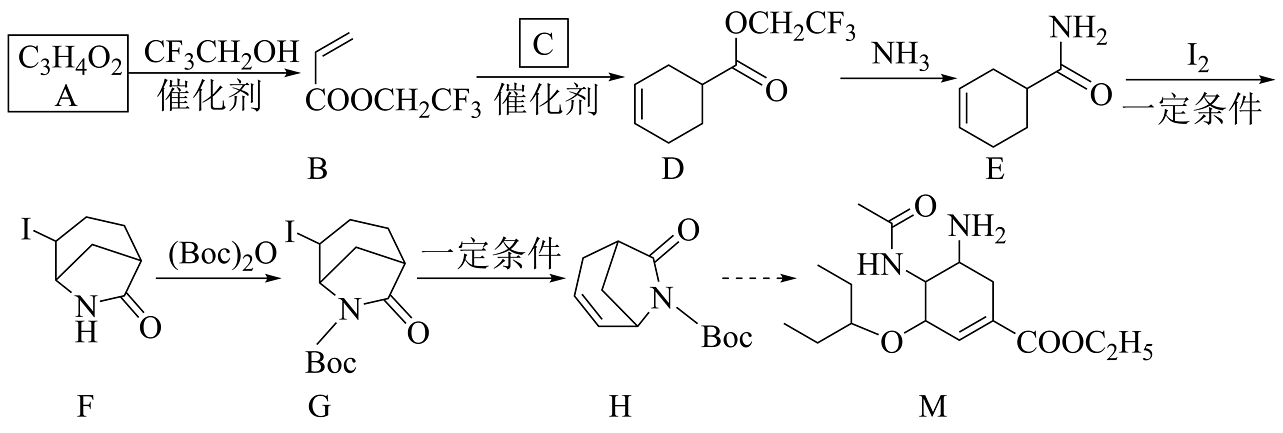
已知:的结构简式为
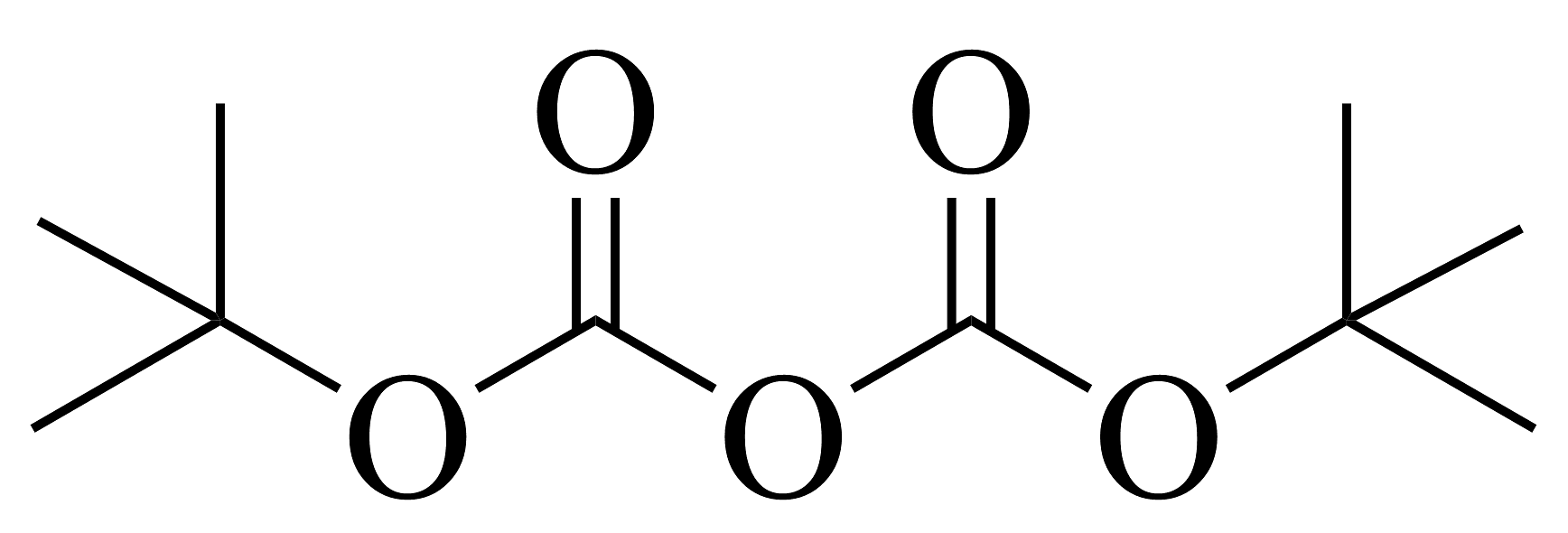 。回答下列问题:(1)、写出A的结构简式;其中碳原子的杂化方式是。(2)、B中含氧官能团名称为。(3)、已知C的分子式为C4H6 , 写出B→D的化学方程式为。(4)、E→F的反应分两步进行,第一步反应是加成反应,第二步的反应类型是。(5)、有关奥司他韦(M),下列说法错误的是___________。A、其官能团种类为5种 B、其所有碳原子有可能共平面 C、1mol奥司他韦最多可与3mol H2发生加成 D、可与盐酸反应生成有机盐(6)、在B的同分异构体中,同时满足下列条件的共有种(不考虑立体异构)。
。回答下列问题:(1)、写出A的结构简式;其中碳原子的杂化方式是。(2)、B中含氧官能团名称为。(3)、已知C的分子式为C4H6 , 写出B→D的化学方程式为。(4)、E→F的反应分两步进行,第一步反应是加成反应,第二步的反应类型是。(5)、有关奥司他韦(M),下列说法错误的是___________。A、其官能团种类为5种 B、其所有碳原子有可能共平面 C、1mol奥司他韦最多可与3mol H2发生加成 D、可与盐酸反应生成有机盐(6)、在B的同分异构体中,同时满足下列条件的共有种(不考虑立体异构)。①链状结构;②能与饱和NaHCO3溶液反应产生气体;③含-CF3。
(7)、已知 (R1、R2、R3、R4为烃基或氢原子),请结合题中流程,写出利用CH3CH2CH2Br和
(R1、R2、R3、R4为烃基或氢原子),请结合题中流程,写出利用CH3CH2CH2Br和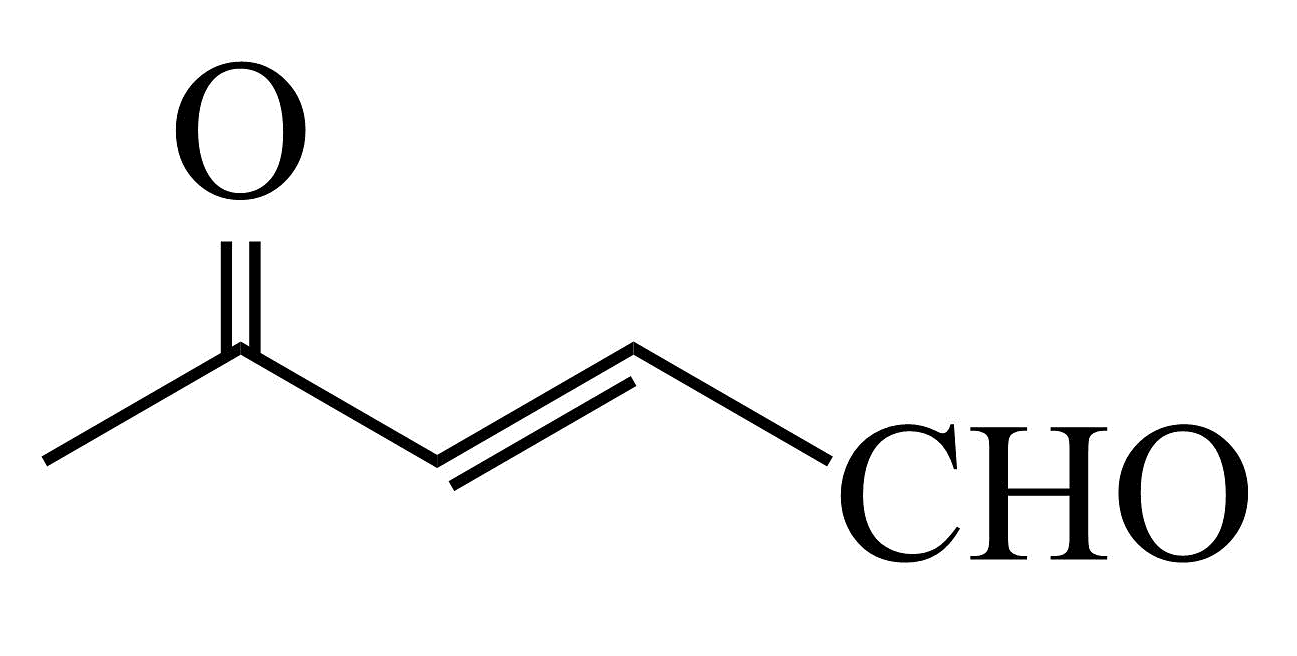 为主要原料制备的
为主要原料制备的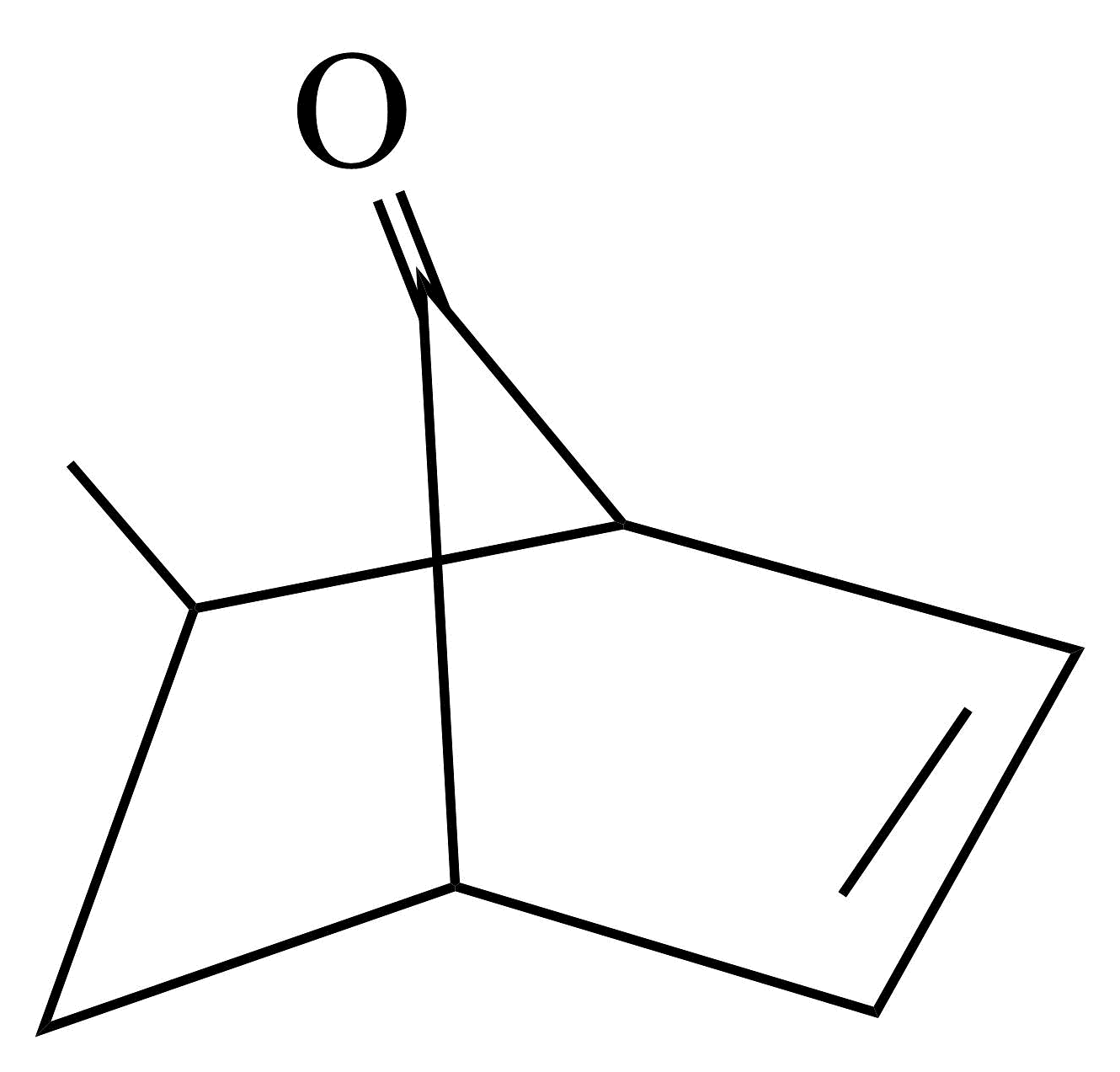 合成路线(无机试剂任选)。
合成路线(无机试剂任选)。 -
6、镍是重要的战略储备金属,广泛用于国防、航空航天、能源领域。从红土镍矿中冶炼镍成为了研究热点,红土镍矿主要含有NiO、SiO2、Fe2O3、Fe3O4等成分。一种碳还原-超声氨浸工艺流程如图所示:
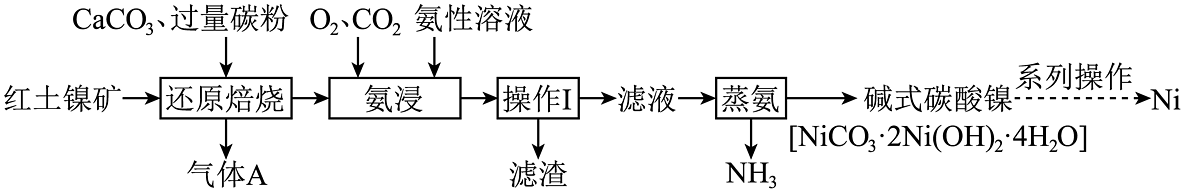
已知:氨性溶液由NH3•H2O、NH4HCO3配制;“还原焙烧”反应的产物为镍铁合金、硅酸钙。
回答下列问题:
(1)、“气体A”为(填名称)。(2)、“氨浸”时的温度为20℃,在此条件下超声浸出一小时,浸出率可达60%以上,选择该温度的原因是。(3)、经过“氨浸”后转化为含[Ni(NH3)4]2+的某酸式盐,写出“氨浸”中Ni发生反应的离子方程式:。(4)、“操作Ⅰ”中需使用的玻璃仪器为。(5)、“系列操作”中包含高温热解碱式碳酸镍生成NiO,再通入H2制得Ni单质。请写出“高温热解”的化学方程式:;若生产59吨镍,理论上需要H2kg。(6)、碱式碳酸镍受热过程中可能生成其它镍的氧化物,其中一种晶胞结构如下图所示,该氧化物的化学式为 , 该晶胞的俯视图为(填字母代号)。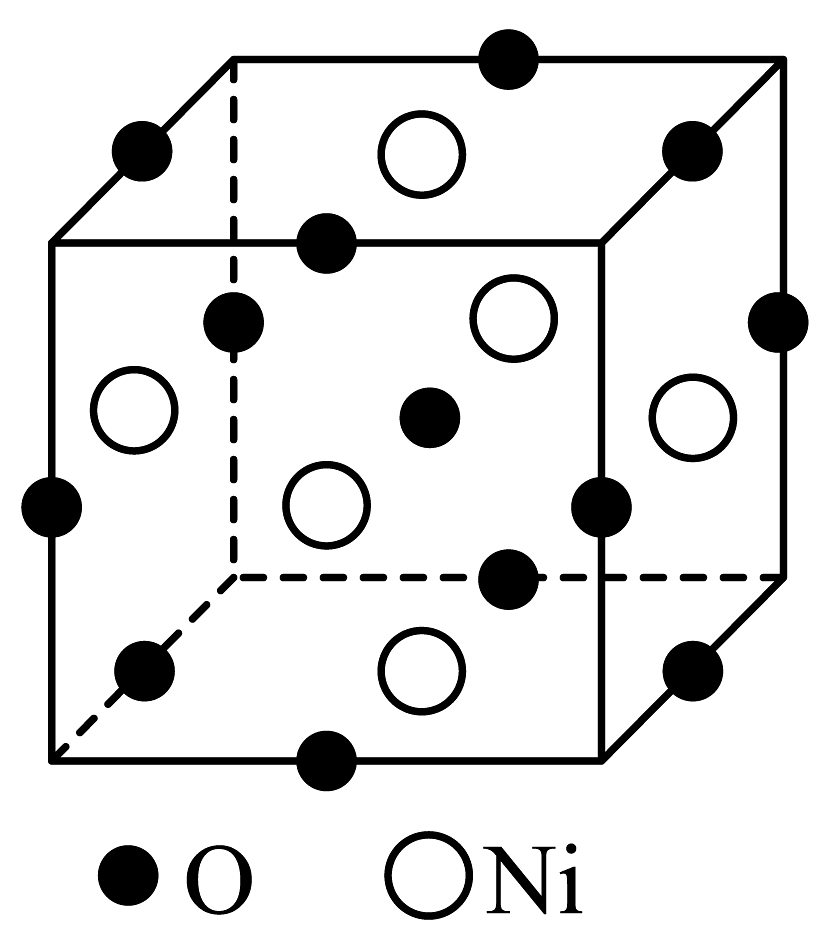
A.
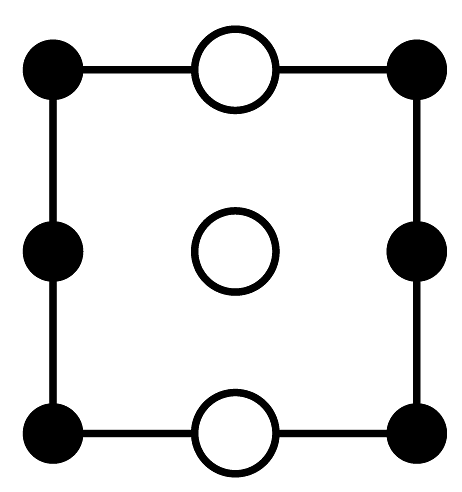 B.
B.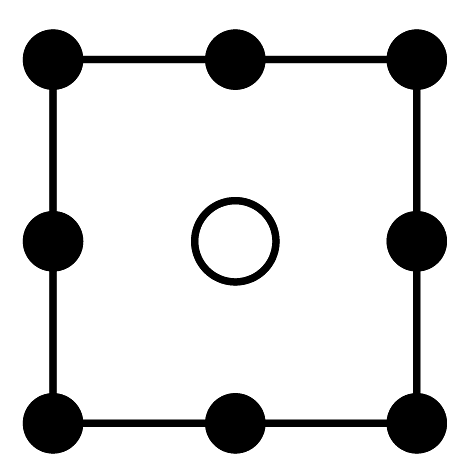 C.
C.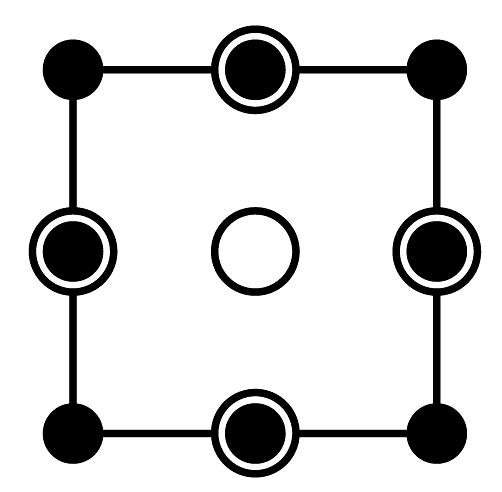
-
7、叶绿素铜钠是国家食品安全允许使用的食品添加剂,医疗领域叶绿素铜钠能止血抗炎、促进伤口愈合。某实验小组利用茭白叶,在实验室制备叶绿素铜钠,反应原理如下:
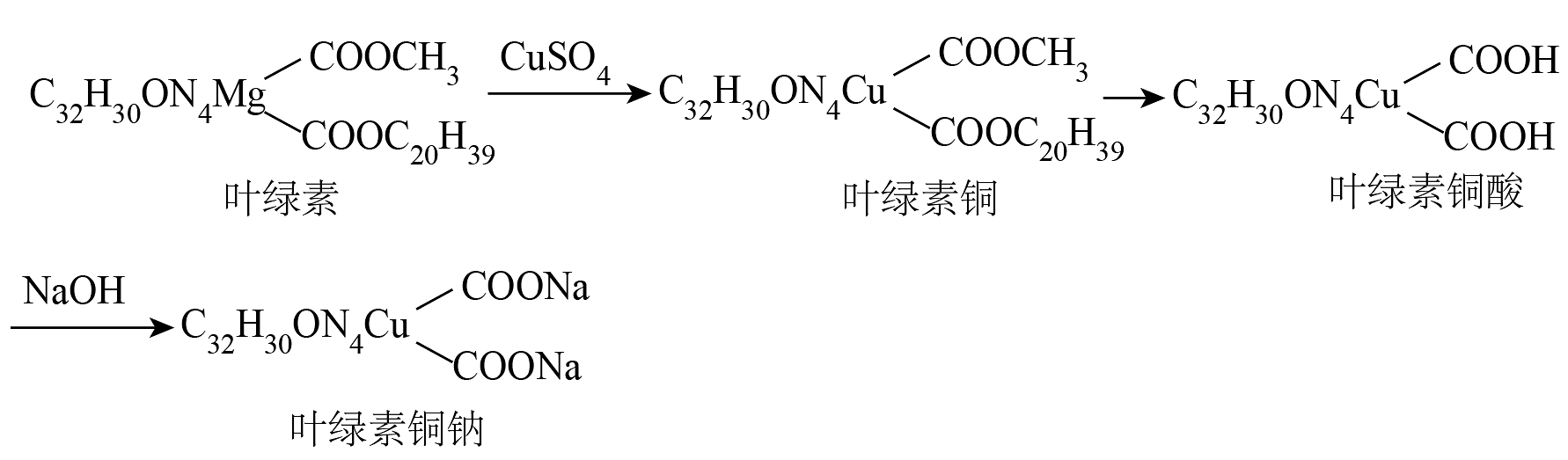
实验步骤:
Ⅰ.称取洗净剪碎的茭白叶10.0g(叶绿素含量为17.84%),加入少量石英砂、碳酸钙粉末,研磨。
Ⅱ.加入10mL96%乙醇继续研磨成均匀浆状,微波加热6min后抽滤。滤渣加入10mL96%乙醇,再次微波加热、浸提、抽滤,将两次滤液合并。
Ⅲ.滤液装入仪器C,加入硫酸酸化,加入硫酸铜晶体,搅拌至硫酸铜晶体溶解后,再加入盐酸调节溶液pH至2~3,搅拌加热半小时以上。
Ⅳ.……
Ⅴ.将叶绿素铜与50%乙醇混合,加入NaOH溶液,加热15min,再加入稀 溶液,加热至有墨绿色物质浮起,过滤、洗涤、干燥,得到叶绿素铜酸。
Ⅵ.将叶绿素铜酸放入烧杯中,保温80℃,逐滴加入2%氢氧化钠溶液至pH为10,过滤,滤液经蒸发结晶,烘干即得成品1.026g。
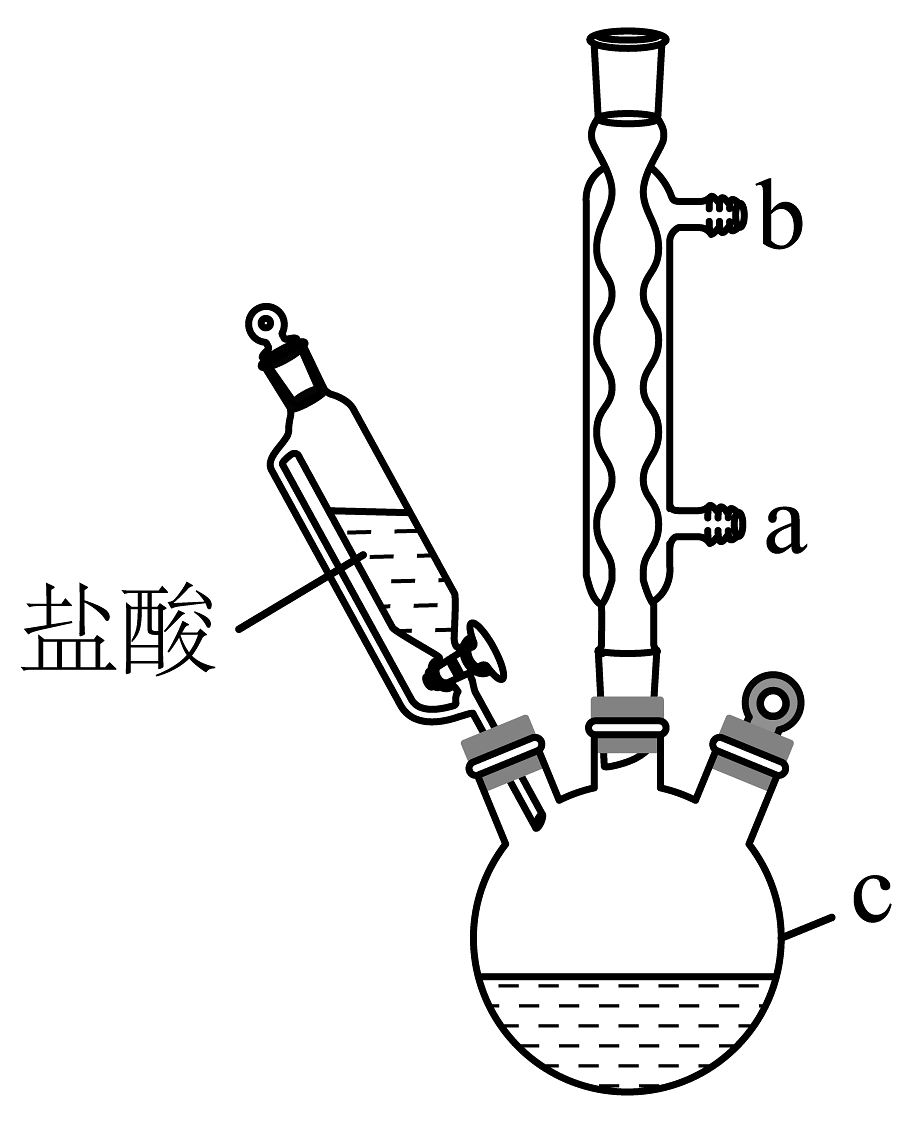
已知:
物质
相对分子质量
部分性质
叶绿素
892
蓝绿色固体,不溶于水,易溶于有机溶剂,对热不稳定,最佳提取温度约为80℃
叶绿素铜
932
绿色固体,不溶于水和50%乙醇
叶绿素铜酸
640
墨绿色固体,不溶于水
叶绿素铜钠
684
墨绿色固体,易溶于水,水溶液透明,受热较稳定
(1)、仪器C的名称是 , 冷却水应从(填“a”或“b”)口通入。(2)、96%的乙醇的主要作用是。(3)、步骤Ⅲ中加入硫酸酸化的目的是(结合离子方程式和化学平衡移动原理说明)。(4)、步骤IⅤ的操作为:冷却后向混合物中加入(填标号),静置后过滤、洗涤、干燥,得到叶绿素铜。A.蒸馏水 B.无水乙醇 C.NaOH
(5)、本实验采用微波加热,微波加热时,电炉内的微波场以极高的频率改变电场的方向,使水分子迅速摆动而产生热效应。在高频改变方向的电场中水分子会迅速摆动的原因是。A.水分子具有极性共价键B.水分子中有共用电子对
C.水由氢、氧两种元素组成D.水分子是极性分子
用甲烷高温分解制炭黑的工业生产中,是否适合使用该技术加热并请说明原因。
(6)、本实验的产率为% -
8、保持总压恒为P0 , 在相同的催化剂下发生反应2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g) ∆H<0。当起始投料比=3时H2的平衡转化率与T的关系、T0K时H2的平衡转化率与的关系如图所示。下列说法错误的是
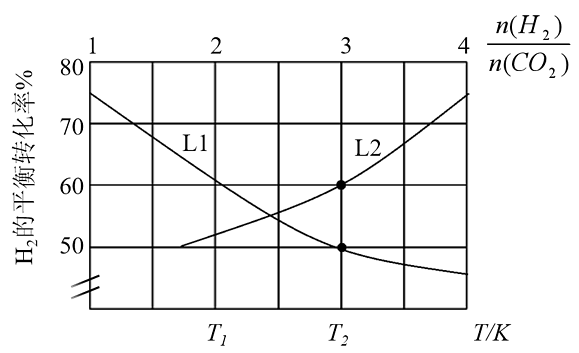 A、L1表示T0K时H2的平衡转化率与的关系 B、T1>T2 C、=3,T0K的条件下,达到平衡时,体系中水蒸气的体积分数为32.1% D、T0K时,该反应的压强平衡常数(用平衡分压代替平衡浓度)KP=3P0-4
A、L1表示T0K时H2的平衡转化率与的关系 B、T1>T2 C、=3,T0K的条件下,达到平衡时,体系中水蒸气的体积分数为32.1% D、T0K时,该反应的压强平衡常数(用平衡分压代替平衡浓度)KP=3P0-4 -
9、利用草酸(H2C2O4)及草酸盐的性质可测定人体血液中钙离子的浓度。已知:25℃,H2C2O4的电离常数;草酸钙的 , 碳酸钙的。25℃时,下列叙述错误的是A、在Na2C2O4溶液中:c(Na+)=2c(C2O)+2c(HC2O)+ 2c(H2C2O) B、在0.1mol/L的H2C2O4溶液中:c(H+)>c(H2C2O) C、将等浓度的H2C2O4溶液与NaOH溶液等体积混合,所得混合溶液的pH<7 D、向20mL碳酸钙的饱和溶液中逐滴加入的草酸钠溶液20mL,会产生草酸钙的沉淀
-
10、资料表明,烷烃的卤代反应为自由基反应,自由基是分子在光、热等外界条件下共价键发生均裂(指共价键断裂时均等的将共用电子对分配给成键的两个原子)而形成的原子或原子团,在水中不易形成。下图是氯气与甲烷发生取代反应的能量变化图。下列说法不正确的是
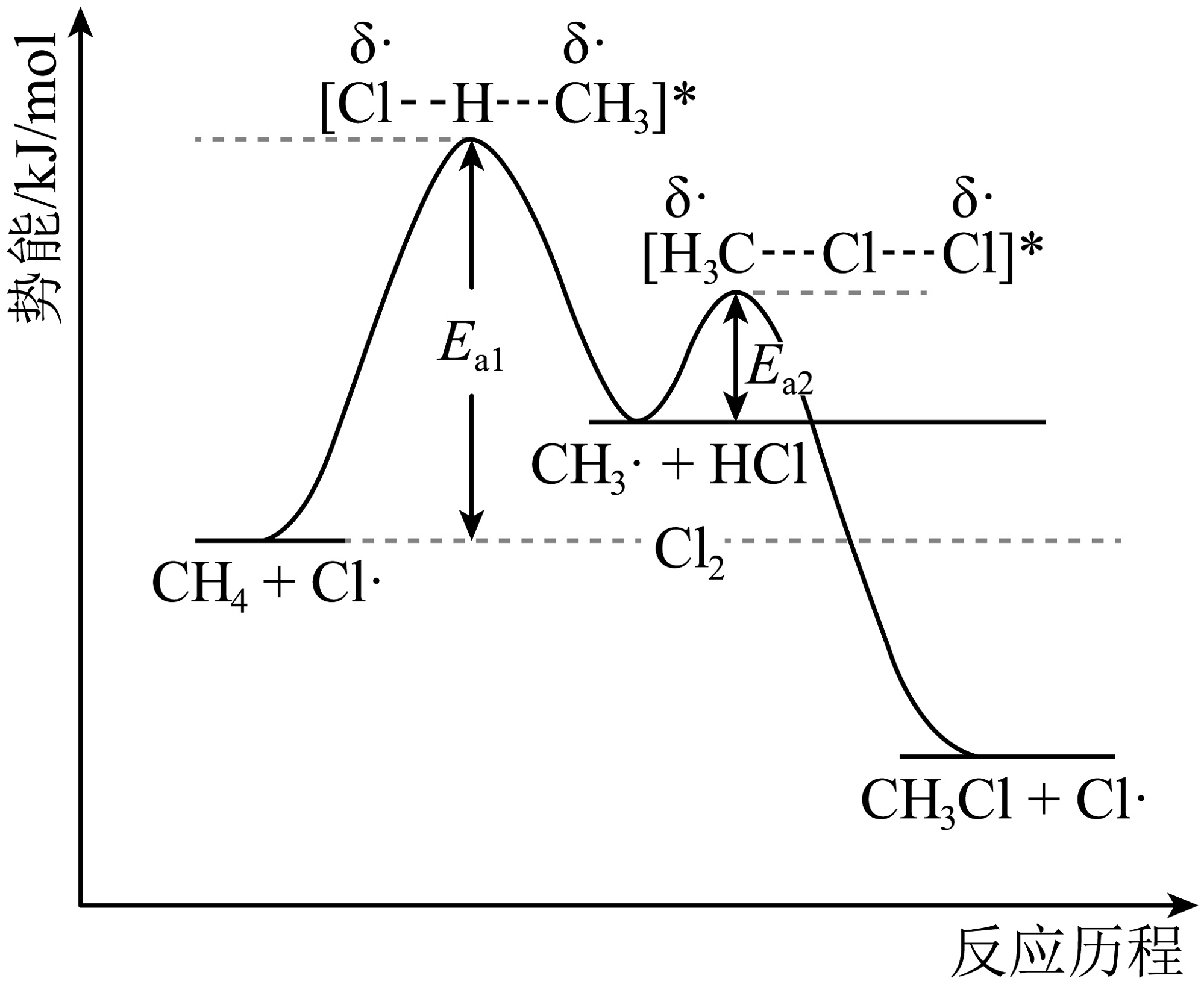 A、烷烃可与卤素气态单质发生卤代反应 B、烷烃可与溴水发生取代反应 C、烷烃可在光照或高温下发生卤代反应 D、产物中可能含有乙烷
A、烷烃可与卤素气态单质发生卤代反应 B、烷烃可与溴水发生取代反应 C、烷烃可在光照或高温下发生卤代反应 D、产物中可能含有乙烷 -
11、[Co(NH3)6]Cl3(三氯六氨合钴)是合成其它含钴配合物的重要原料,其晶体制备流程如下,下列说法错误的是
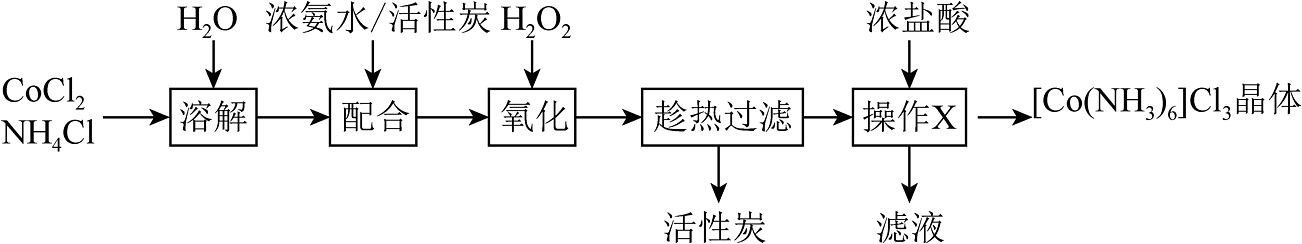 A、活性炭的作用是催化剂 B、已知氧化步骤需控温在60℃进行,故H2O2溶液应缓慢滴加 C、操作X中加入盐酸的目的是提供酸性环境 D、[Co(NH3)6]3+是以Co3+为中心的正八面体结构,则[Co(NH3)4Cl2]+的空间结构可能有2种
A、活性炭的作用是催化剂 B、已知氧化步骤需控温在60℃进行,故H2O2溶液应缓慢滴加 C、操作X中加入盐酸的目的是提供酸性环境 D、[Co(NH3)6]3+是以Co3+为中心的正八面体结构,则[Co(NH3)4Cl2]+的空间结构可能有2种 -
12、乙醇电催化氧化制备乙醛的原理如下图所示,下列说法正确的是
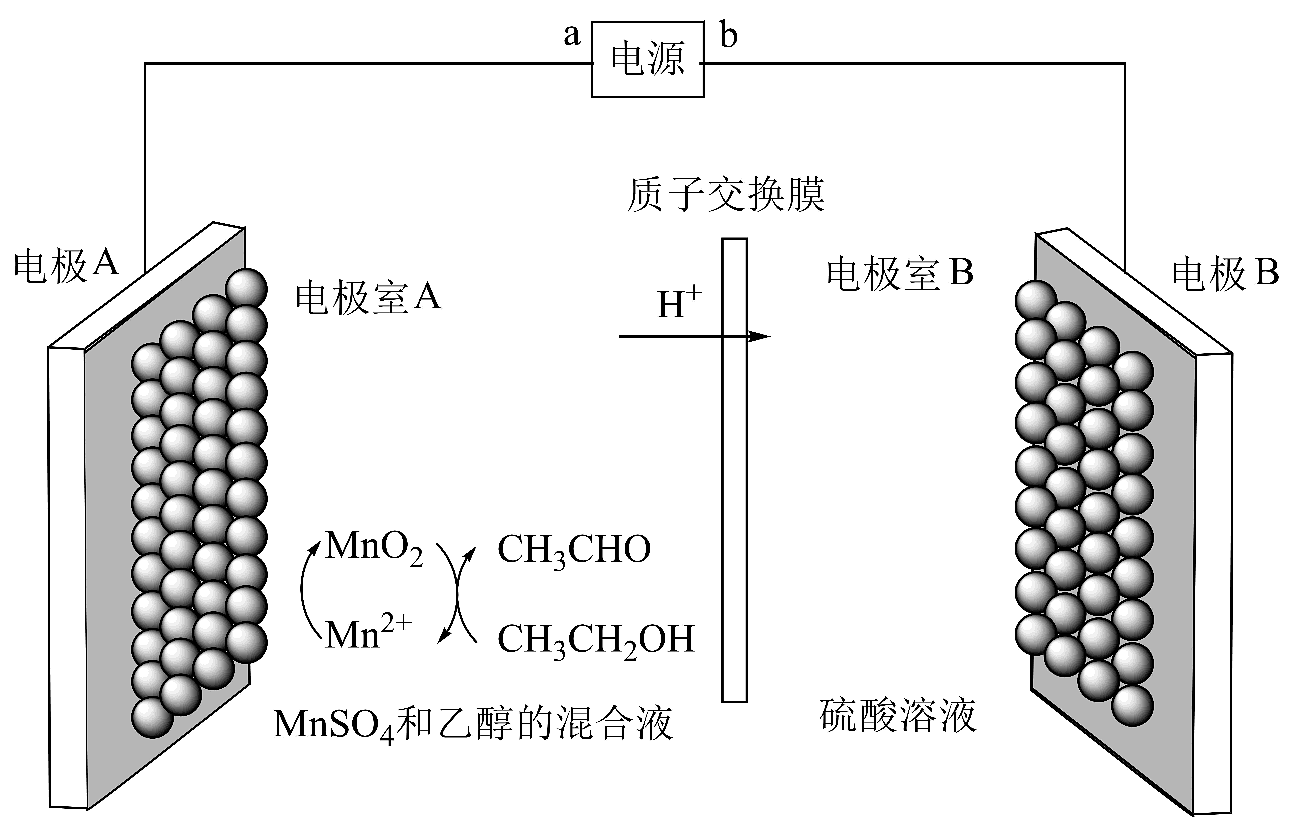 A、a为电源正极 B、电解过程中,电极室A的pH值不变,电极室B的pH值减小 C、电极B的电极反应为2H2O+2e-=H2↑+2OH- D、当生成n molCH3CHO时,理论上A、B两室溶液质量变化之和为n g
A、a为电源正极 B、电解过程中,电极室A的pH值不变,电极室B的pH值减小 C、电极B的电极反应为2H2O+2e-=H2↑+2OH- D、当生成n molCH3CHO时,理论上A、B两室溶液质量变化之和为n g -
13、某化合物的晶胞如图所示,下列说法不正确的是
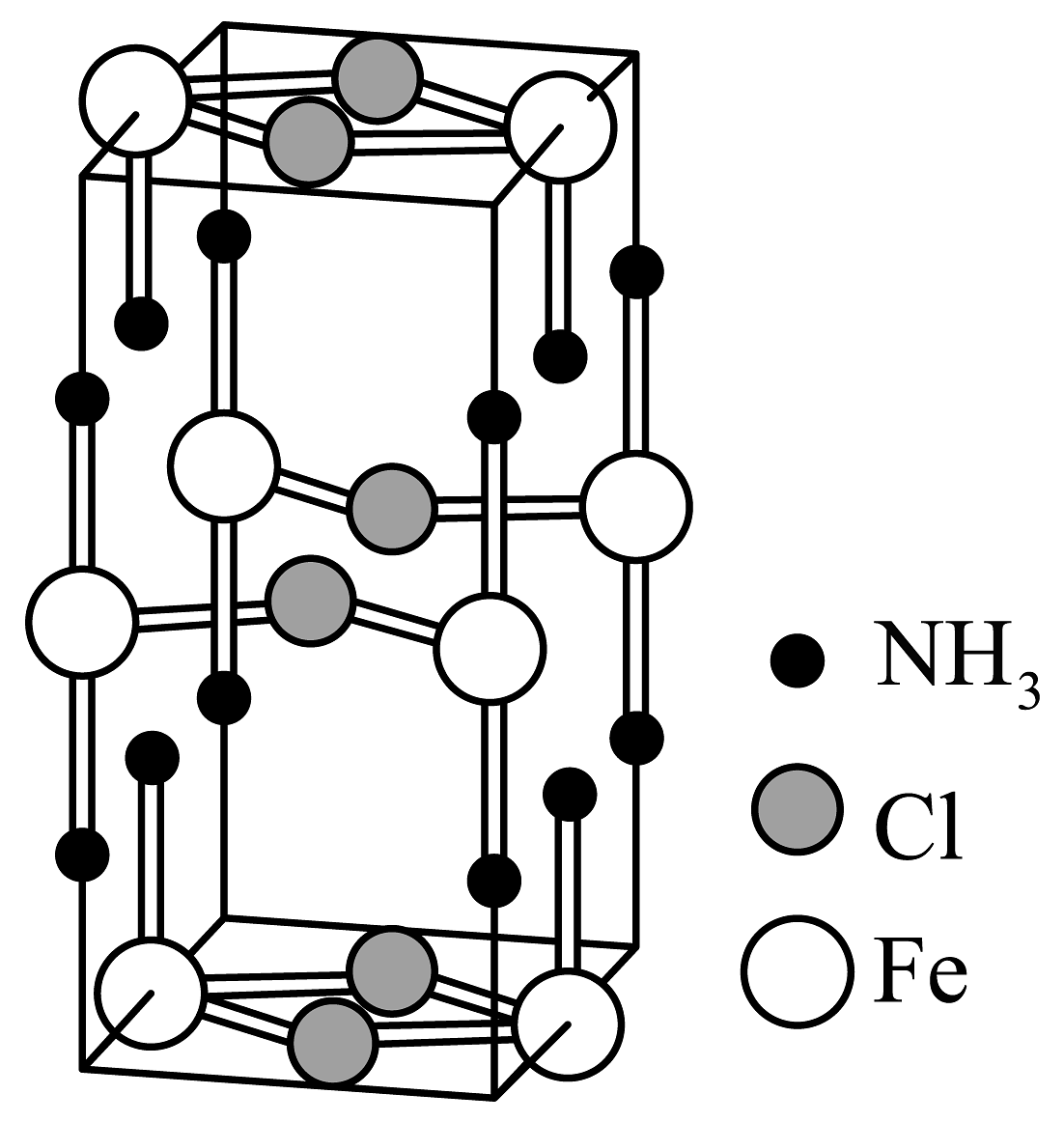 A、该物质化学式为Fe(NH3)2Cl2 B、该物质的熔点高于FeCl2 C、该晶体中含离子键、配位键 D、若该晶胞体积为a cm3 , 则晶胞的密度为g/cm3
A、该物质化学式为Fe(NH3)2Cl2 B、该物质的熔点高于FeCl2 C、该晶体中含离子键、配位键 D、若该晶胞体积为a cm3 , 则晶胞的密度为g/cm3 -
14、聚合物固态电解质(SPE)替代传统有机液态电解液,有望从根本上解决电池安全性问题,是电动汽车和规模化储能理想的化学电源。某SPE的基体材料结构如图所示,已知X、Y、Z为原子序数依次增大的短周期元素,Z的电负性为4.0,则下列说法错误的是
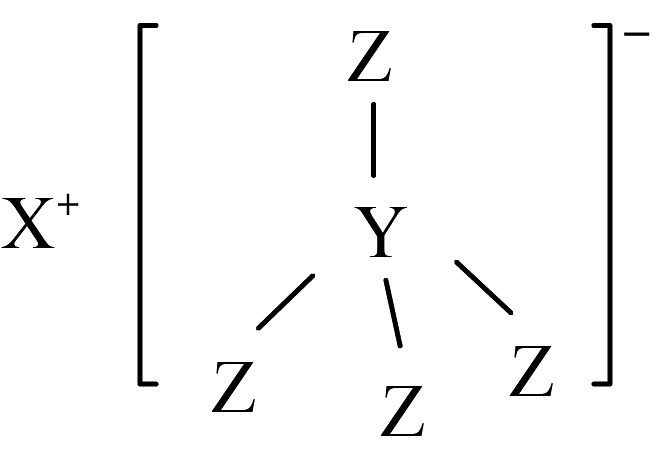 A、X的单质在空气中燃烧只生成一种氧化物 B、该物质的阴离子中含有配位键 C、Z是所在周期第一电离能最大的元素 D、Y的最高价氧化物对应的水化物是一元弱酸
A、X的单质在空气中燃烧只生成一种氧化物 B、该物质的阴离子中含有配位键 C、Z是所在周期第一电离能最大的元素 D、Y的最高价氧化物对应的水化物是一元弱酸 -
15、制备芯片需要大量使用光刻胶。光刻胶又称光致抗蚀剂,是指通过紫外光、电子束、离子束、X射线等的照射或辐射,其溶解度发生变化的耐蚀剂刻薄膜材料。如图是某种光刻胶的光交联反应。下列有关说法正确的是
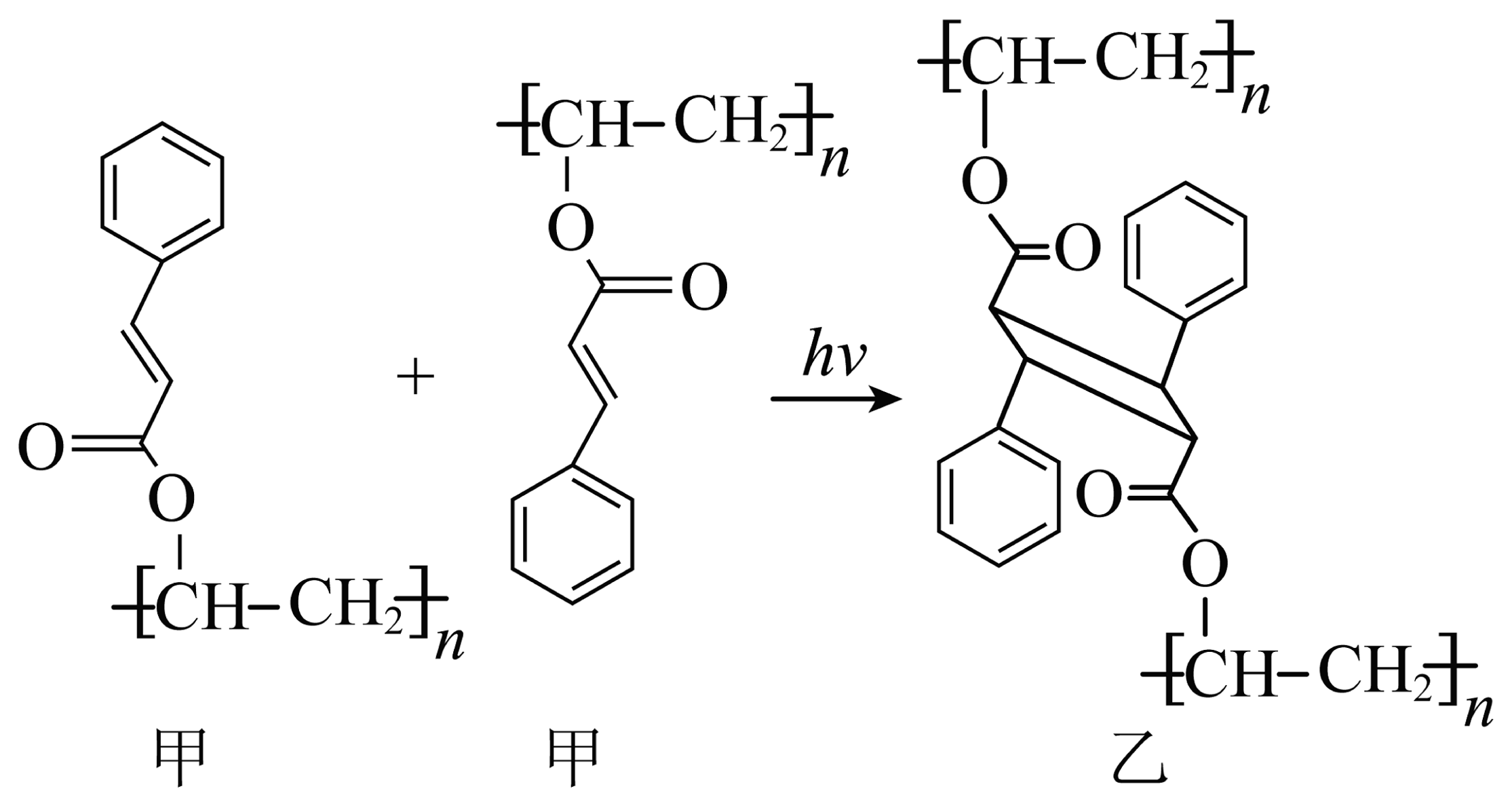 A、物质甲的单体的分子式为C11H8O2 B、1mol物质甲与足量H2加成时最多消耗3molH2 C、可利用红外光谱测量有机物的键长、键角 D、该光交联反应属于加成反应
A、物质甲的单体的分子式为C11H8O2 B、1mol物质甲与足量H2加成时最多消耗3molH2 C、可利用红外光谱测量有机物的键长、键角 D、该光交联反应属于加成反应 -
16、下列微观结构或现象不能解释其性质的是
选项
性质
结构因素
A
细胞膜的双分子膜层头向外,尾向内排列
细胞膜由大量两性分子(一端有极性,另一端无极性)组装而成
B
HCOOH的酸性强于CH3COOH
烷基是拉电子基团
C
原子光谱是不连续的线状谱线
原子核外电子的能量是量子化的
D
椅式环己烷(C6H12)比船式环己烷稳定
分子空间结构不同,椅式的空间位阻小
A、A B、B C、C D、D -
17、为达到实验目的,下列实验设计及现象都合理的是
选项
实验设计
实验目的
A
已知CuCl2溶液中存在平衡:[Cu(H2O)4]2+(蓝色)+4Cl−[CuCl4]2-(黄色)+4H2O,加热某浓度的CuCl2溶液,溶液由蓝色变为黄绿色
证明该平衡反应的正反应是吸热反应
B
加热使I2(s)升华
除去Fe粉中的I2
C
向丙烯醛溶液中滴加溴水,溴水褪色
验证丙烯醛中含碳碳双键
D
将SO2通入品红溶液中,品红溶液褪色,加热褪色后的溶液,溶液恢复红色
验证SO2的不稳定性
A、A B、B C、C D、D -
18、下列有关方程式书写不正确的是A、用处理含的废液,其离子方程式为: B、电解精炼铜的阴极反应:Cu2++2e−=Cu C、将SO2通入酸性KMnO4溶液中: D、证明NH3对Cu2+的配位能力强于H2O:
-
19、下列有关实验操作规范,说法不正确的是A、使用聚四氟乙烯活塞的滴定管为酸碱通用滴定管 B、将结块的硝酸铵置于研钵中用研杵敲碎,研细 C、磨口玻璃瓶塞洗净、晾干后应在瓶塞处垫一张纸条以免瓶塞与瓶口粘连 D、制取氧气后,剩余的高锰酸钾固体需要配成溶液或转化为其它物质后排放
-
20、下列化学用语或图示表示正确的是A、晶态和非晶态SiO2粉末的X射线衍射图谱对比:
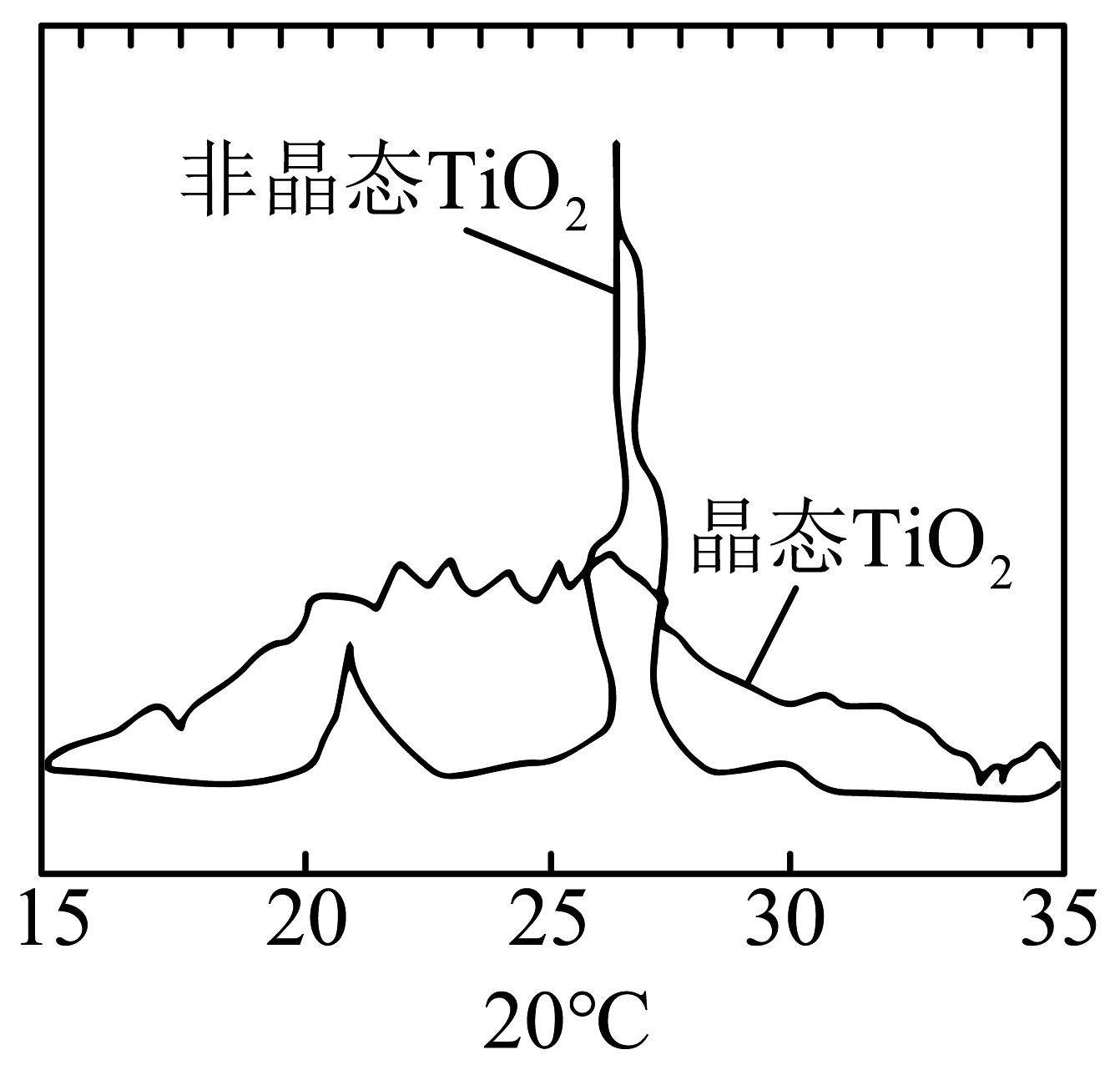 B、基态29Cu原子的价层电子轨道表示式:
B、基态29Cu原子的价层电子轨道表示式: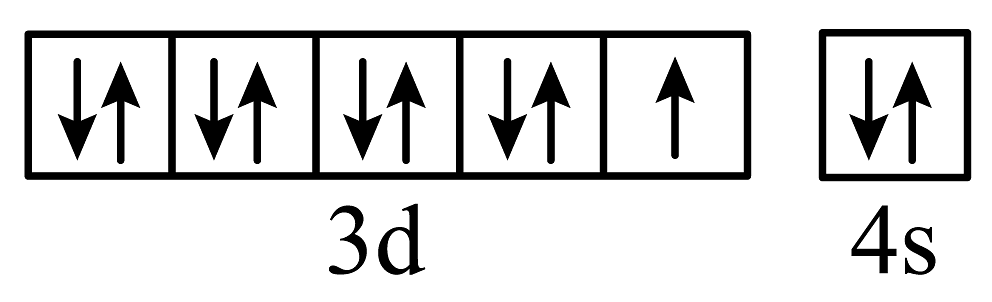 C、中子数为20的Ca原子:Ca
D、SO的VSEPR模型为:
C、中子数为20的Ca原子:Ca
D、SO的VSEPR模型为: