相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列装置能达到实验目的是( )




甲
乙
丙
丁
A、甲:测定KI溶液浓度 B、乙:利用牺牲阳极法来防止钢铁输水管的腐蚀 C、丙:中和反应反应热的测定 D、丁:测定Zn和稀硫酸反应的速率 -
2、下列有关电解质溶液的说法不正确的是( )A、常温下,磷酸中加水至原体积的两倍, B、将溶液从常温加热到80℃,溶液仍呈中性,但 C、常温下,相同的盐酸和醋酸溶液, D、常温下,相同的和溶液导电能力相同
-
3、设NA为阿伏加德罗常数的值。下列说法错误的是( )A、30℃时,的溶液中,水电离出的数目为 B、电解精炼粗铜,阳极溶解铜时,外电路中通过的电子数目为 C、为的新制氯水中次氯酸分子与次氯酸根离子数目之和为 D、常温下,的溶液中,与数目都小于
-
4、下列热化学相关的描述正确的是( )A、在光照和点燃条件下不同 B、已知 , , 则 C、表示的燃烧热: D、一定条件下 , 则和置于密闭容器中充分反应放热
-
5、下列表述正确的是( )A、2p能级的三个轨道相互垂直,能量相等 B、最外层电子数为2的元素都分布在区 C、基态S原子有16种空间运动状态不同的电子 D、第ⅦA族元素从上到下氢化物水溶液酸性逐渐减弱
-
6、以CO2和NH3为原料合成尿素反应分两步完成,ⅰ.CO2和NH3生成H2NCOONH4;ⅱ.H2NCOONH4分解生成尿素,总反应为: △H。反应过程能量变化如图。下列说法错误的是( )
 A、第一步ΔS<0 B、第二步活化能大于第一步 C、△H =+87.5 kJ∙mol-1 D、升高温度,总反应反应物活化分子百分数增大,反应速率增大
A、第一步ΔS<0 B、第二步活化能大于第一步 C、△H =+87.5 kJ∙mol-1 D、升高温度,总反应反应物活化分子百分数增大,反应速率增大 -
7、下列关于盐类水解的应用,说法不正确的是( )A、工业上可利用水解制备 B、水溶液蒸发结晶能得到固体 C、除去溶液中的可加入后过滤 D、配制溶液时,先将固体溶于较浓的盐酸中
-
8、下列基态粒子化学用语表达正确的是( )A、的最高能级的电子云轮廓图:
 B、的电子排布图:
B、的电子排布图:  C、Br原子的价层电子排布式:
D、Cr的简化电子排布式:
C、Br原子的价层电子排布式:
D、Cr的简化电子排布式:
-
9、下列水溶液呈碱性的盐是( )A、 B、 C、 D、
-
10、元素化合物知识是学习化学学科的基石,化合物X由三种元素组成,某学习小组为探究其组成,按如下流程进行实验:

回答下列问题:
(1)、气体B为 , 白色沉淀E为(填化学式)。(2)、化合物X中的三种元素为 , X的化学式为。(3)、已知黄色沉淀为硫单质,C→D的反应过程中,部分粒子的数目随时间变化如图所示,则溶液中生成硫单质的离子方程式为。 (4)、D→E的化学方程式为。
(4)、D→E的化学方程式为。 -
11、(1)、Ⅰ.是一种重要的无机化合物,可添加在食盐中用于补充碘成分,预防碘缺乏病。利用“氧化法”制备工艺流程如图所示:

已知:酸化反应为:
“酸化反应”中每生成1个 , 电子转移个。而反应所需从海带中提取。经历灼烧海带,浸泡海带灰等步骤,向获得的含的溶液中加入 , 在酸性条件下生成 , 其离子方程式为。(2)、“逐”可采用的方法是 , “滤液”中的溶质主要是。(3)、用“调pH”时发生反应的化学方程式为。(4)、Ⅱ.某反应的一种反应机理如图所示:
该过程的总反应化学方程式为。
(5)、该反应的催化剂是(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。(6)、该催化循环Ⅰ→Ⅱ过程中铁元素的化合价(填“不变”或“发生了变化”。 -
12、(1)、Ⅰ.历史会被尘封,但不会被掩盖,更不会被忘记。1939年4月,日寇在侵略晋城时使用了生化武器氯气弹,犯下了滔天之罪。某化学兴趣小组同学利用以下装置制备和收集少量干燥、纯净的氯气,选用如图所示仪器及药品:
上述实验中,用来盛放浓盐酸的仪器的名称是。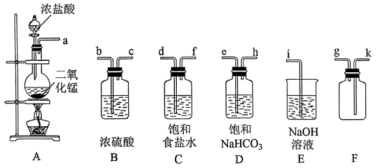 (2)、选择上述仪器并按顺序连接(填各接口处的字母):。(3)、制得的通过盛有饱和食盐水的装置,目的是。(4)、氢氧化钠溶液的作用是(用化学方程式表示)。(5)、若需要制取 , 需要的质量为g。(6)、Ⅱ.亚氯酸钠是一种高效的漂白剂和消毒剂,它在酸性条件下生成并放出 , 有类似的性质。某兴趣小组探究亚氯酸钠的制备与性质。
(2)、选择上述仪器并按顺序连接(填各接口处的字母):。(3)、制得的通过盛有饱和食盐水的装置,目的是。(4)、氢氧化钠溶液的作用是(用化学方程式表示)。(5)、若需要制取 , 需要的质量为g。(6)、Ⅱ.亚氯酸钠是一种高效的漂白剂和消毒剂,它在酸性条件下生成并放出 , 有类似的性质。某兴趣小组探究亚氯酸钠的制备与性质。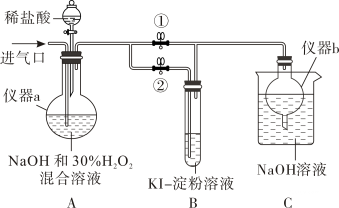
(Ⅰ)制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量 , 充分反应。
装置A中生成的离子方程式为。
(7)、(Ⅱ)探究亚氯酸钠的性质停止通气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因。
(8)、实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①,。
-
13、分类是一种重要的学习方法,对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。现有以下物质:
①熔融 ②Fe ③高锰酸钾 ④胶体 ⑤酒精
⑥漂白液 ⑦盐酸 ⑧石灰水 ⑨小苏打 ⑩溶液
(1)、以上物质中属于非电解质的是(填序号,下同),属于电解质的是 , 不能导电的有。(2)、写出②和⑦反应的离子方程式。(3)、已知氧化性:③ , 且③在酸性条件下被还原生成;写出③氧化⑦的浓溶液的化学方程式。(4)、写出⑨和少量的⑧反应的离子方程式。 -
14、表中除去物质中杂质选用的试剂或操作方法错误的是( )。
选项
物质
杂质
除去杂质选用的试剂或操作方法
A
铜粉
加入过量稀硫酸,并过滤
B
溶液
加入过量 , 并过滤
C
先后通过盛有足量溶液和浓硫酸的洗气瓶
D
溶液
加入适量溶液,并过滤
A、A B、B C、C D、D -
15、如图所示,试管b中盛有水,气球a中装有干燥的粉末,U形管中注有水。将气球用橡皮绳紧紧地系在试管口。实验时将气球中的粉末抖入试管b的水中,下列说法正确的是( )。
 A、U形管内的液面:c高于d B、该反应属于置换反应 C、过氧化钠在该反应中既作还原剂又作氧化剂 D、反应结束后(已反应完),立即往试管中滴加几滴无色酚酞试液,可观察到试管中溶液的颜色由无色变为红色
A、U形管内的液面:c高于d B、该反应属于置换反应 C、过氧化钠在该反应中既作还原剂又作氧化剂 D、反应结束后(已反应完),立即往试管中滴加几滴无色酚酞试液,可观察到试管中溶液的颜色由无色变为红色 -
16、下列有关氯气性质的说法正确的是( )。A、碱石灰是常用的气体干燥剂,也可用来干燥 B、具有很强的氧化性,但在化学反应中既能作氧化剂也能作还原剂 C、铁丝在氯气中燃烧,产生棕褐色的烟,加水溶解后,溶液呈红褐色 D、氯气通入水中能使有色布条褪色,说明氯气有漂白性
-
17、下列有关与的说法正确的是( )。A、除去中的可以通过对溶液进行加热 B、相同温度下的溶解性: C、不可用溶液将两者区分开来 D、与两种溶液,分别滴入酚酞,溶液红色一定更深
-
18、氯水中包含许多分子和离子,因此在化学反应中表现出不一样的性质,下列实验现象与结论正确的是( )。A、氯水能导电,氯水是电解质 B、溶液呈浅黄绿色,且具有刺激性气味,说明有分子存在 C、往氯水中滴加溶液产生气泡,因此氯水中含有 D、往一瓶氯水中加入酚酞试液没有任何现象,说明氯水已经变质
-
19、化学镀银实验中,常使用将转化为Ag,具有较强的还原性,在溶液中常被氧化成 , 下列选项中正确的是( )。A、反应中P元素化合价下降,被氧化 B、每生成一个粒子,反应中转移了3个电子 C、该反应中氧化产物为Ag D、还原产物与氧化产物的个数比为
-
20、将Na投入下列物质中,不能同时产生气体和沉淀的是( )。A、溶液 B、溶液 C、溶液 D、溶液